Clear Sky Science · fr
L’activation de NF-κB dans les astrocytes altère la cicatrisation après un traumatisme crânien chez la souris mâle
Pourquoi les contusions cérébrales ne cicatrisent pas toujours proprement
Lorsqu’une personne reçoit un coup à la tête, la blessure visible à l’extérieur ne raconte qu’une partie de l’histoire. Au cœur du cerveau, une réponse de réparation complexe se déploie et peut déterminer si la personne récupère bien ou développe des troubles durables de la cognition, de l’humeur ou du mouvement. Cette étude chez des souris mâles révèle comment une voie de stress clé, au sein des cellules de soutien appelées astrocytes, peut transformer une réponse de réparation normale en un processus qui aggrave en réalité les lésions après un traumatisme crânien.
Les premiers intervenants cachés du cerveau
Les astrocytes sont des cellules en forme d’étoile qui entourent les neurones et les vaisseaux sanguins, contribuant à maintenir l’homéostasie du milieu cérébral. Après une lésion crânienne, elles modifient rapidement leur morphologie et leur comportement, formant une barrière autour de la zone endommagée et participant à la reconstruction tissulaire. Les chercheurs se sont focalisés sur un interrupteur moléculaire au sein de ces cellules nommé NF-κB, connu pour réguler l’inflammation dans de nombreux tissus. Ils ont cherché à savoir si, après une lésion fermée du crâne comparable aux commotions et contusions humaines courantes, cet interrupteur aide ou nuit à la capacité du cerveau à cicatriser.
Un commutateur de stress qui s’allume après l’impact
En analysant l’activité génique dans le tissu cérébral de souris après la blessure, l’équipe a observé une montée des gènes liés à l’inflammation et à la signalisation NF-κB, particulièrement trois à sept jours après le traumatisme, période où les lésions secondaires augmentent. À l’aide de souris rapporteurs, ils ont montré que l’activation de NF-κB n’était pas diffuse dans tout le cerveau mais concentrée autour du site d’impact. Là, elle était particulièrement active dans les microglies (les sentinelles immunitaires du cerveau) et dans les astrocytes formant la bordure de la plaie. Ce timing et cette localisation ont suggéré que NF-κB dans les astrocytes pourrait être un régulateur critique de l’organisation de la cicatrice et du contrôle de la réponse immunitaire.
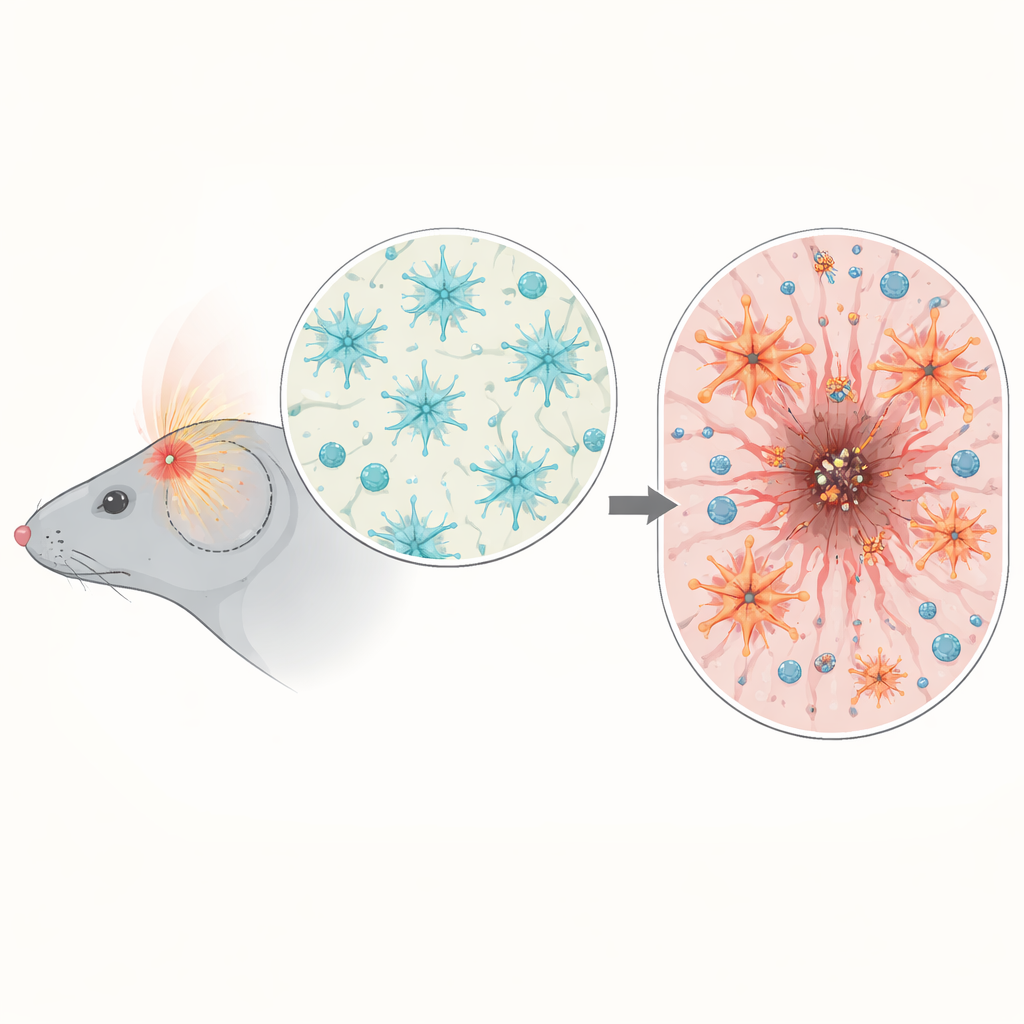
Une activation excessive des astrocytes
Pour tester la relation de cause à effet, les scientifiques ont conçu des souris dans lesquelles l’activité de NF-κB dans les astrocytes était soit artificiellement augmentée, soit diminuée, mais seulement après la fin du développement cérébral. Lorsque ces souris ont subi un traumatisme crânien, celles avec NF-κB hyperactif dans les astrocytes ont perdu plus de poids, présenté des scores neurologiques précoces plus mauvais et présenté des lésions cérébrales plus grandes et plus persistantes, visibles à la fois en coupe histologique et en IRM. Au lieu de former une cicatrice nette et bien définie qui isole le noyau endommagé, leurs astrocytes produisaient une bordure épaisse et désorganisée qui n’aidait pas à réduire la plaie avec le temps. L’équilibre normal des protéines de matrice autour de la blessure était perturbé et une structure barrière externe clé, connue sous le nom de limitante gliale, se formait mal, laissant le cerveau environnant moins protégé.
Quand les programmes de réparation déraillent
En examinant les détails moléculaires, l’équipe a isolé astrocytes et cellules immunitaires voisines pour une analyse gène par gène. Chez les animaux sains, la lésion supprime normalement certaines fonctions d’entretien des astrocytes tout en activant des gènes favorisant la fermeture de la plaie et la régénération. En revanche, les astrocytes avec NF-κB activé de façon chronique présentaient déjà un profil « blessé » avant même le traumatisme, et après l’impact ils n’ont pas réussi à activer pleinement les programmes de réparation bénéfiques, tels que ceux associés à une transformation contrôlée aidant les cellules à construire une bordure efficace. À la place, ils privilégiaient fortement les gènes inflammatoires, adoptaient des traits d’un état d’astrocyte toxique lié au vieillissement et aux maladies neurodégénératives, et montraient des signes d’un profil sécrétoire de type sénescence associé à des plaies chroniques non résolutives.
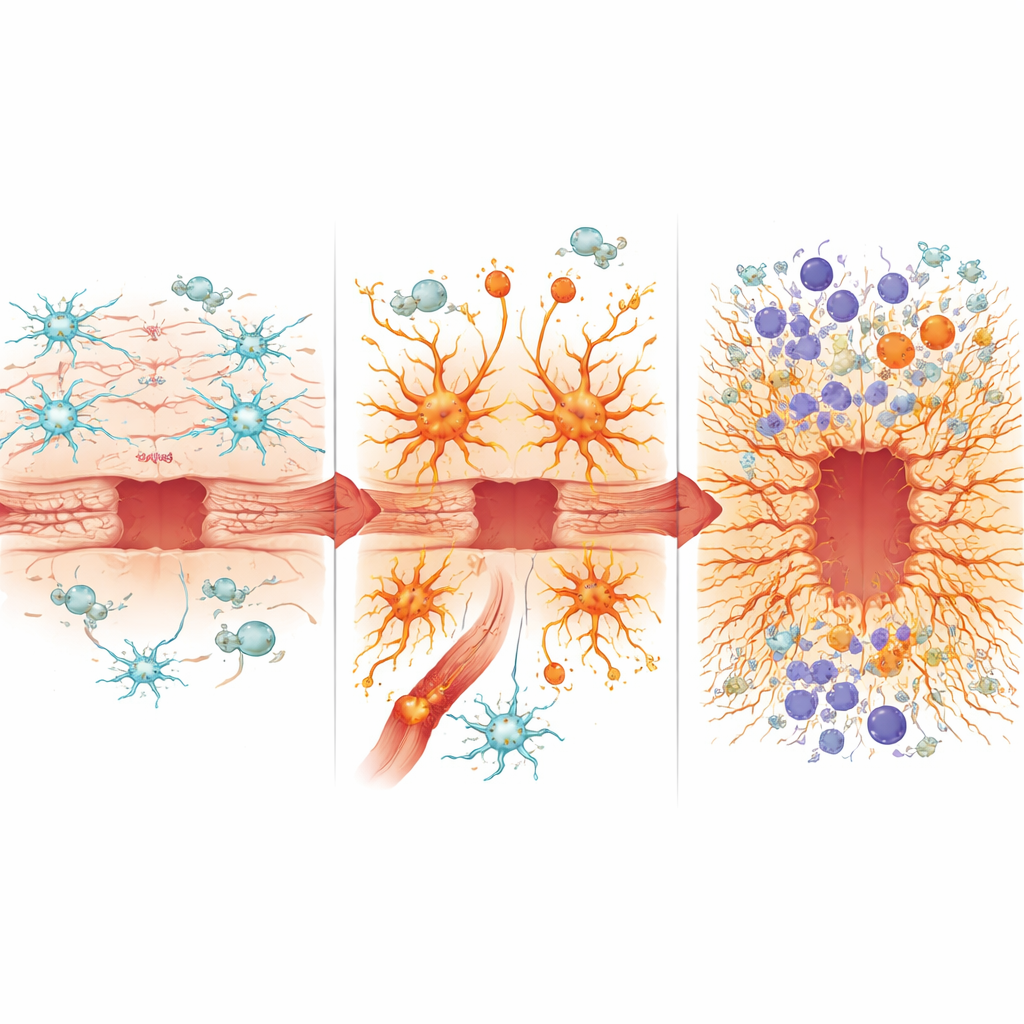
Alimenter l’incendie immunitaire
Ces astrocytes mal programmés ont aussi remodelé le paysage immunitaire du cerveau. La barrière hémato‑encéphalique devenait plus perméable, laissant entrer davantage de cellules immunitaires périphériques. Les souris avec NF-κB hyperactif dans les astrocytes présentaient une infiltration plus importante de cellules myéloïdes inflammatoires et des mélanges altérés de neutrophiles, monocytes et cellules dendritiques, ainsi qu’une augmentation des lymphocytes T cytotoxiques pouvant aggraver les lésions tissulaires. Dans cet environnement, les cellules immunitaires exprimaient des signaux renforcés pilotés par les voies de l’interféron et de l’inflammasome, toutes deux associées à une inflammation agressive et potentiellement neurotoxique. Parallèlement, les niveaux de plusieurs protéines protectrices ou pro‑réparation, comme l’ostéopontine, étaient réduits, tandis que d’autres liées au stress oxydatif, à la surcharge en fer et à la cicatrisation, dont l’hème oxygénase‑1 et la lipocaline‑2, étaient élevés. Le ratio entre ostéopontine et lipocaline‑2 est apparu comme un marqueur simple corrélant avec une meilleure ou pire cicatrisation selon les souches de souris.
Ce que cela signifie pour la récupération après traumatisme crânien
Pris ensemble, les résultats montrent que lorsque la voie de stress NF-κB dans les astrocytes reste chroniquement activée, ces cellules passent d’un soutien à la réparation organisée à une promotion d’une cicatrisation chaotique et d’une inflammation prolongée. Plutôt que de construire une bordure propre qui contient les dommages et permet le remodelage tissulaire, elles contribuent à créer un microenvironnement fuyant et inflammatoire qui agrandit la lésion et compromet le pronostic à long terme. Bien que le travail ait été réalisé chez des souris mâles, il désigne NF-κB astrocytaire comme une cible prometteuse pour des thérapies visant à améliorer la récupération après traumatisme crânien et suggère que les concentrations sanguines de molécules telles que l’ostéopontine et la lipocaline‑2 pourraient un jour aider les cliniciens à suivre la qualité de la cicatrisation cérébrale d’un patient.
Citation: Hein, T.M., Nespoli, E., Hakani, M. et al. NF-κB activation in astrocytes impairs wound healing after traumatic brain injury in male mice. Nat Commun 17, 2323 (2026). https://doi.org/10.1038/s41467-026-70304-7
Mots-clés: traumatisme crânien, astrocytes, neuroinflammation, formation de cicatrice cérébrale, NF-kappa B