Clear Sky Science · fr
NAA40 et NAC coopèrent pour l’acétylation cotraductionnelle des histones chez l’homme
Comment les cellules ajustent finement leurs interrupteurs génétiques
À l’intérieur de chaque cellule humaine, les protéines nouvellement synthétisées subissent de petites modifications chimiques au fur et à mesure qu’elles sortent des machines à fabriquer les protéines, les ribosomes. Ces ajustements peuvent déterminer la destination d’une protéine, sa durée de vie et même la façon dont nos gènes sont activés ou réprimés. Cet article se concentre sur une enzyme très spécifique, NAA40, et sur un complexe assistant nommé NAC, révélant comment ils coopèrent sur le ribosome pour modifier les histones — les enrouleurs autour desquels l’ADN est emballé — et influer ainsi sur l’activité génique et, potentiellement, sur le développement du cancer.
Un petit capuchon qui change le comportement des histones
Beaucoup de protéines humaines reçoivent une petite « coiffe » chimique à leur extrémité N-terminale, un processus appelé acétylation N-terminale. Les histones H2A et H4, qui contribuent à empaqueter l’ADN en chromatine, sont presque toujours modifiés de cette manière. NAA40 est inhabituelle parmi les enzymes car elle se spécialise presque exclusivement dans l’ajout de cette coiffe sur ces histones pendant leur synthèse. Cette marque d’acétylation entre en compétition avec d’autres modifications chimiques, comme la phosphorylation et la méthylation, sur la même région des histones ; l’action ou l’absence d’action de NAA40 peut donc modifier la compaction de l’ADN et la régulation des gènes. De façon importante, des altérations du niveau de NAA40 ont été associées à plusieurs cancers, ce qui en fait une cible prometteuse pour de nouvelles thérapies.
Un partenariat à la porte de l’usine à protéines
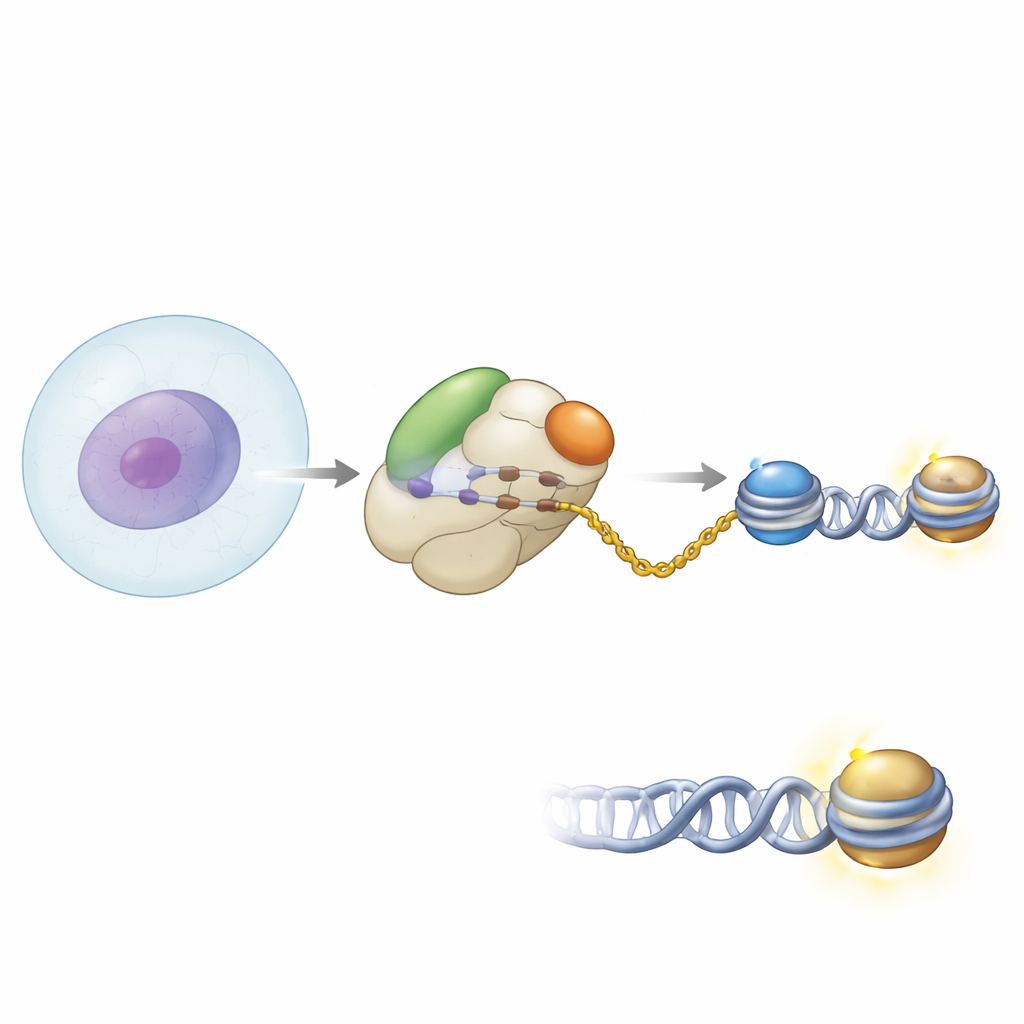
Les auteurs ont utilisé des méthodes biochimiques et la cryo‑microscopie électronique à haute résolution pour visualiser la position de NAA40 sur le ribosome humain. Ils ont découvert que NAA40 se place juste à la sortie du tunnel où émergent les chaînes polypeptidiques naissantes. Là, elle ne travaille pas seule : elle se lie aux côtés du complexe associé aux polypeptides naissants, ou NAC, un assistant courant fixé au ribosome qui surveille les nouvelles protéines à leur sortie. Des clichés structuraux ont montré que NAA40 est ancrée au ribosome par un segment hélicoïdal chargé positivement à son extrémité N‑terminale, tandis que NAC est attaché via l’une de ses sous‑unités à la surface ribosomale. Un domaine flexible de NAC s’étend pour contacter NAA40, faisant ainsi le pont entre l’enzyme et le ribosome.
Pourquoi NAC est nécessaire pour l’ajustement des histones
Pour tester l’importance de ce partenariat, les chercheurs ont reconstitué ces interactions avec des composants purifiés en éprouvette. Ils ont observé que NAA40 seule se lie faiblement aux ribosomes, mais qu’en présence de NAC, la liaison au ribosome devient beaucoup plus forte. Si l’on supprime une région « UBA » spécifique de NAC qui contacte NAA40, cette liaison renforcée disparaît. Dans des cellules humaines, l’épuisement de NAC a entraîné une diminution de l’acétylation de l’histone H4 dépendante de NAA40 et une augmentation correspondante d’une marque de phosphorylation concurrente sur la même queue d’histone. Ce changement est survenu sans modification de la quantité ou de la localisation de NAA40 elle‑même, indiquant que le rôle principal de NAC est de recruter et de positionner correctement NAA40 sur les ribosomes en traduction afin que les histones puissent être modifiés efficacement au moment de leur synthèse.
Une chaîne de production coordonnée pour le traitement des histones
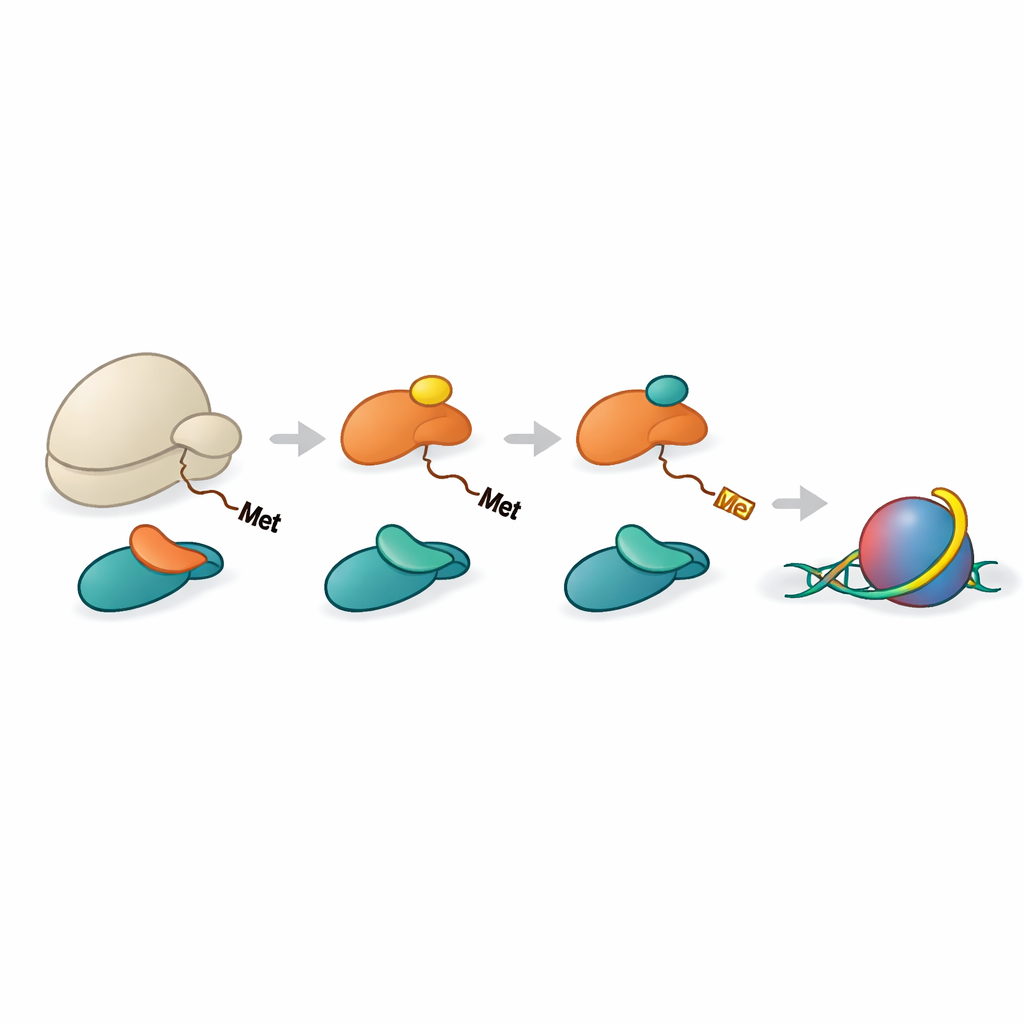
Les histones H2A et H4 doivent d’abord perdre leur acide aminé méthionine initial avant que NAA40 puisse les reconnaître. Une autre enzyme, METAP1, effectue ce raccourcissement. L’équipe a montré que NAC peut aider à rapprocher METAP1 et NAA40 du ribosome, formant une assemblée multi‑enzymatique à la sortie peptidique. Des structures à haute résolution de complexes reconstitués ont révélé METAP1 et NAA40 liés côte à côte sur le ribosome, avec leurs sites actifs positionnés à des distances presque égales du tunnel de sortie. Cette géométrie signifie que, dès que la queue d’un histone dépasse d’une douzaine d’acides aminés environ, METAP1 peut enlever la méthionine initiale et NAA40 peut immédiatement ajouter la coiffe acétyle, minimisant tout délai entre les deux étapes.
Conséquences pour le contrôle génétique et le cancer
Globalement, l’étude montre que NAA40 ne se contente pas de flotter dans la cellule à la recherche d’histones à modifier. Au contraire, elle est ancrée au ribosome par NAC, formant une station de traitement organisée qui prépare les histones au moment même de leur synthèse. En couplant étroitement le retrait de la méthionine et l’ajout de l’acétylation, la cellule veille à ce que les histones H2A, H4 et la variante liée aux dégâts de l’ADN H2A.X reçoivent rapidement une marque d’acétylation susceptible de façonner la structure de la chromatine et l’expression des gènes. Parce que les perturbations de cette étape précoce de marquage des histones peuvent favoriser la croissance cancéreuse, comprendre l’agencement précis de NAA40, NAC et METAP1 sur le ribosome fournit un plan structural qui pourrait guider la conception de médicaments visant à ajuster ce point de contrôle épigénétique critique.
Citation: Guan, D., Denk, T., Klavaris, A. et al. NAA40 and NAC cooperate in co-translational histone acetylation in humans. Nat Commun 17, 2486 (2026). https://doi.org/10.1038/s41467-026-70279-5
Mots-clés: acétylation des histones, NAA40, ribosome, complexe associé aux polypeptides naissants, régulation épigénétique