Clear Sky Science · fr
Une transition dépendante du cycle cellulaire, de l’acétylation vers la phosphorylation, régule la maturation chronométrée du centrosome
Maintenir notre cargaison génétique sur la bonne voie
Chaque fois qu’une cellule de notre organisme se divise, elle doit répartir son ADN avec une précision extrême. Lorsque ce processus déraille, les cellules peuvent gagner ou perdre des chromosomes, un état dangereux associé au cancer et à d’autres pathologies. Cette étude révèle un dispositif moléculaire de synchronisation qui aide les cellules à assembler les petites structures nécessaires pour séparer correctement les chromosomes, dévoilant une vulnérabilité potentielle que les thérapies anti-cancer futures pourraient exploiter.
Les petits carrefours du trafic cellulaire
Au cœur de chaque cellule en division se trouvent les centrosomes, de petites structures qui jouent le rôle de carrefours pour les fibres qui tirent les chromosomes. Avant qu’une cellule n’entre en division, ces carrefours doivent « mûrir » : ils s’enrichissent en protéines auxiliaires et deviennent de puissants organiseurs de microtubules, ces fibres dynamiques qui forment le fuseau de division. Si cette maturation survient trop tôt, trop tard ou pas du tout, les chromosomes peuvent être mal répartis, conduisant à des cellules au nombre de chromosomes anormal. Comprendre comment les cellules déclenchent la mise en marche des centrosomes au bon moment est une question de longue date en biologie cellulaire.
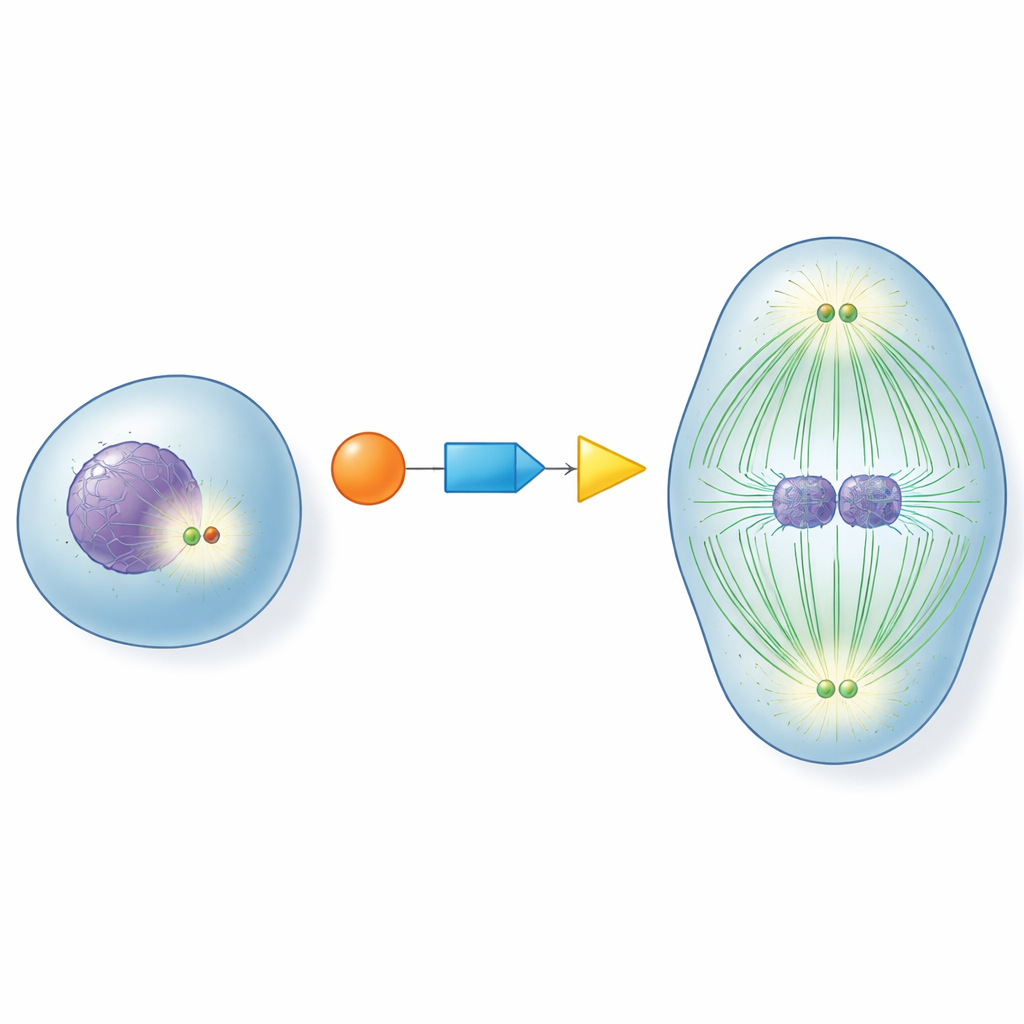
Un relais moléculaire pour une synchronisation parfaite
Les auteurs se sont concentrés sur trois protéines clés qui agissent en relais : CDK1, un maître régulateur du cycle cellulaire ; RNF40, connu jusqu’ici surtout pour modifier les protéines d’emballage de l’ADN ; et PLK1, un moteur majeur de la division cellulaire. Ils ont découvert que RNF40 est physiquement présent aux centrosomes tout au long du cycle cellulaire et se lie directement à PLK1. À l’approche de la division, CDK1 marque chimiquement RNF40 en deux points précis, ce qui rend RNF40 meilleur site d’ancrage pour PLK1. Cette chaîne CDK1–RNF40–PLK1 garantit que PLK1 arrive aux centrosomes précisément pendant la phase finale de préparation à la division, déclenchant une maturation robuste des centrosomes, la croissance des microtubules et l’assemblage d’un fuseau bipolaire bien formé.
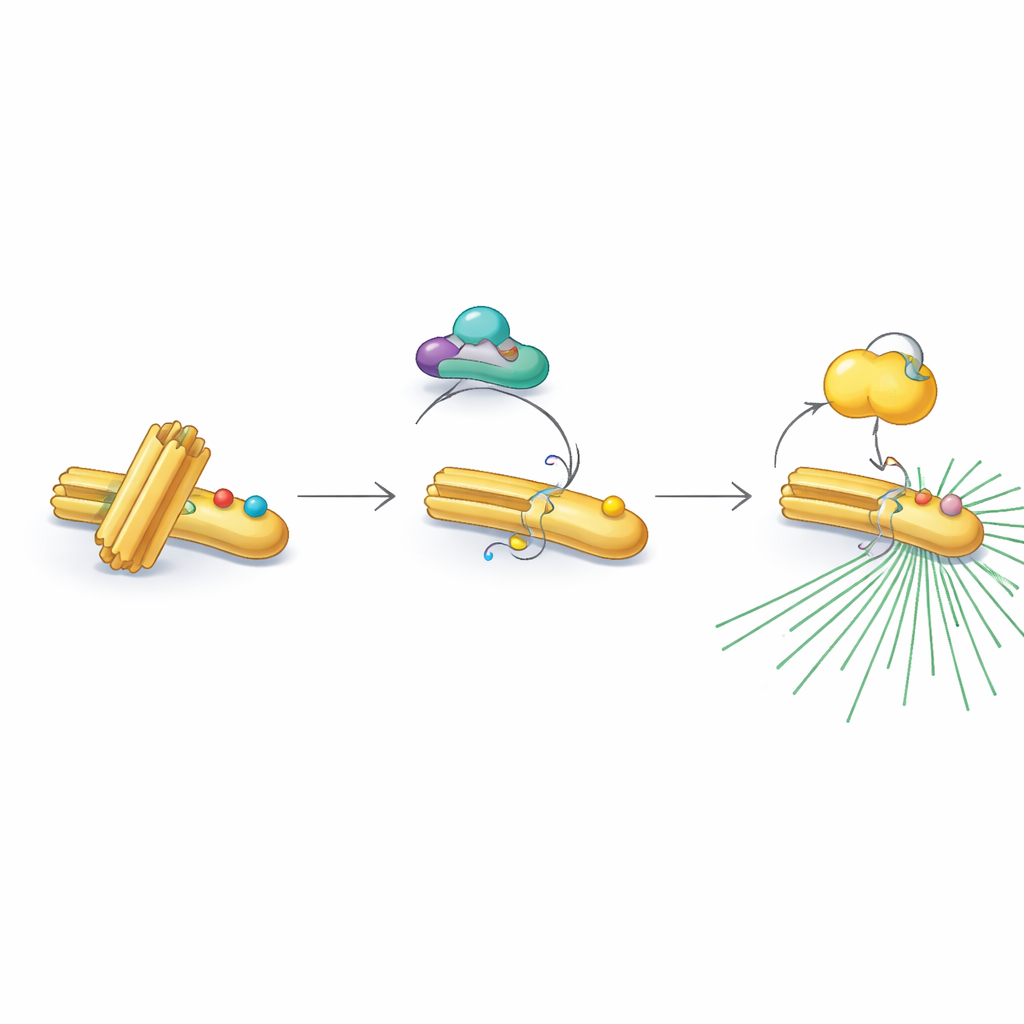
Un interrupteur protéique qui change de forme
De façon intrigante, RNF40 n’accepte pas toujours ces marques activatrices. Dans les phases non divisantes et de réplication de l’ADN, RNF40 porte une autre modification chimique — des groupes acétyle — sur deux positions voisines. Ces marques d’acétylation sont ajoutées par une enzyme appelée PCAF et retirées ensuite par un partenaire déacétylase, HDAC1. La forme acétylée de RNF40 résiste à la modification par CDK1, bloquant effectivement l’étape suivante du relais. Lorsque les cellules entrent dans la dernière phase pré-division, HDAC1 efface progressivement les marques d’acétylation, permettant à CDK1 d’ajouter des groupes phosphate à la place. Ce passage minuté de l’acétylation à la phosphorylation convertit RNF40 d’un état « en veille » à un état « activé », prêt à recruter PLK1 et à mettre sous tension le centrosome.
Que se passe-t-il quand la synchronisation échoue
Pour tester l’importance de cet interrupteur, les chercheurs ont conçu des cellules dans lesquelles RNF40 ne pouvait plus être phosphorylé, ou qui étaient contraintes de rester dans un état mimant l’acétylation. Dans les deux cas, PLK1 n’a pas pu s’accumuler correctement aux centrosomes. Ces cellules présentaient une croissance des microtubules affaiblie à partir des centrosomes, des fuseaux mal formés et des chromosomes mal alignés. Nombre d’entre elles ont fini avec des chromosomes en trop ou manquants — une condition anormale appelée aneuploïdie — et certaines sont devenues binoyautées, signes d’erreurs catastrophiques de division. Dans des modèles de cancer, les cellules verrouillées dans l’état « acétylé » de RNF40 formaient des tumeurs plus petites chez la souris et étaient plus sensibles aux chimiothérapies courantes utilisées contre le cancer colorectal, ce qui suggère que perturber cet interrupteur peut ralentir la croissance tumorale.
Liens avec le cancer humain et perspectives
L’équipe a également examiné des données de patients et des échantillons tumoraux. Ils ont constaté que RNF40 est souvent anormalement abondant dans les cancers colorectaux et que certaines mutations associées au cancer, situées près de ses sites de modification, perturbent sa phosphorylation, compromettant ainsi la fonction correcte des centrosomes. Ces observations relient directement le mécanisme de synchronisation nouvellement décrit à la maladie humaine. En identifiant une protéine spécifique qui coordonne le moment de la maturation des centrosomes et la séparation des chromosomes, l’étude met en lumière un « nœud » de signalisation qui pourrait être ciblé pour pousser les cellules cancéreuses à division rapide vers des erreurs fatales, tout en épargnant davantage les cellules saines.
Une nouvelle poignée pour une division cellulaire fidèle
Pour les non-spécialistes, le message clé est que les cellules reposent sur un interrupteur chimique finement réglé porté par une seule protéine, RNF40, pour décider précisément quand activer la machinerie qui sépare les chromosomes. Cette transition de l’acétylation vers la phosphorylation agit comme un feu de circulation à une intersection très fréquentée, devenant vert seulement lorsque la cellule est vraiment prête à se diviser. Lorsque le feu dysfonctionne, les cellules trébuchent pendant la division, accumulent des erreurs génétiques et peuvent devenir cancéreuses. Comprendre et contrôler cet interrupteur pourrait ouvrir de nouvelles voies thérapeutiques visant à déstabiliser sélectivement les cellules cancéreuses en sabotant leur capacité à se diviser proprement.
Citation: Li, J., Liang, J., Chen, G. et al. A cell cycle-dependent transition of acetylation to phosphorylation regulates timely centrosome maturation. Nat Commun 17, 2583 (2026). https://doi.org/10.1038/s41467-026-70271-z
Mots-clés: maturation du centrosome, division cellulaire, instabilité chromosomique, signalisation PLK1, cancer colorectal