Clear Sky Science · fr
Réacteur électrochimique intégré à électrolyte solide poreux et réacteur à lit fixe pour la synthèse efficace du précurseur du nylon‑6
Des éléments constitutifs plus propres pour les plastiques du quotidien
Le nylon‑6 est présent dans d’innombrables produits, des moquettes et vêtements aux pièces automobiles. Pourtant, les étapes chimiques utilisées pour fabriquer son ingrédient clé, l’oxime de cyclohexanone, reposent encore sur des substances toxiques et des procédés énergivores. Cette étude présente une méthode continue plus propre qui produit la même molécule cruciale en n’utilisant que l’air, l’eau, l’électricité et l’ammoniac — offrant une voie pour réduire l’empreinte environnementale d’une grande industrie des plastiques.
Pourquoi la filière actuelle du nylon pose problème
Les usines conventionnelles fabriquent l’oxime de cyclohexanone en faisant réagir la cyclohexanone avec de l’hydroxylamine, un composé à la fois instable et potentiellement explosif. Pour le maîtriser, l’industrie ajoute des acides forts puis les neutralise ensuite, générant de grandes quantités de déchets salins et augmentant les coûts. Des voies alternatives « plus vertes » ont tenté de générer l’hydroxylamine directement à partir d’oxydes d’azote dans une cellule électrochimique, mais ces méthodes tendent à sur‑réduire l’azote en ammoniac ordinaire, gaspillant de l’énergie et limitant la quantité de produit utile obtenue par unité d’électricité.
Un dispositif en deux étapes, emboîtable
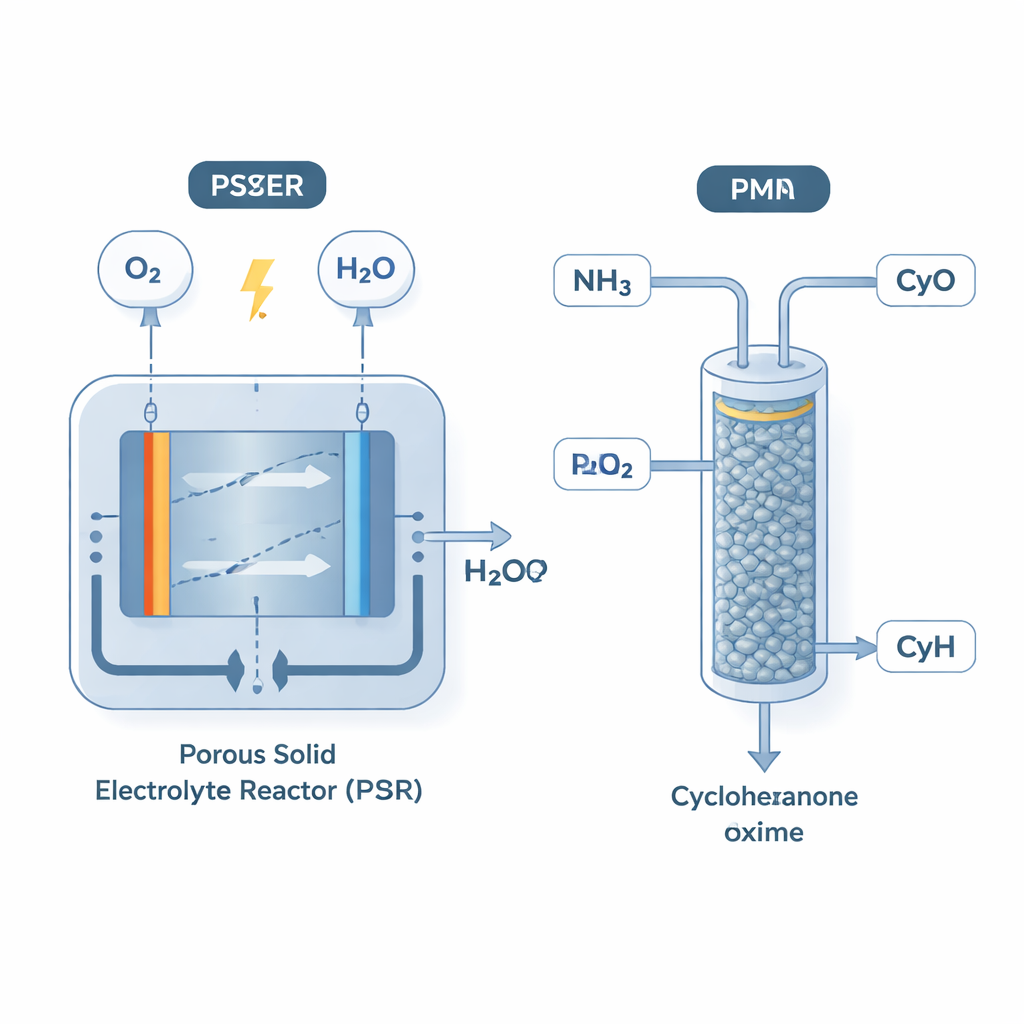
Les auteurs abordent le problème en le séparant en deux unités étroitement liées. D’abord, ils utilisent un réacteur à électrolyte solide poreux (PSER) pour convertir l’oxygène de l’air et l’eau en peroxyde d’hydrogène grâce à l’électricité. Cet appareil est construit avec trois chambres et des membranes spéciales de sorte que la solution de peroxyde qui en sort est très pure et contient presque pas de sels ou d’additifs stabilisants. Ensuite, ils alimentent ce peroxyde fraîchement produit, avec la cyclohexanone et l’ammoniac, dans un réacteur à lit fixe (PBR) rempli d’un catalyseur commercial appelé TS‑1, déjà utilisé en industrie. À l’intérieur du tube empilé, le peroxyde et l’ammoniac forment sur place l’hydroxylamine, qui réagit immédiatement avec la cyclohexanone pour donner l’oxime souhaitée.
Rendements élevés à des débits pertinents industriellement
Travaillant d’abord sur chaque unité séparément, l’équipe a ajusté températures, quantités de catalyseur et choix de solvants dans le réacteur à lit fixe pour maximiser la production d’oxime de cyclohexanone à partir d’un flux donné. Ils ont constaté qu’un fonctionnement autour de 80 °C avec des concentrations de réactifs soigneusement choisies donnait une conversion élevée de la cyclohexanone et très peu de produits secondaires. Côté électrochimie, ils ont porté le PSER à 25 centimètres carrés — six fois la taille de leur conception antérieure — et ont montré qu’il pouvait générer en continu du peroxyde d’hydrogène à des concentrations modulables simplement en modifiant le courant électrique, tout en conservant une efficacité électrique élevée.
Meilleure performance que le peroxyde commercial et réduction des coûts
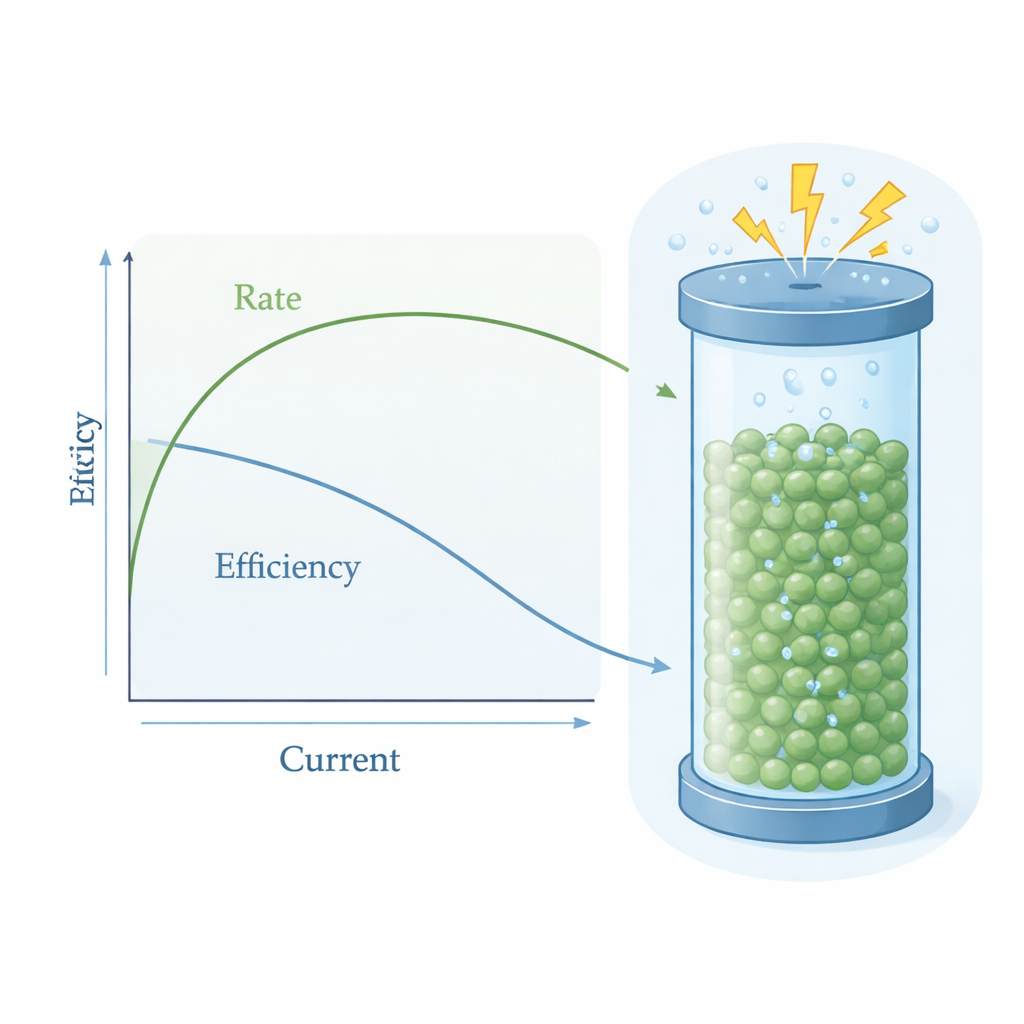
Lorsque les deux unités ont été connectées, le système a produit en continu de l’oxime de cyclohexanone avec des performances remarquables. À courant modéré, le procédé a converti plus de 96 % de la cyclohexanone de départ, atteint plus de 97 % de sélectivité pour l’oxime désirée, et utilisé plus de 96 % du peroxyde d’hydrogène généré — mieux que lors de l’utilisation de peroxyde commercial stabilisé par des additifs. À des courants plus élevés, d’intérêt industriel, le taux de production est monté à 28,3 millimoles par heure sur l’appareil à l’échelle laboratoire, bien au‑dessus des approches précédentes, même si une partie de l’efficacité est perdue parce que le peroxyde concentré se décompose en bulles d’oxygène. Une analyse techno‑économique suggère que, sous des prix raisonnables de l’électricité, cette approche pourrait produire le précurseur du nylon‑6 à environ un quart de son prix de marché actuel, principalement parce qu’elle utilise de l’ammoniac peu coûteux et du peroxyde sur site au lieu de réactifs onéreux et d’étapes de séparation complexes.
Au‑delà d’une seule molécule, vers des usines plus vertes
Pour montrer que leur installation n’est pas une méthode limitée, les chercheurs ont appliqué la même combinaison PSER‑PBR à une gamme d’autres cétones et démontré qu’elle pouvait former plusieurs oximes différentes avec une forte sélectivité. Des essais de longue durée sur de nombreuses heures ont montré une opération stable et une qualité de produit constante, et le design modulaire du lit fixe permettrait aux opérateurs industriels d’échanger et de régénérer des cartouches catalytiques sans arrêter toute la ligne. Pour un non‑spécialiste, la conclusion est simple : en couplant étroitement une source d’oxydant propre et pilotée par l’électricité à un réacteur chimique robuste, ce travail ouvre la voie à un avenir où les ingrédients clés des plastiques sont fabriqués de manière plus sûre, plus efficace et avec beaucoup moins de déchets.
Citation: Zhang, SK., Feng, Y., Hao, S. et al. Integrated electrochemical porous solid electrolyte reactor and packed bed reactor for efficient synthesis of nylon-6 precursor. Nat Commun 17, 2163 (2026). https://doi.org/10.1038/s41467-026-70236-2
Mots-clés: nylon‑6, chimie verte, réacteur électrochimique, peroxyde d’hydrogène, oxime de cyclohexanone