Clear Sky Science · fr
Sélection de voie entre réactions click et transfert d’acyle pilotée par des phosphates aminoacylés
Pourquoi le timing compte en chimie quotidienne
À l’intérieur de chaque cellule, des molécules importantes sont synthétisées et modifiées dans un ordre très précis, comme les étapes d’une recette. Ce calendrier détermine si une protéine s’active, se désactive ou change de conformation. Les chimistes cherchent à imiter ce type d’ordonnancement intégré avec de petites molécules non vivantes en milieu aqueux, sans recourir aux enzymes ni à des déclencheurs externes tels que la lumière ou des sauts de pH. Cet article décrit un système réactionnel artificiel qui fait exactement cela : il utilise la structure de petits peptides et une réaction de liaison populaire de la « chimie click » pour décider quelle étape chimique se produit en premier et laquelle doit attendre son tour.
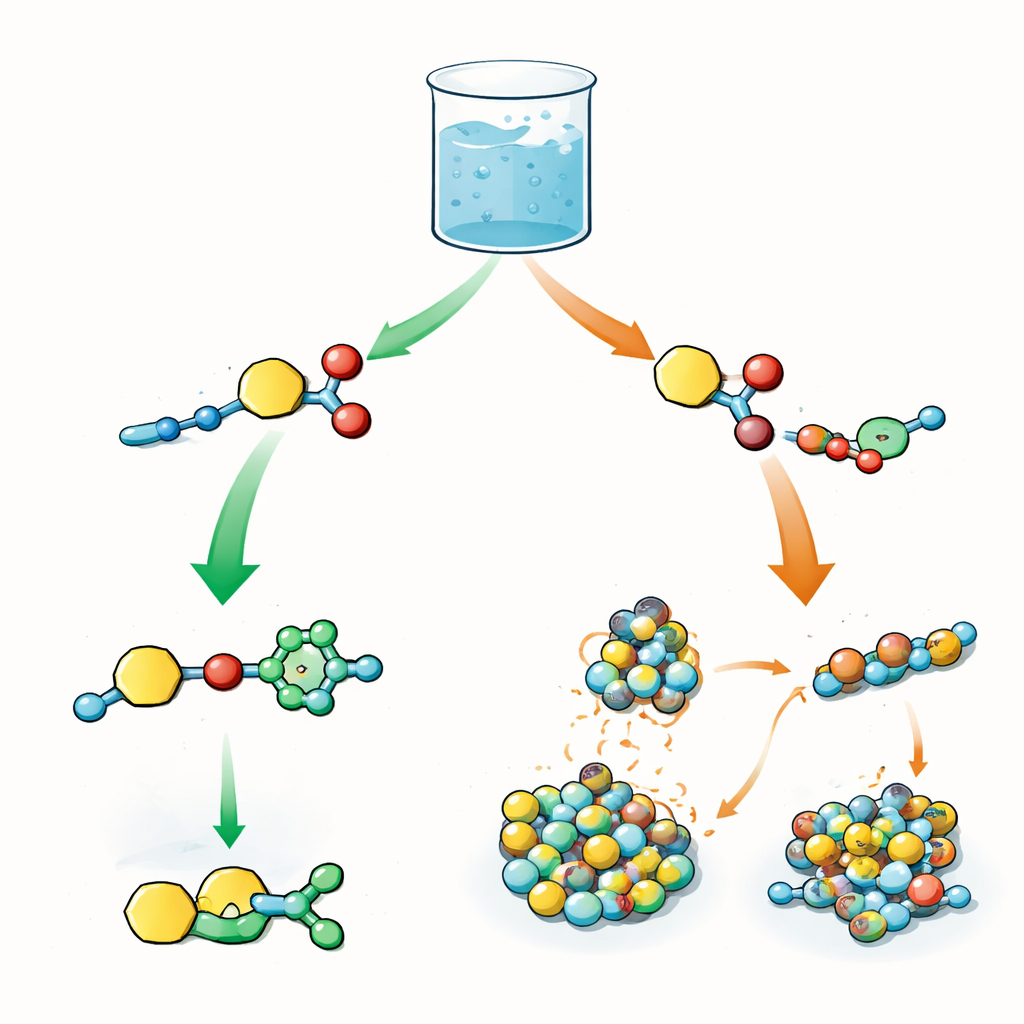
Deux réactions rivales dans un même pot
Les auteurs conçoivent un bloc de construction central portant deux fonctionnalités réactives : l’une capable de transférer un groupe acyle (un petit fragment chimique souvent utilisé pour modifier des protéines) et l’autre pouvant subir une réaction click appelée cycloaddition azide‑alcynyle catalysée par le cuivre. Dans le même bécher, ce bloc est mélangé avec des azides et de courts peptides jouant le rôle de nucléophiles, c’est‑à‑dire qu’ils captent le groupe acyle. En biologie, l’ordre de telles étapes — activation, transfert et modifications ultérieures — contrôle le comportement des protéines. Ici, la question est similaire : lorsque les deux réactions sont possibles simultanément, le système choisit‑il d’abord la click, d’abord le transfert d’acyle, ou un mélange des deux ?
Oxygène lent, soufre rapide
L’équipe étudie d’abord des peptides contenant de la tyrosine, un acide aminé avec une chaîne latérale oxygénée. Dans des conditions faiblement basiques, la réaction click prend rapidement l’avantage : l’alcyne et l’azide se joignent vite, tandis que le transfert d’acyle sur la chaîne latérale de la tyrosine est lent et n’accumule guère d’intermédiaires détectables. Plusieurs produits dérivés de la click coexistent, et il y a peu d’écart temporel net entre les étapes. Lorsque les chercheurs passent à la cystéine, un acide aminé à chaîne latérale sulfurée, la situation s’inverse. La cystéine forme rapidement des thioesters — des produits acylés liés au soufre — qui apparaissent en rendement élevé bien avant tout produit issu de la click. Ce n’est qu’après plusieurs heures que des produits click commencent à émerger. Ce basculement vient du fait que le soufre réagit non seulement plus volontiers mais se lie aussi aux ions cuivre, immobilisant le catalyseur et « suspendant » temporairement la voie click.
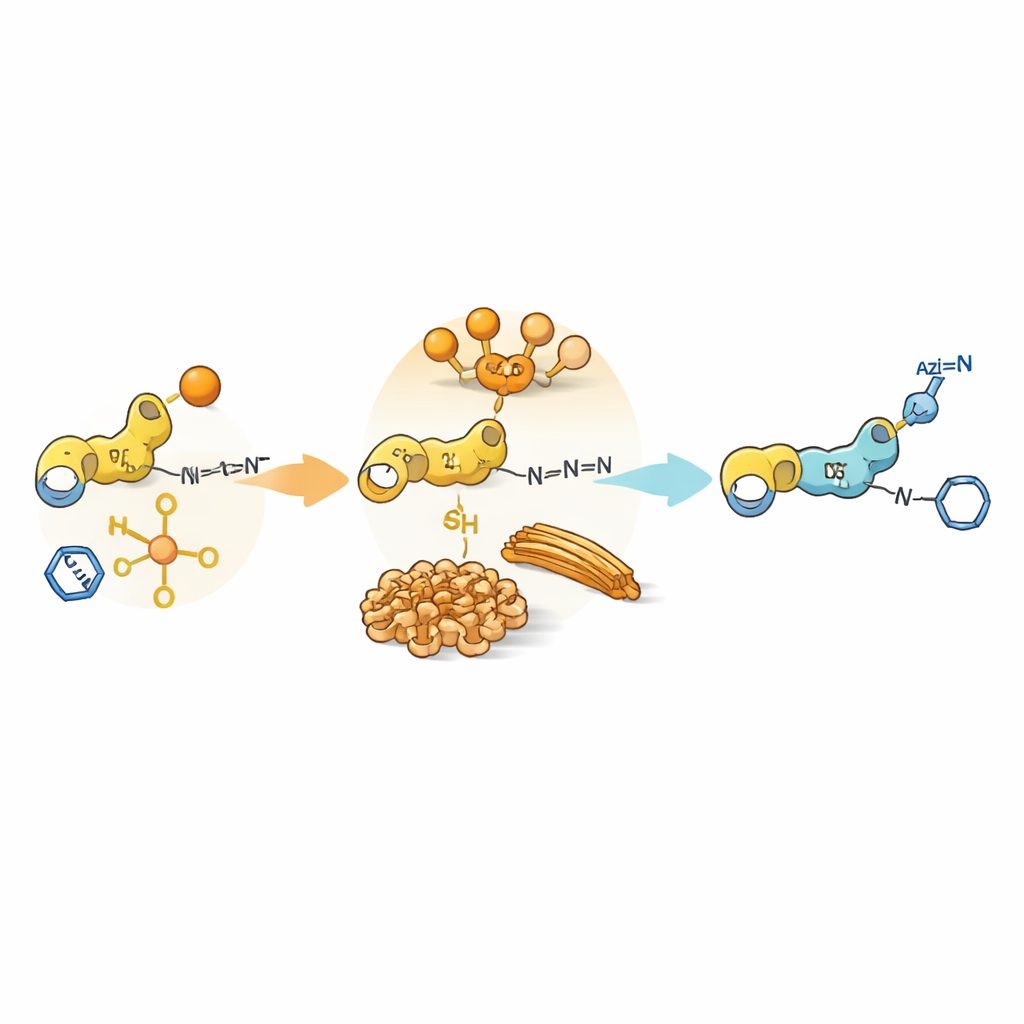
L’auto‑assemblage comme verrou chimique
Au‑delà de la simple réactivité, les peptides eux‑mêmes peuvent s’agglomérer en structures plus grandes, formant des gels mous ou des fibres en milieu aqueux. Ces assemblages créent de petits domaines où certains partenaires sont concentrés et d’autres exclus. Pour certains dipeptides contenant de la tyrosine ou de la cystéine et portant des groupes aromatiques supplémentaires, les intermédiaires s’auto‑assemblent en fibrilles ou en particules denses. À l’intérieur de ces régions compactes, le transfert d’acyle est favorisé parce que le nucléophile et le donneur d’acyle se trouvent côte à côte, tandis que l’azide et le catalyseur à base de cuivre restent principalement en solution environnante. En conséquence, bien que la réaction click soit intrinsèquement rapide en solution libre, elle est ralentie par la nécessité d’atteindre des sites réactifs enfouis. Ce « décalage de phase » entre l’emplacement du catalyseur et celui des substrats prolonge la durée de vie des intermédiaires acylés et retarde le déclenchement de la chimie click.
Programmer des cascades et des choix
Pour tester l’étendue de ce planificateur intégré, les auteurs conçoivent des situations plus complexes. Dans un cas, un seul peptide contient à la fois cystéine et tyrosine, offrant deux sites de transfert d’acyle différents. La réaction suit alors une cascade en trois étapes : d’abord un thioester se forme sur la cystéine, puis un second groupe acyle migre sur la tyrosine, et ce n’est qu’après ces étapes que des produits click apparaissent. Dans une autre série d’expériences, deux azides différents — l’un flexible et aliphatique, l’autre rigide et aromatique — entrent en compétition pour le même centre réactif. De manière surprenante, le système favorise systématiquement l’azide aliphatique, révélant que même la forme et le caractère électronique de l’azide peuvent biaiser les produits dominants, tandis que le calendrier du transfert d’acyle reste sous le contrôle du peptide.
Ce que cela signifie pour les matériaux intelligents de demain
En langage courant, ce travail montre comment on peut intégrer plusieurs réactions potentiellement concurrentes dans un même mélange aqueux simple et les faire s’enclencher dans un ordre prédéfini — sans enzymes, pompes ni interrupteurs externes. En choisissant si un peptide porte de l’oxygène ou du soufre, en modulant sa tendance à s’auto‑assembler et en ajustant la nature du partenaire azide, les auteurs codent une sorte d’horloge interne dans un petit réseau chimique. Des transferts d’acyle précoces et réversibles créent des intermédiaires de courte durée qui déterminent quand et comment l’étape click robuste et quasi irréversible a lieu. De telles séquences programmées pourraient servir de base à des matériaux intelligents et à des réseaux réactionnels synthétiques qui « décident » leurs propres voies au fil du temps, à la manière de la chimie minutieusement ordonnancée des cellules vivantes.
Citation: Bhattacharjee, D., Sharma, A., Dai, K. et al. Pathway selection between click and acyl transfer reactions driven by aminoacyl phosphates. Nat Commun 17, 2407 (2026). https://doi.org/10.1038/s41467-026-70199-4
Mots-clés: chimie click, transfert d’acyle, auto‑assemblage supramoléculaire, réseaux de réactions, chimie peptidique