Clear Sky Science · fr
Cartographie moléculaire en DNA-PAINT via un modèle de mélange gaussien modifié
Voir le monde invisible des molécules
La biologie moderne repose de plus en plus sur des microscopes capables de voir non seulement des cellules, mais aussi des molécules individuelles en leur sein. Transformer la lumière faible et intermittente émise par ces molécules en une « carte » fiable de leur position est pourtant étonnamment difficile. Cette étude présente une nouvelle méthode computationnelle, baptisée G5M, qui rend ces cartes moléculaires beaucoup plus précises et détaillées, aidant les biologistes à comprendre comment les protéines sont disposées et groupées dans des cellules réelles, à l'échelle de quelques milliardièmes de mètre.
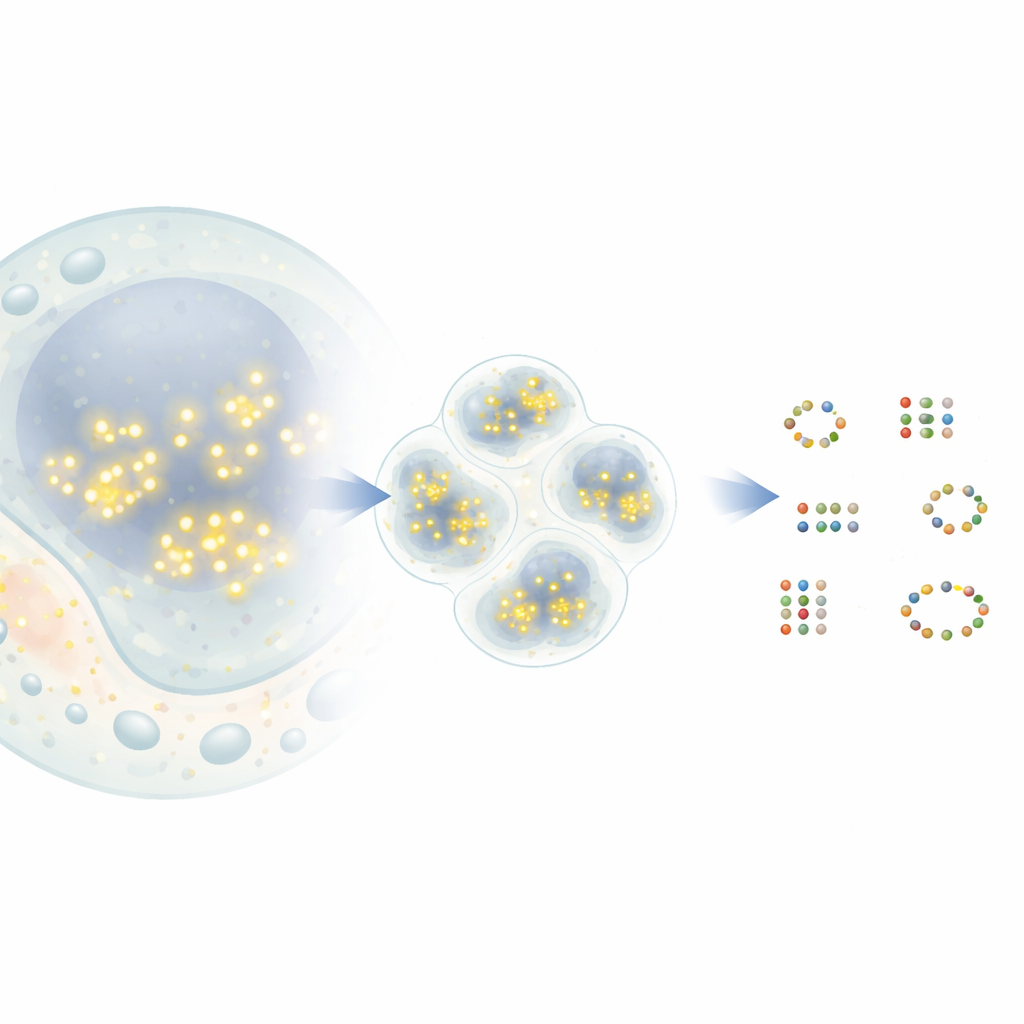
Des points qui clignotent aux cartes moléculaires
Dans une technique de super‑résolution populaire appelée DNA‑PAINT, de courts brins d'ADN portant des colorants fluorescents se lient et se détachent brièvement à des étiquettes d'ADN appariées fixées aux protéines cibles. À chaque liaison, le colorant apparaît comme un point lumineux dans le microscope avant de disparaître. Au fil du temps, de nombreux événements forment un nuage de points autour de chaque protéine. En principe, le centre de chaque nuage indique la position réelle d'une protéine avec une précision nanométrique. En pratique, toutefois, les points issus de protéines proches peuvent se chevaucher, et certains proviennent de signaux de fond aléatoires. Les outils d'analyse existants fusionnent souvent des voisins proches en une seule protéine ou, au contraire, inventent des protéines inexistantes, limitant ainsi les informations biologiques exploitables.
Une méthode plus intelligente pour détecter les vraies molécules
La nouvelle méthode, G5M, considère l'essaim de points comme un mélange de nuages simples en forme de cloche, chacun correspondant à une molécule réelle. Plutôt que de se contenter de regrouper les points proches selon leur densité, G5M utilise un modèle probabiliste qui intègre ce que l'on sait déjà de l'expérience : la précision des mesures de position, la cinétique de liaison/déliaison des brins d'ADN, et la façon dont le microscope floute la lumière en deux ou trois dimensions. Il teste ensuite différentes explications possibles — différents nombres et formes de nuages — et choisit automatiquement celle qui équilibre le mieux qualité d'ajustement et simplicité. Des garde‑fous supplémentaires rejettent les solutions suspectes, comme des nuages trop étroits ou trop larges, basés sur trop peu de points, ou pas clairement séparés les uns des autres.
Preuve de son efficacité par simulations et structures d'ADN nanoconstruite
Pour tester G5M, les auteurs ont d'abord utilisé des simulations informatiques réalistes de scènes simples : paires de molécules et petites grilles de douze molécules espacées de seulement quelques nanomètres. Par rapport à la méthode de référence actuelle, connue sous le nom de Gradient Ascent, G5M a retrouvé beaucoup plus de molécules qui devraient être visibles à la limite théorique de résolution, tout en signalant presque jamais de molécules inexistantes. Dans des cas clés, il a récupéré des paires fortement rapprochées vingt‑sept fois plus souvent que l'ancienne méthode et amélioré la résolution effective de plus de moitié. L'équipe a ensuite confirmé ces gains expérimentalement en utilisant des structures d'origami d'ADN — formes d'ADN artificielles avec des sites d'ancrage placés à des positions précisément connues — montrant que G5M pouvait compter et localiser de manière fiable presque tous les sites attendus sur une gamme de conditions d'imagerie.
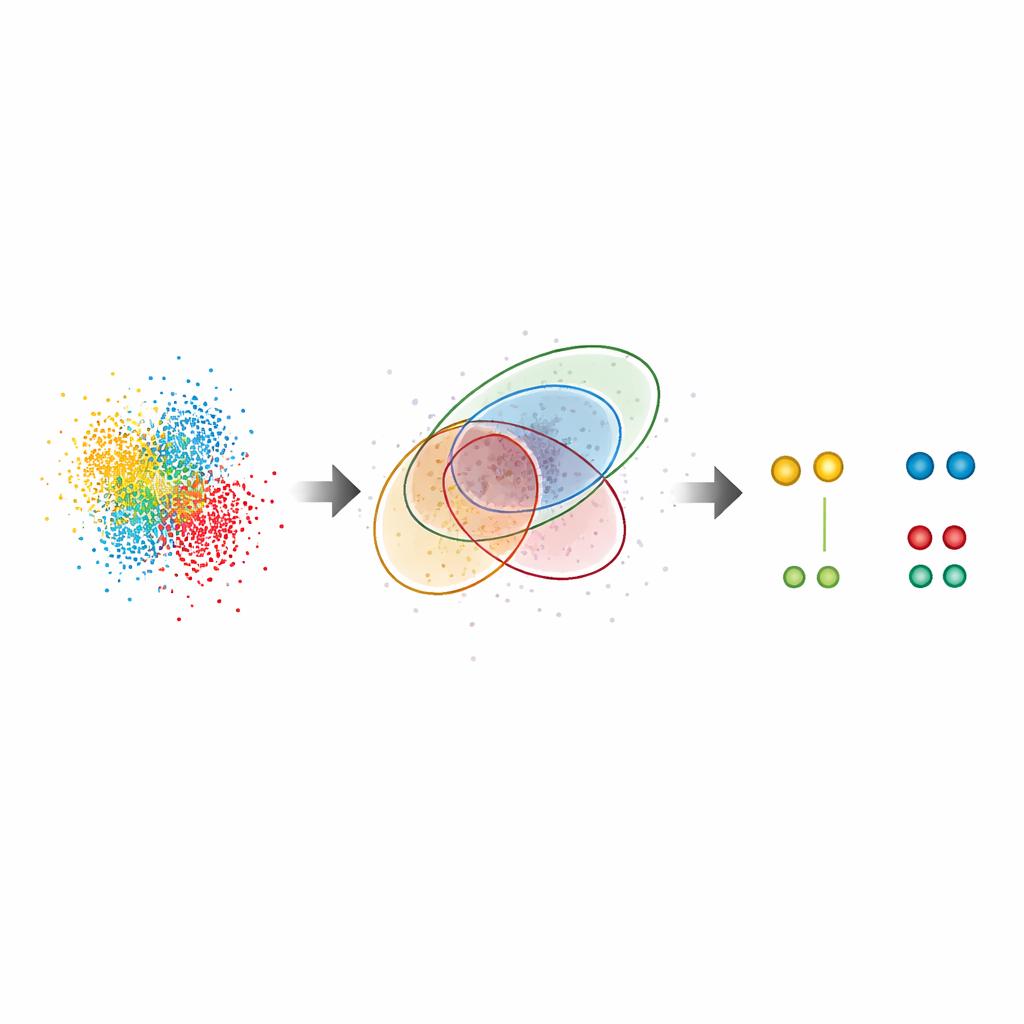
Révéler des motifs cachés dans des cellules réelles
Au‑delà des échantillons tests, G5M a été appliqué à des systèmes biologiques complexes. Dans les complexes du pore nucléaire, gigantesques portails du noyau cellulaire, la méthode a retrouvé l'agencement en anneau connu d'une protéine clé, Nup96, même lorsque les partenaires étaient séparés d'environ dix nanomètres. Elle a détecté près de deux fois plus de paires de protéines que la méthode standard et reproduit des estimations indépendantes de l'efficacité de marquage, suggérant qu'elle ne manque pas un grand nombre de molécules ni n'en ajoute de fictives. Les auteurs ont aussi étudié CD20, un récepteur de surface impliqué dans des cancers du sang et cible d'anticorps thérapeutiques. Là, G5M a révélé beaucoup plus de petits agrégats (dimères, trimères et tétramères) de CD20 sur la membrane cellulaire, éclaircissant la manière dont un anticorps anti‑cancer et des formats thérapeutiques apparentés réorganisent ces récepteurs. Il a même amélioré les performances d'une approche ultra‑haute résolution appelée RESI, qui s'appuie sur la séparation des signaux sur plusieurs cycles d'imagerie.
Ce que cela signifie pour la microscopie future
En extrayant des informations plus fiables à partir des données DNA‑PAINT existantes, G5M montre qu'un meilleur logiciel seul peut révéler de nouveaux détails biologiques, sans modifier les microscopes ou les colorants. L'algorithme maintient un taux de détections fausses extrêmement faible tout en résolvant des molécules presque en contact, ce qui est essentiel pour savoir combien de protéines composent un complexe, comment elles sont espacées, ou comment un médicament modifie leur organisation. Intégré à la plateforme open‑source Picasso et robuste aux réglages typiques, G5M est bien placé pour devenir un outil standard pour transformer la fluorescence clignotante en cartes moléculaires fiables, aidant les chercheurs à cartographier l'organisation nanométrique de la vie à l'intérieur des cellules.
Citation: Kowalewski, R., Reinhardt, S.C.M., Pachmayr, I. et al. Molecular mapping in DNA-PAINT via modified Gaussian Mixture Modeling. Nat Commun 17, 2315 (2026). https://doi.org/10.1038/s41467-026-70198-5
Mots-clés: microscopie à super-résolution, DNA-PAINT, cartographie moléculaire, oligomérisation des protéines, algorithmes d'analyse d'images