Clear Sky Science · fr
La multiomique unicellulaire révèle un axe mécanosensible endothélial PIEZO1‑IL‑33 conduisant à la fibrose pulmonaire
Pourquoi des poumons rigides comptent
La fibrose pulmonaire est une maladie dévastatrice dans laquelle des alvéoles autrefois élastiques se transforment peu à peu en tissu cicatriciel rigide, rendant chaque respiration pénible. Les médecins peuvent aujourd’hui seulement ralentir la progression, sans pouvoir l’arrêter ni l’inverser. Cette étude pose une question apparemment simple mais aux grandes implications : comment les cellules qui tapissent les vaisseaux sanguins pulmonaires perçoivent‑elles que le tissu environnant est devenu anormalement rigide, et comment cette perception se convertit‑elle en cicatrisation accrue ? En retraçant cette chaîne d’événements jusqu’aux cellules uniques et aux gènes individuels, les chercheurs mettent au jour un « interrupteur » mécanique dans les vaisseaux sanguins qui pourrait être ciblé par des médicaments.
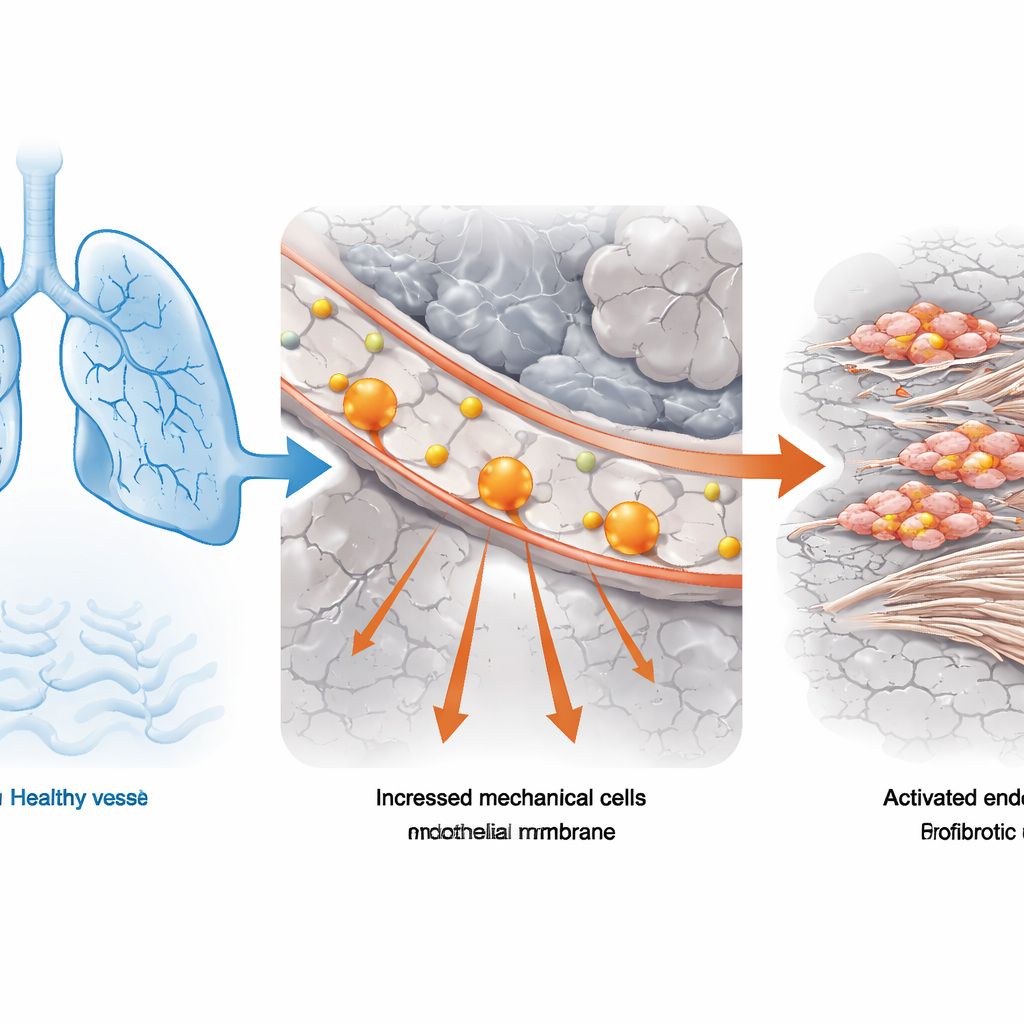
Des tests de la fonction pulmonaire aux cellules uniques
L’équipe a commencé par analyser des tissus pulmonaires de personnes atteintes de fibrose pulmonaire idiopathique, la forme la plus fréquente de la maladie, et de donneurs ayant des poumons normaux. Ils ont combiné des mesures cliniques standard de la fonction pulmonaire (la quantité d’air qu’une personne peut expirer de façon forcée) avec un séquençage ARN unicellulaire puissant, qui révèle quels gènes sont actifs dans des milliers de cellules individuelles. En utilisant un outil informatique reliant des données cliniques globales aux profils unicellulaires, ils ont identifié les types cellulaires les plus fortement associés à une fonction pulmonaire gravement altérée. Les cellules endothéliales vasculaires — les cellules qui forment la couche interne des vaisseaux sanguins — se sont démarquées, particulièrement enrichies chez les patients dont la capacité pulmonaire était inférieure à la moitié de la normale. Dans ces cellules endothéliales, les programmes génétiques liés au « stress mécanique » étaient systématiquement amplifiés, suggérant que des forces physiques anormales faisaient partie du problème.
Le stress mécanique comme moteur caché
Pour tester si ce lien entre détection du stress et maladie était général, les chercheurs ont eu recours à deux modèles murins de cicatrisation pulmonaire : l’un déclenché par la chimiothérapie au bléomycine, l’autre par une exposition chronique à la poussière de silice, un risque professionnel. En appliquant des méthodes unicellulaires à ces poumons expérimentaux, ils ont à nouveau constaté que les cellules endothéliales présentaient des signatures claires d’un stress mécanique accru. Dans les deux modèles, à mesure que le tissu pulmonaire environnant s’épaississait et se rigidifiait, l’endothélium vasculaire semblait basculer vers un état inadapté. Cette convergence entre échantillons humains et modèles animaux renforçait l’idée que des forces physiques altérées dans le poumon, au‑delà de l’inflammation ou de l’activité immunitaire, jouent un rôle central dans le développement et la progression de la fibrose.
Un capteur de pression ayant un rôle clé
En approfondissant, l’équipe a recherché des « mécanorécepteurs » spécifiques — des protéines qui convertissent l’étirement physique en signaux biochimiques — sur‑exprimés dans les cellules endothéliales soumises au stress. Une protéine canal, appelée PIEZO1, est apparue à plusieurs reprises comme suspecte principale. Chez la souris comme chez l’humain atteint de fibrose, les niveaux de PIEZO1 étaient nettement plus élevés dans les cellules endothéliales vasculaires que chez les témoins sains. Lorsque les chercheurs ont conçu des souris chez lesquelles PIEZO1 était supprimé uniquement dans l’endothélium, ces animaux ont été beaucoup plus résistants à la cicatrisation pulmonaire induite par la bléomycine : accumulation de collagène réduite, moins de cellules activées formant la cicatrice et niveaux plus faibles d’un marqueur chimique de fibrose. Le blocage pharmacologique de PIEZO1 par un inhibiteur peptidique a également atténué la cicatrisation, tandis que son activation a aggravé la fibrose — sauf si le récepteur faisait défaut dans les cellules endothéliales. Ensemble, ces expériences montrent que PIEZO1 dans les cellules qui tapissent les vaisseaux n’est pas un simple spectateur, mais un moteur nécessaire de la maladie.
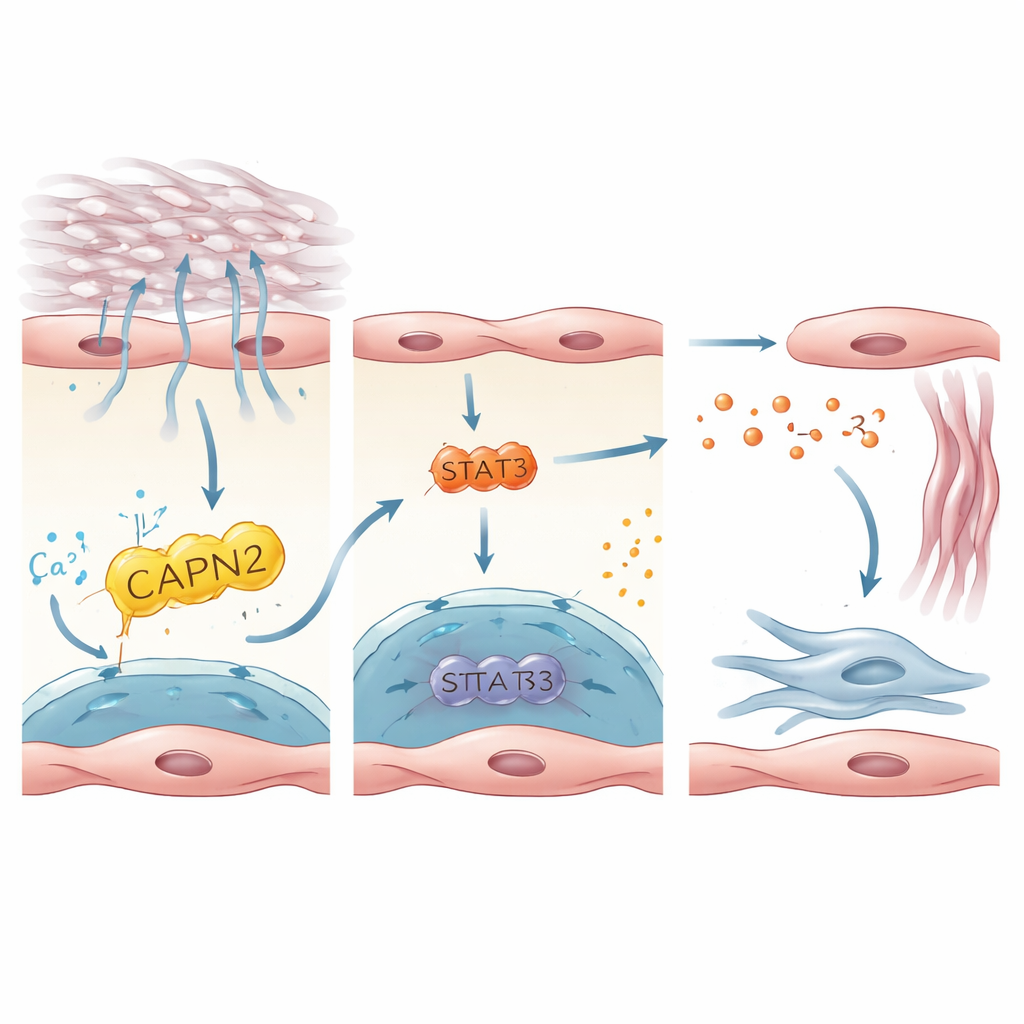
Une chaîne de signalisation qui réveille les cellules formant la cicatrice
L’étude a ensuite retracé comment l’activation de PIEZO1 à l’intérieur des cellules endothéliales se traduit en signaux qui réveillent les fibroblastes, les cellules qui déposent le tissu cicatriciel. En intégrant des jeux de données humains et murins, les auteurs ont mis en évidence l’interleukine‑33 (IL‑33), une petite protéine libérée par des cellules stressées ou endommagées, comme messager clé. IL‑33 était fortement exprimée dans les cellules endothéliales positives pour PIEZO1 et élevée dans les poumons de patients et de souris fibrosés. Dans des cellules endothéliales humaines en culture, cultivées sur des substrats rigides ou étirées pour simuler la respiration contre un poumon raide, l’activation de PIEZO1 augmentait la production d’IL‑33. Cela dépendait d’une enzyme en aval, CAPN2, et d’un facteur de transcription, STAT3, qui, ensemble, régulaient l’activité du gène IL‑33. Chez la souris, la suppression spécifique d’IL‑33 dans les cellules endothéliales protégeait contre la fibrose, tandis que la surexpression forcée d’IL‑33 dans l’endothélium annulait l’effet protecteur de la perte de PIEZO1. Ces résultats décrivent un axe linéaire : stress mécanique → PIEZO1 → CAPN2/STAT3 → IL‑33 → activation des fibroblastes et cicatrisation.
Ce que cela implique pour les traitements futurs
Pour les non‑spécialistes, le message est que la fibrose pulmonaire n’est pas seulement provoquée par des cellules immunitaires déchaînées ; c’est aussi une maladie liée à un défaut de « perception du toucher » dans les vaisseaux. Les cellules endothéliales perçoivent que leur environnement est devenu trop rigide, activent l’interrupteur PIEZO1 et libèrent en réponse IL‑33, un signal de danger qui incite les fibroblastes voisins à poursuivre le dépôt de cicatrice. En disséquant cette chaîne, du signal mécanique à l’expression génique, le travail met en lumière plusieurs cibles prometteuses — PIEZO1 lui‑même, la relais CAPN2‑STAT3 et IL‑33 — pour des thérapies visant à interrompre le cycle auto‑entretenu de rigidité et de cicatrisation. Bien que des études supplémentaires soient nécessaires pour moduler ces voies en toute sécurité chez l’humain, cet axe endothélial mécanosensible offre une nouvelle approche, fondée sur la physique, pour s’attaquer à une maladie qui a longtemps résisté aux traitements efficaces.
Citation: Zhang, L., Gui, X., Hou, R. et al. Single-cell multiomics uncovers an endothelial mechanosensitive PIEZO1-IL-33 axis driving pulmonary fibrosis. Nat Commun 17, 2655 (2026). https://doi.org/10.1038/s41467-026-70193-w
Mots-clés: fibrose pulmonaire, cellules endothéliales, mécanotransduction, PIEZO1, IL-33