Clear Sky Science · fr
Les adaptations de la tubuline de Plasmodium déterminent des architectures microtubulaires, une mécanique et une sensibilité aux médicaments distinctes
Pourquoi le squelette du paludisme est important
Les parasites du paludisme survivent à l’intérieur des globules rouges humains, mais ils doivent aussi se faufiler à travers les moustiques et divers tissus. Pour cela, ils s’appuient sur une charpente interne constituée de tubes microscopiques appelés microtubules. Cette étude pose une question simple mais puissante : comment les microtubules du parasite peuvent-ils être à la fois si spécialisés et robustes alors que leurs éléments de base ressemblent tant à ceux de nos propres cellules ? La réponse révèle non seulement comment le parasite conserve sa forme, mais aussi comment nous pourrions concevoir des médicaments qui ciblent son squelette sans endommager le nôtre. 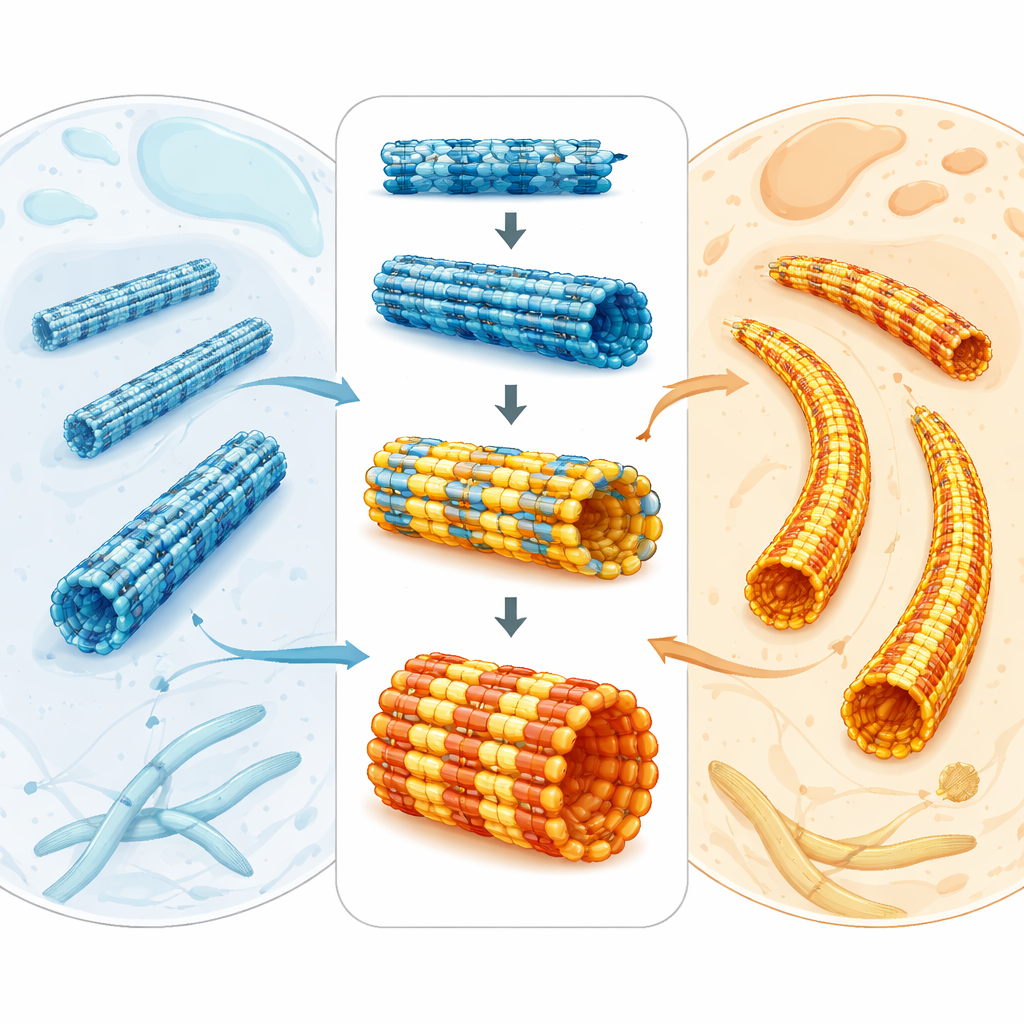
Les petits tubes qui façonnent un parasite mortel
Les microtubules sont des tubes protéiques creux qui aident les cellules à se diviser, à se déplacer et à maintenir leur forme. Ils sont construits à partir d’unités protéiques appariées appelées tubuline. Chez les animaux, les plantes et les parasites, la tubuline est étonnamment similaire, ce qui rend difficile d’expliquer pourquoi les microtubules peuvent apparaître et se comporter si différemment selon les organismes. Chez le parasite du paludisme Plasmodium falciparum, les microtubules forment des réseaux variés : certains sont dynamiques et interviennent lors de la division cellulaire, tandis que d’autres sont de longs supports rigides sous la membrane externe du parasite. Parce que ces structures sont essentielles à la croissance et à la transmission du parasite, elles constituent des cibles attrayantes pour des antipaludiques — d’autant plus que la résistance aux traitements actuels continue d’augmenter.
Voir la tubuline du parasite en détail atomique
Les chercheurs ont purifié la tubuline directement à partir de parasites P. falciparum et ont utilisé la cryo‑microscopie électronique à haute résolution pour observer comment elle s’assemble en microtubules. Ils ont comparé ces structures aux microtubules bien étudiés du cerveau des mammifères. À première vue, la tubuline du parasite ressemble presque à la version humaine et adopte le même repli global. Mais une comparaison attentive a mis au jour des grappes de petites variations de séquence autour de poches clés où se lient des molécules porteuses d’énergie (GTP et GDP) et où interagissent certains médicaments. Ces déplacements subtils modifient la position des hélices et des boucles voisines, en particulier à la surface du dimère de tubuline où d’autres protéines et des médicaments s’accrochent. Le travail suggère que, bien que le plan général soit conservé, des ajustements locaux dans le parasite remodèlent finement ces sites importants.
Des tubes plus rigides dus à des liaisons latérales renforcées
Les microtubules sont des polymères : de nombreux dimères de tubuline s’empilent bout à bout en protofilaments, et plusieurs protofilaments s’alignent côte à côte pour former la paroi du tube. L’équipe a constaté que, dans les microtubules du parasite, les contacts longitudinaux le long de chaque protofilament ressemblent beaucoup à ceux des microtubules cérébraux. La différence apparaît dans les contacts latéraux, entre protofilaments voisins. Bien que la zone de contact soit en réalité un peu plus petite chez le parasite, les simulations révèlent que ces connexions latérales sont collectivement plus fortes, rendant le réseau plus rigide. La modélisation informatique de portions de la paroi microtubulaire a montré que la tubuline du parasite fléchit et vrille moins que celle du cerveau. La tomographie électronique d’extrémités de microtubules réelles a confirmé que les microtubules du parasite présentent des boucles de protofilaments plus courtes et moins écartées, un signe distinctif d’un tube plus solide. 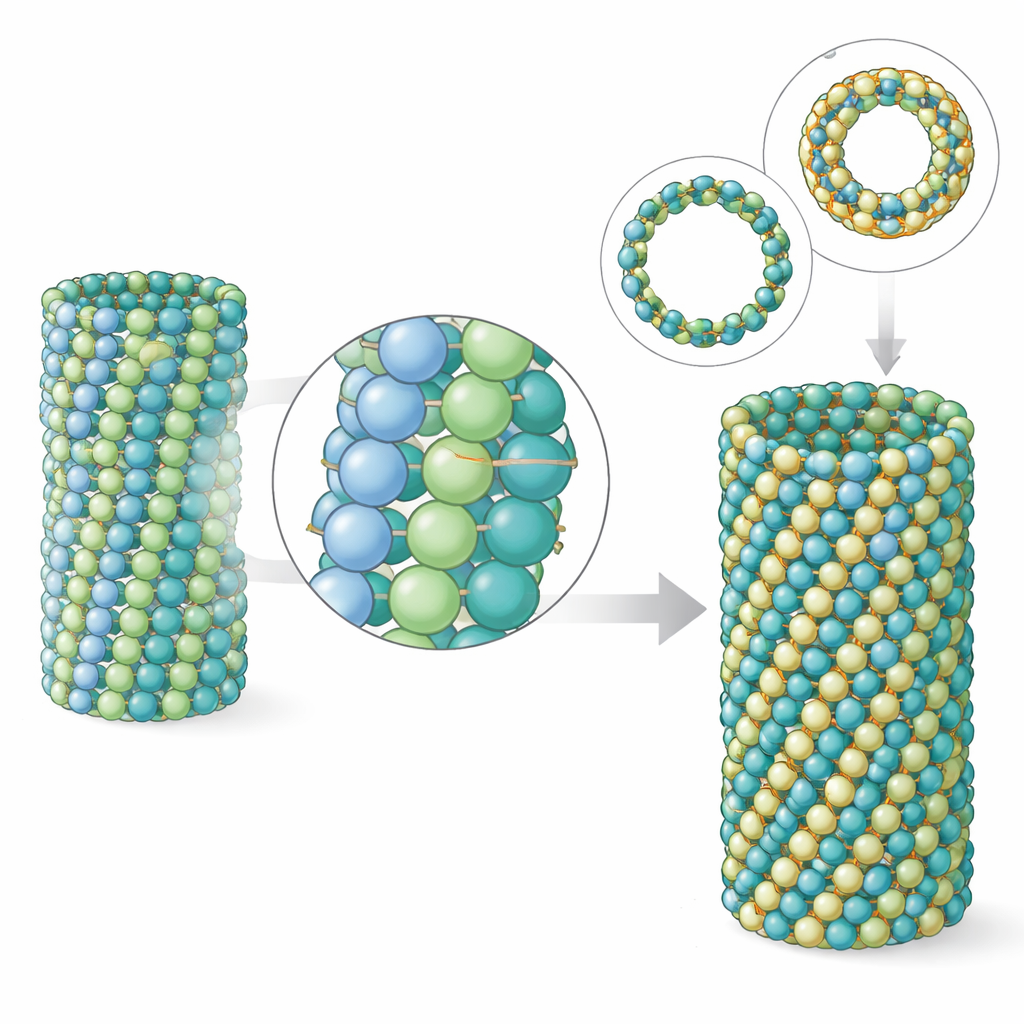
Des tailles de tubes inhabituelles adaptées à l’action du parasite
Autre caractéristique frappante de P. falciparum : à certains stades de son cycle, ses microtubules contiennent plus d’unités autour de leur circonférence que les 13 habituelles observées dans la plupart des cellules animales — souvent 15 voire 17 rangées de protofilaments. L’équipe a recréé ce comportement en éprouvette en changeant le nucléotide utilisé pendant l’assemblage. Avec une molécule de type GTP qui stabilise l’état en croissance, la tubuline du parasite favorise naturellement les microtubules à 15 protofilaments. Les auteurs ont résolu la structure de ces tubes plus épais et montré comment ils accommodent les protofilaments supplémentaires par une légère inclinaison du réseau, tout en restant presque parfaitement cylindriques. En comparant ces tubes à 15 protofilaments fabriqués en laboratoire à ceux observés à l’intérieur des cellules du parasite, la correspondance de forme et de dimensions était remarquablement proche, indiquant que des propriétés intrinsèques de la tubuline elle‑même — plutôt que la présence d’une foule de protéines auxiliaires — suffisent à générer les architectures distinctives du parasite.
Des indices pour des médicaments futurs spécifiques au parasite
La conclusion de l’étude est que l’évolution a ajusté la tubuline du parasite par de petites modifications de séquence dispersées qui, collectivement, modifient la mécanique des microtubules, leur architecture et leur sensibilité aux médicaments. Ces ajustements rendent les microtubules du parasite plus rigides et capables de former des tailles de tube non standard adaptées à son cycle de vie exigeant, tout en conservant le design de base de la tubuline reconnaissable. Important pour la médecine, certaines poches de liaison aux médicaments semblent quasi identiques entre parasite et hôte (comme pour le médicament anticancéreux paclitaxel), ce qui suggère qu’elles sont de mauvais candidats pour des antipaludiques sélectifs. D’autres régions, telles que celle supposée lier le composé de type herbicide oryzalin, montrent à la fois des déplacements de séquence et des déplacements structurels subtils qui pourraient expliquer pourquoi les microtubules du parasite y sont plus vulnérables que ceux de l’homme. Cartographier ces différences nuancées fournit une feuille de route pour concevoir à l’avenir des médicaments qui perturbent le squelette du parasite du paludisme tout en épargnant en grande partie nos propres cellules.
Citation: Bangera, M., Wu, J., Beckett, D. et al. Adaptations in Plasmodium tubulin determine distinct microtubule architectures, mechanics and drug susceptibility. Nat Commun 17, 2275 (2026). https://doi.org/10.1038/s41467-026-70181-0
Mots-clés: parasite du paludisme, microtubules, structure de la tubuline, ciblage médicamenteux, cryo‑microscopie électronique