Clear Sky Science · fr
Catalyseurs monoatomiques asymétriques Zn-N2O2 d’inspiration biologique via un squelette naturel pour une N‑alkylation efficace des nitroarènes par des alcools
Transformer des coquilles de déchets en outils chimiques utiles
De nombreux médicaments importants, agents de protection des cultures et matériaux spécialisés contiennent une caractéristique structurale simple : un atome d’azote lié à une petite chaîne carbonée. La production industrielle de ces molécules « N‑alkylées » requiert généralement des produits chimiques agressifs, des températures élevées et des métaux coûteux. Cette étude présente une alternative plus verte inspirée par la nature elle‑même, utilisant des atomes de zinc ancrés sur un support fabriqué à partir de chitosane, un matériau dérivé de coquilles de fruits de mer jetées, pour réaliser ces réactions plus efficacement et avec moins de déchets.
Pourquoi une chimie de l’azote plus verte compte
Les méthodes conventionnelles pour lier des chaînes carbonées à l’azote reposent sur des produits halogénés réactifs et des additifs forts qui génèrent de grandes quantités de sous‑produits. Elles nécessitent aussi souvent des métaux précieux rares et coûteux comme le palladium ou le platine en tant que catalyseurs. En revanche, une approche plus récente appelée stratégie de « borrowing hydrogen » (emprunt d’hydrogène) utilise des alcools courants à la fois comme source de la chaîne carbonée et de l’hydrogène, l’eau étant le principal sous‑produit. Si le concept est attrayant, les catalyseurs à base de métaux non nobles existants fonctionnent généralement seulement dans des conditions sévères ou avec des types limités de réactifs. Le défi a été de concevoir un catalyseur peu coûteux et recyclable capable de conduire cette réaction efficacement dans des conditions plus douces.
Emprunter l’hydrogène avec des atomes simples de zinc
Les chercheurs ont abordé ce problème en utilisant la catalyse monoatomique, où des atomes métalliques isolés plutôt que des particules plus grosses sont ancrés sur une surface solide. Ils ont dissous le chitosane, un polymère biodégradable riche en groupes oxygène et azote, et l’ont transformé en microsphères poreuses tridimensionnelles par un procédé sol‑gel. Des ions zinc ont ensuite été introduits et chauffés doucement, verrouillant des atomes de zinc isolés dans la matrice de chitosane dans une configuration que les auteurs décrivent comme Zn‑N2O2 : chaque atome de zinc est entouré de deux atomes d’azote et de deux atomes d’oxygène issus du support. Cet environnement local d’inspiration biologique imite la manière dont les métaux sont coordonnés dans de nombreuses enzymes naturelles et maximise le nombre de sites actifs disponibles pour la réaction.
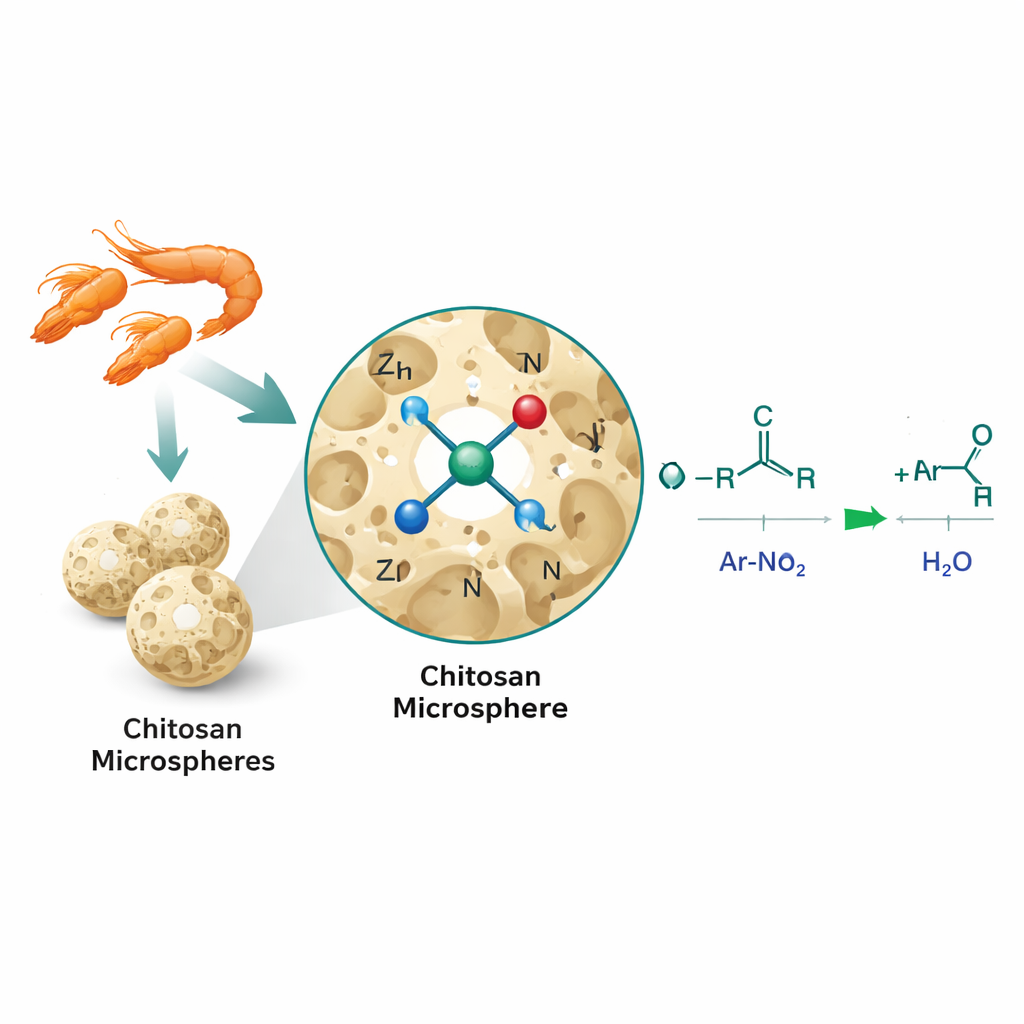
Vérifier la structure et la performance
Pour confirmer que le zinc existait réellement sous forme d’atomes isolés plutôt que de particules plus grosses, l’équipe a combiné plusieurs méthodes avancées d’imagerie et de spectroscopie. Les microscopes électroniques ont montré des sphères de chitosane poreuses mais aucun amas de zinc visible, tandis que des images en champ sombre à grand angle ont révélé de petites taches brillantes correspondant à des atomes de zinc individuels répartis uniformément à la surface. Des techniques basées sur les rayons X ont en outre indiqué que le zinc était principalement lié à l’azote et à l’oxygène, sans liaisons détectables zinc–zinc, soutenant ainsi le modèle monoatomique. Ces caractéristiques structurelles se sont traduites par des performances remarquables : dans une réaction modèle entre le nitrobenzène et l’alcool benzyl, le catalyseur zinc‑sur‑chitosane (Zn/CS) a fourni des rendements très élevés avec une charge métallique exceptionnellement faible et a surpassé du zinc commercial sur charbon, des nanoparticules de zinc et des sels de zinc dissous simples. Il a également fonctionné pour 56 combinaisons différentes de composés nitro et d’alcools, incluant des éléments structuraux complexes utilisés en découverte de médicaments, et a pu être réutilisé au moins cinq fois avec une perte d’activité minimale.
Comment le catalyseur fonctionne réellement
Au niveau moléculaire, le processus d’emprunt d’hydrogène suit une séquence d’étapes. D’abord, l’alcool est temporairement oxydé en aldéhyde tout en transférant de l’hydrogène au site de zinc. Cet hydrogène est ensuite utilisé pour réduire le groupe nitro en amine. L’aldéhyde et la nouvelle amine se combinent pour former une imine, qui est enfin réduite en produit N‑alkylé désiré, bouclant le cycle. La RMN résolue dans le temps, la chromatographie en phase gazeuse et des réactions de contrôle soigneusement conçues ont confirmé la présence d’intermédiaires clés le long de cette voie. Des expériences de marquage au deutérium, où certains atomes d’hydrogène ont été remplacés par un isotope plus lourd, ont montré que l’espèce zinc–hydrogène joue le rôle dominant dans les étapes de réduction. Des simulations informatiques ont aidé à expliquer pourquoi ce catalyseur particulier est si efficace : l’environnement asymétrique Zn‑N2O2 attire la densité électronique loin de l’atome de zinc, le rendant légèrement appauvri en électrons. Cet ajustement électronique rend le zinc meilleur pour lier et activer l’intermédiaire dérivé de l’alcool, abaissant la barrière énergétique pour l’étape la plus difficile — l’élimination initiale de l’hydrogène de l’alcool.
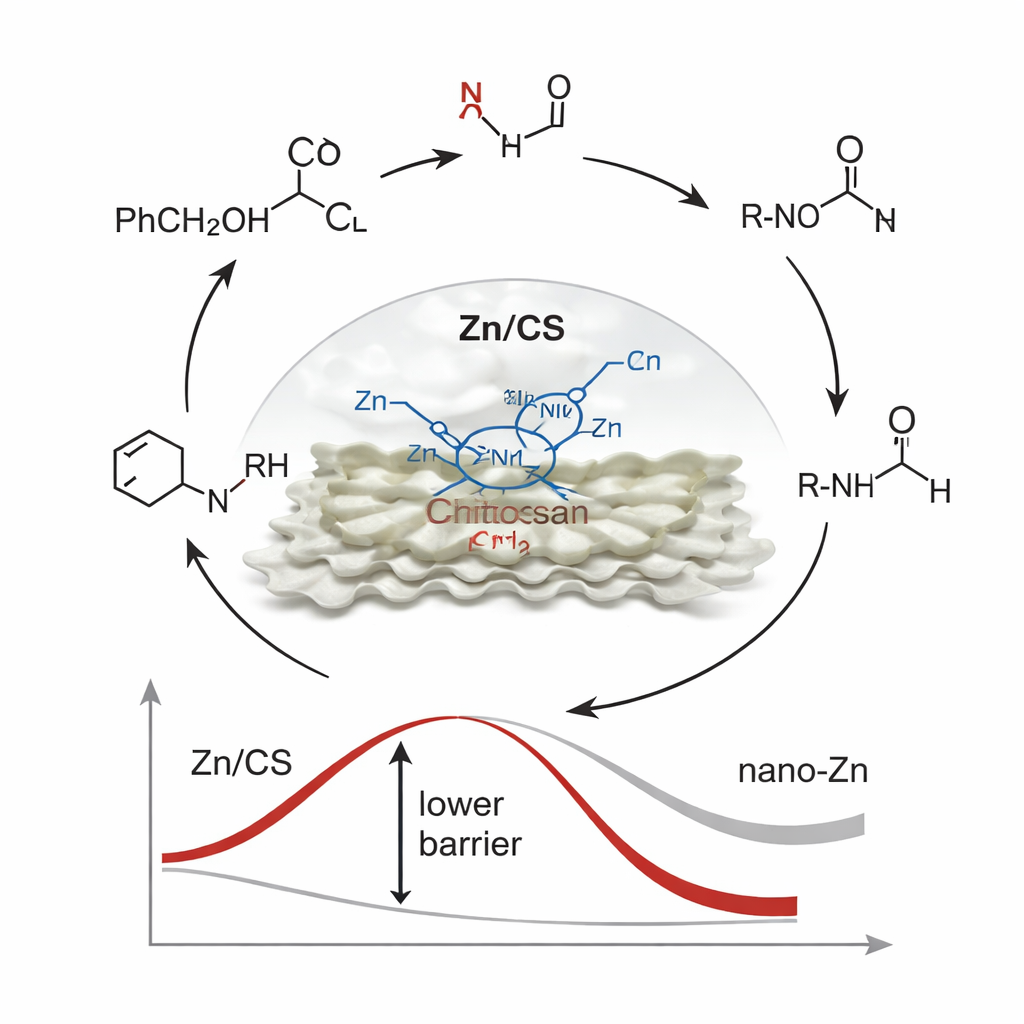
Des déchets marins aux catalyseurs intelligents
En termes accessibles, ce travail montre comment des atomes de zinc individuels, arrangés précisément sur un support naturel et spongieux issu de déchets de fruits de mer, peuvent surpasser de nombreux catalyseurs métalliques traditionnels dans une classe importante de réactions chimiques. En utilisant des alcools au lieu de réactifs toxiques et en générant principalement de l’eau comme sous‑produit, le système offre une manière plus propre et potentiellement moins coûteuse de fabriquer une large gamme de molécules contenant de l’azote, y compris des motifs pharmaceutiques. La combinaison d’un support en biopolymère renouvelable avec des sites monoatomiques finement ajustés illustre une voie prometteuse vers une chimie plus durable, où des réactions industrielles utiles empruntent leurs principes de conception — et certains de leurs matériaux bruts — à la nature.
Citation: Huang, Y., Li, Y., Yin, X. et al. Bio-inspired asymmetric Zn-N2O2 single-atom catalysts via natural skeleton for efficient N-alkylation of nitroarenes with alcohols. Nat Commun 17, 2242 (2026). https://doi.org/10.1038/s41467-026-70172-1
Mots-clés: catalyse monoatomique, chimie verte, emprunt d’hydrogène, chitosane, catalyseur au zinc