Clear Sky Science · fr
L’assemblage d’un groupe réactif covalent dans la biosynthèse de la fostriecine implique la malonylation-lactonisation par une thioestérase bifonctionnelle et une démalonylation enzymatique
Comment la nature construit un minuscule groupe réactif
Les médicaments anticancéreux et certains antibiotiques reposent souvent sur quelques atomes arrangés avec précision — un petit « groupe réactif » qui se fixe sur une protéine et l’inactive. La fostriecine, composé naturel, est l’un de ces molécules, dotée d’une forte activité contre des enzymes impliquées dans la croissance cellulaire. Mais sa structure complexe rend sa fabrication et sa modification en laboratoire difficiles. Cette étude dévoile, étape par étape, comment des bactéries assemblent le groupe réactif crucial de la fostriecine, révélant des astuces enzymatiques que les chimistes peuvent désormais emprunter pour concevoir de nouveaux médicaments.
Le crochet particulier des médicaments naturels puissants
De nombreux médicaments prometteurs issus de bactéries du sol appartiennent à une famille appelée polykétides. Au sein de cette famille, un sous-groupe porte un cycle réactif, connu des chimistes sous le nom de δ-lactone α,β-insaturée, qui agit comme un hameçon moléculaire. Il peut former une liaison permanente avec certains acides aminés des protéines, éteignant des commutateurs biologiques clés. Dans la fostriecine et des molécules apparentées, ce crochet est associé à un groupe phosphate qui les aide à cibler des enzymes spécifiques contrôlant la division cellulaire. Ces caractéristiques en font des pistes anticancéreuses intéressantes, mais la même réactivité et la complexité structurale rendent leur synthèse délicate et les rendent instables pendant le stockage.
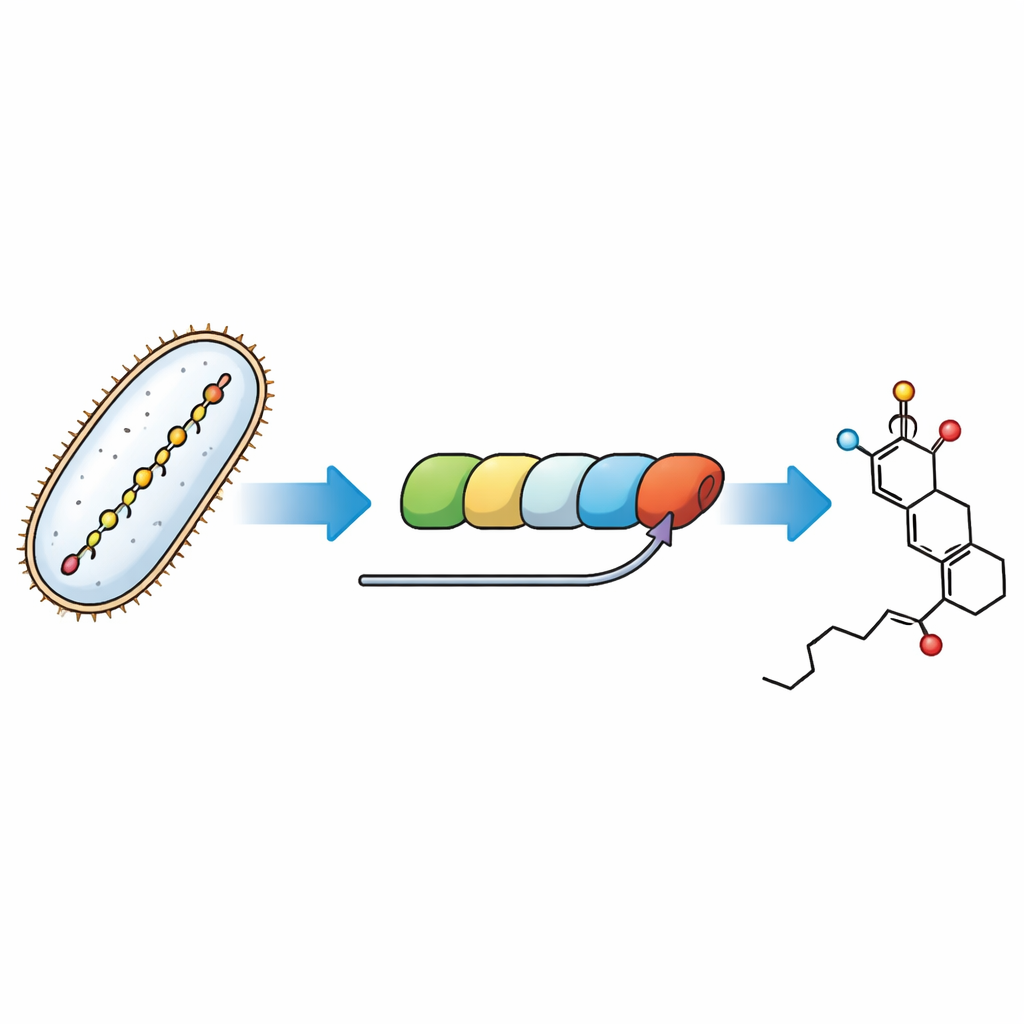
Suivre les dernières étapes d’une chaîne de montage moléculaire
Les bactéries fabriquent la fostriecine à l’aide d’une énorme machinerie protéique modulaire appelée polykétide synthase — une chaîne de montage où chaque station rallonge et façonne une chaîne carbonée en croissance. Le casse-tête abordé ici est de savoir comment le dernier module de cette machinerie forge le cycle du groupe réactif et installe une « poignée » temporaire appelée groupe malonyl, qui doit ensuite être retirée. En recréant la voie dans des éprouvettes avec des enzymes purifiées et des analogues petites molécules soigneusement conçus des intermédiaires naturels, les chercheurs ont pu observer les étapes individuelles et les attribuer à des parties spécifiques de la chaîne de montage.
Une enzyme multitâche dotée d’un talent inattendu
L’équipe a découvert que la station finale de la chaîne de montage, un domaine nommé FosTE, se comporte d’une manière inédite. Les versions typiques de ce domaine se contentent généralement de détacher le produit fini de la chaîne. FosTE, au contraire, saisit d’abord un fragment malonyl issu d’un précurseur cellulaire courant et le transfère sur un oxygène précis de la chaîne en croissance, puis aide la chaîne à se replier pour se refermer en un cycle formant le groupe réactif. La mutation d’un seul acide aminé sérine réactif dans FosTE supprime les deux activités. La modélisation structurale met en évidence deux résidus d’arginine chargés positivement dans le site actif qui enveloppent le fragment malonyl et le positionnent pour le transfert — des fonctions normalement assurées par un autre type d’enzyme. Le remplacement de ces arginines par des résidus neutres efface l’étape de transfert du malonyl tout en laissant la formation basique du cycle largement intacte, confirmant leur rôle critique.
Verrouiller le groupe réactif et éviter le gaspillage
Une fois le cycle formé et portant son groupe malonyl temporaire, une autre enzyme, FosM, doit enlever ce groupe pour dévoiler le groupe réactif pleinement armé. L’étude montre que FosM fonctionne efficacement seulement après qu’une autre enzyme, une kinase à spécificité large appelée FosH, a ajouté un phosphate à une position voisine de la molécule. Lorsque les chercheurs ont fourni le cycle malonylé à FosM seul, la conversion n’était que modeste. L’ajout préalable de FosH a conduit à une suppression presque complète du groupe malonyl et à la formation de l’unité réactive finale. Fait important, FosH peut aussi phosphoryler des intermédiaires « dérivés » issus de réactions secondaires, les sauvant pour qu’ils soient correctement traités au lieu d’être perdus comme produits sans suite.
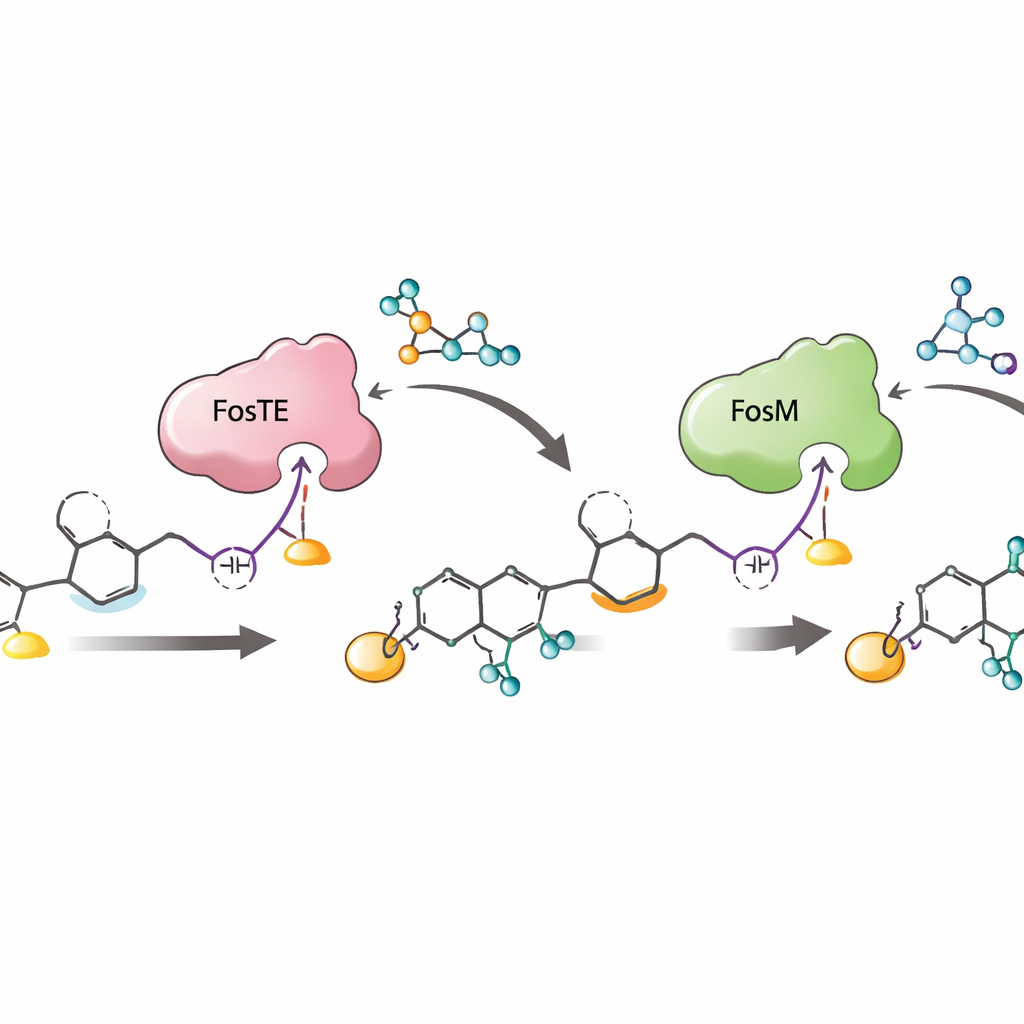
Pourquoi cette chorégraphie enzymatique est importante
Pris ensemble, les résultats révèlent une séquence finement chorégraphiée : extension de la chaîne sur la chaîne de montage, addition de malonyl et fermeture du cycle pilotées par FosTE, phosphorylation par FosH, puis démalonylation déclenchée par FosM. Cet ordre non seulement construit efficacement le fragile groupe réactif, mais protège aussi les intermédiaires instables de la dégradation et maximise la production de la forme phosphorylée désirée, la plus active en tant que piste médicamenteuse. En montrant comment un seul domaine enzymatique peut à la fois décorer et libérer une molécule en croissance — et comment des enzymes partenaires affinent et récupèrent des intermédiaires réactifs — l’étude offre un plan pour l’ingénierie de nouveaux polykétides porteurs de groupes réactifs et pour la conception de voies synthétiques plus courtes et plus efficaces vers des agents anticancéreux complexes comme la fostriecine.
Citation: Nguyen, L.N.K.T., Schlotte, L., Hoffmann, J. et al. Covalent warhead assembly in fostriecin biosynthesis involves malonylation-lactonisation by a bifunctional thioesterase and enzymatic demalonylation. Nat Commun 17, 2365 (2026). https://doi.org/10.1038/s41467-026-70144-5
Mots-clés: fostriecine, biosynthèse des polykétides, ingénierie enzymatique, groupes réactifs de produits naturels, synthèse chimioenzymatique