Clear Sky Science · fr
Régulation de la traduction par désulfuration oxydative des modifications de l’ARNt
Comment les cellules ajustent la production de protéines en situation de stress
Toute cellule doit choisir quelles protéines produire, à quelle vitesse et quand ralentir. Cette étude met en lumière un interrupteur chimique subtil sur les molécules d’ARN de transfert (ARNt) qui aide les cellules à réduire la production protéique lorsque l’environnement devient plus oxydant, comme lors d’inflammations ou de stress métabolique. En observant le comportement de cet interrupteur dans des cellules de mammifères et dans des systèmes in vitro, les chercheurs dévoilent une nouvelle façon dont des modifications ressemblant à des dommages de l’ARN peuvent en réalité servir de signal régulateur.
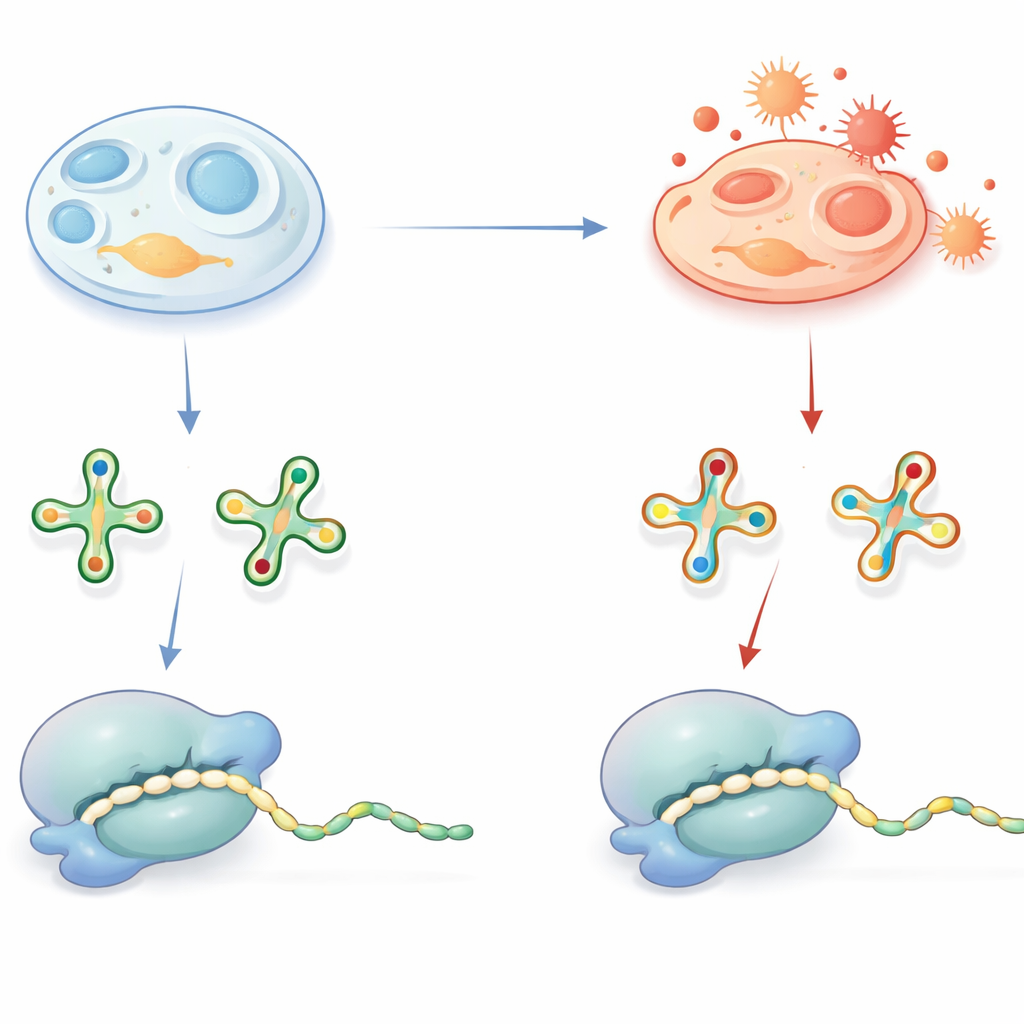
Petites marques sur l’ARNt aux grandes conséquences
Les ARNt jouent le rôle d’adaptateurs qui lisent les « mots » de trois lettres de l’ARN messager et apportent les acides aminés correspondants lors de la synthèse protéique. Pour accomplir cette tâche avec précision et efficacité, de nombreux ARNt portent des décorations chimiques spéciales, en particulier à une position clé qui contacte la troisième lettre de chaque codon. Une décoration répandue est un groupe contenant du soufre sur une base uridine, souvent notée comme un dérivé de 2-thiouridine. En conditions normales, ce groupe sulfuré aide l’ARNt à reconnaître correctement les codons se terminant par A ou G et soutient une traduction rapide et sans erreur. Des défauts dans ces décorations sont déjà connus pour provoquer des maladies humaines, ce qui souligne leur importance.
Quand le stress oxydatif réécrit l’ARNt
Le groupe sulfuré qui améliore le décodage a un revers : il est chimiquement vulnérable à l’oxydation. L’équipe s’est demandé si, à l’intérieur des cellules, ce groupe était effectivement retiré en conditions oxydantes, et quelles seraient les conséquences sur la synthèse protéique. Grâce à une spectrométrie de masse sensible, ils ont identifié des versions oxydées et dépourvues de soufre de ces bases d’ARNt — appelées dérivés h2U — dans des tissus de souris, des mitochondries de porc, des bactéries, des levures et diverses lignées cellulaires humaines. Une expérience astucieuse avec un traceur d’ARNt bactérien ajouté a montré que ces marques h2U ne sont pas des artefacts de préparation d’échantillon mais se forment dans les cellules vivantes. Bien que les versions oxydées ne soient présentes que dans une fraction des ARNt, leur abondance variait selon les tissus et les types cellulaires, ce qui suggère que l’état redox cellulaire et la capacité antioxydante influencent la fréquence de cette conversion.
Comment les ARNt oxydés ralentissent la chaîne de production
Les chercheurs ont ensuite testé comment ces ARNt altérés se comportent pendant la synthèse protéique. Ils ont converti chimiquement la forme sulfurée en forme oxydée h2U dans un ARNt total et utilisé un système de traduction humaine entièrement reconstitué in vitro. Une protéine rapportrice dont la production dépend fortement de ces ARNt modifiés montrait une production fortement réduite lorsque les ARNt étaient désulfurés, tandis qu’un témoin évitant les codons affectés se traduisait normalement. Des essais biochimiques ont expliqué pourquoi : les ARNt oxydés pour la lysine, la glutamine et le glutamate étaient beaucoup moins efficacement aminoacylés, alors que les ARNt correspondants pour l’arginine étaient largement épargnés. De manière importante, les ARNt portant h2U apparaissaient toujours dans des fractions liées aux ribosomes (polysomes) extraites de cellules, indiquant qu’ils participent bien à la traduction, mais de manière inefficace.
Une vue structurale d’un décodage affaibli
Pour voir précisément comment l’oxydation modifie le décodage, l’équipe a utilisé la cryo‑microscopie électronique à haute résolution pour imager des ribosomes bactériens programmés avec un ARNt humain pour la lysine et des codons spécifiques. À l’état normal, contenant du soufre, la base modifiée à la position de « flexibilité » (wobble) de l’ARNt formait soit une paire de bases standard avec un codon se terminant par A, soit une paire wobble spéciale avec un codon se terminant par G, toutes deux bien logées dans le centre de décodage du ribosome. Après désulfuration, la même base ne pouvait établir qu’un contact faible avec le codon se terminant par A et formait une paire wobble moins stable avec le codon en G. Des expériences d’affinité concordaient avec ces structures : l’ARNt lysine oxydé perdait essentiellement la capacité à reconnaître le codon AAA et reconnaissait beaucoup moins efficacement le codon AAG. Ensemble, ces résultats montrent qu’une modification chimique apparemment minime peut se traduire par des ralentissements spécifiques à certains codons au cours de la synthèse protéique.
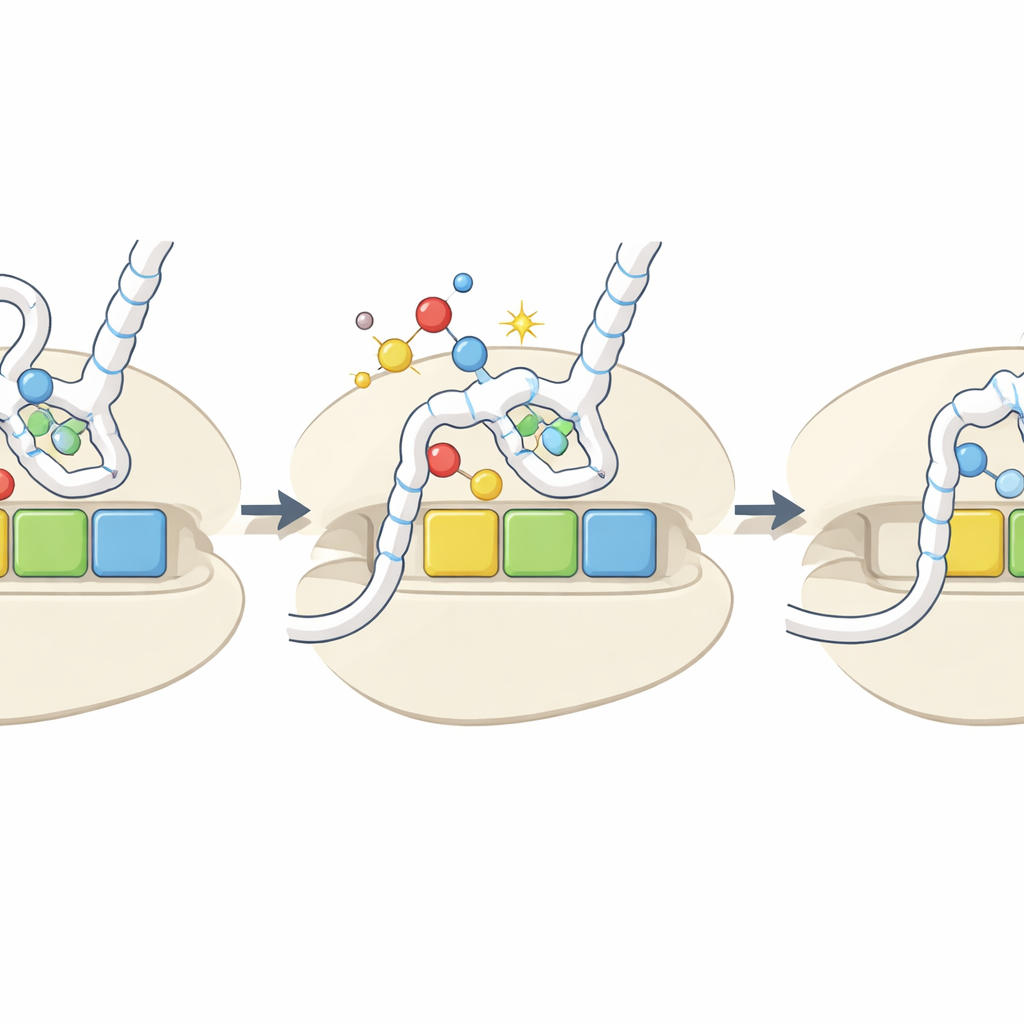
Un signal de dommage qui devient un bouton de réglage
Globalement, l’étude propose que l’élimination oxydative du soufre sur des bases clés de l’ARNt agit comme un capteur intégré de l’environnement redox cellulaire. En situation de stress oxydatif, davantage d’ARNt sont convertis en forme h2U, qui sont mal aminoacylés et se lient faiblement à certains codons. Cela ralentit sélectivement la traduction sur ces codons, ce qui peut modifier la stabilité des ARNm concernés, altérer le repliement des protéines et déclencher des voies de réponse au stress lorsque les ribosomes butent. Bien que ces marques oxydées soient relativement rares et que leurs niveaux n’augmentent pas toujours de façon spectaculaire lors de stress expérimental, leurs effets spécifiques aux codons et aux acides aminés signifient que même des changements modestes pourraient remodeler quelles protéines sont synthétisées, et à quelle vitesse, dans des conditions difficiles.
Citation: Mo, Y., Ishiguro, K., Miyauchi, K. et al. Translational regulation by oxidative desulfuration of tRNA modifications. Nat Commun 17, 2125 (2026). https://doi.org/10.1038/s41467-026-70126-7
Mots-clés: modification de l’ARNt, stress oxydatif, synthèse des protéines, régulation de la traduction, dommages de l’ARN