Clear Sky Science · fr
Cibler l’utilisation de la tyrosine dépendante de l’ARNt révèle une vulnérabilité métabolique dans le carcinome hépatocellulaire
Affamer les cellules cancéreuses d’un élément de base courant
Les cellules du cancer du foie, comme toutes les cellules à division rapide, ont besoin d’un apport constant en acides aminés — ces petits éléments constitutifs des protéines. Cette étude révèle que le carcinome hépatocellulaire, la forme la plus courante de cancer du foie, présente une faiblesse inattendue : il dépend fortement de l’acide aminé tyrosine pour la production d’énergie et la survie. En limitant sélectivement l’usage de la tyrosine par les cellules cancéreuses, les chercheurs ont pu ralentir la croissance tumorale, endommager les centrales énergétiques des cellules cancéreuses et déclencher une forme de mort cellulaire qui pourrait être exploitée pour de nouveaux traitements.
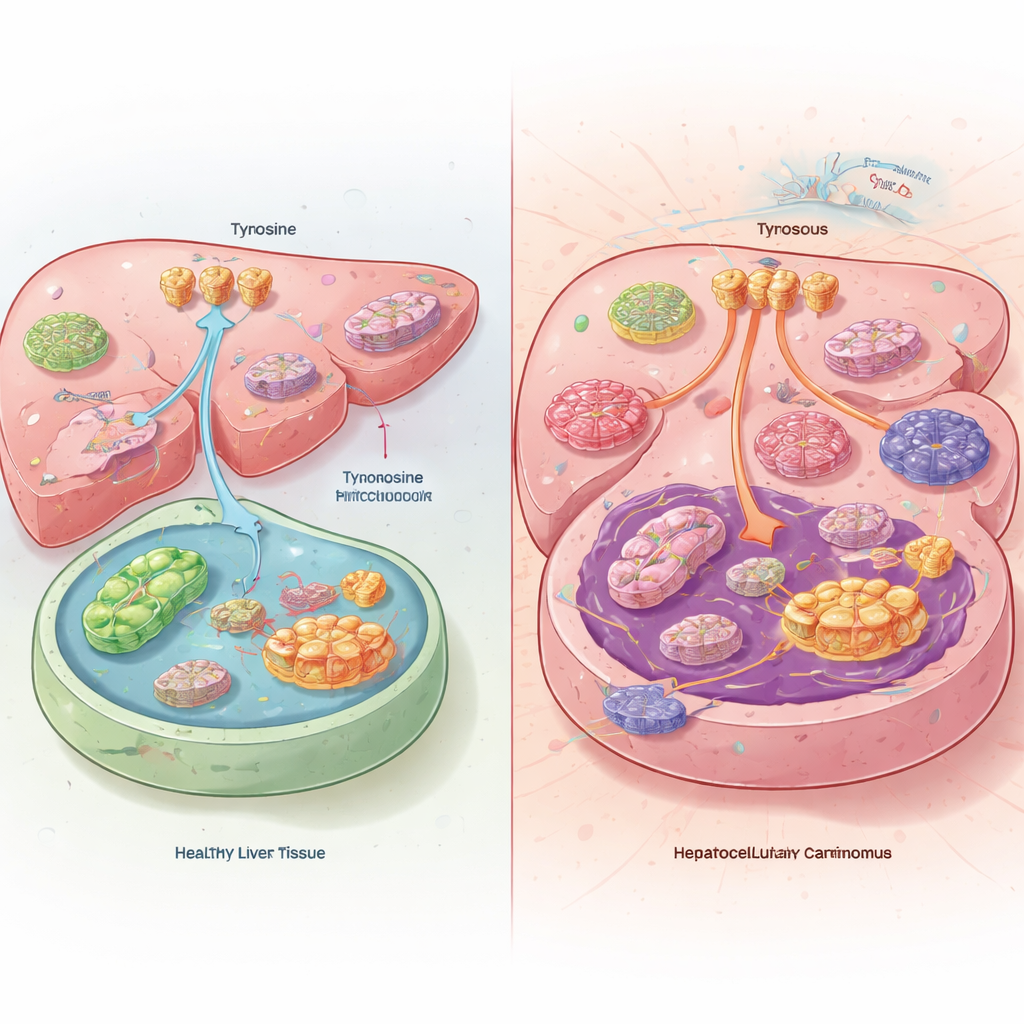
Un déséquilibre caché dans les tumeurs hépatiques
Lorsque l’équipe a comparé des tumeurs hépatiques à du tissu hépatique sain provenant de patients et de souris, elle a trouvé quelque chose de surprenant. À l’intérieur des cellules cancéreuses, les niveaux de tyrosine étaient en réalité faibles, même si les tumeurs captaient davantage de tyrosine depuis le sang et en dégradaient moins. Plutôt que d’oxyder la tyrosine comme carburant, les tumeurs hépatiques la détournaient vers la production protéique. Les cancers y parvenaient en augmentant l’activité des transporteurs de tyrosine à la surface cellulaire et en réduisant les enzymes qui, normalement, dégradent la tyrosine dans le foie. Des souris alimentées avec un régime sans tyrosine développaient des tumeurs plus petites et vivaient plus longtemps, tandis qu’un excès de tyrosine dans l’alimentation faisait croître leurs cancers plus rapidement.
Comment le cancer réorganise la production protéique
Les chercheurs ont relié cette soif de tyrosine à un puissant gène oncogénique appelé MYC. Dans les tumeurs hépatiques, MYC active une protéine nommée YARS1, qui attache la tyrosine à un ARN de transfert spécifique (tRNA-TyrGUA). Cet ARNt chargé est ce dont les ribosomes ont besoin pour fabriquer des protéines riches en tyrosine. L’étude montre que les cancers du foie augmentent à la fois YARS1 et son ARNt correspondant, garantissant un flux privilégié de tyrosine vers la synthèse protéique. Perturber ce flux — soit en diminuant les niveaux de tyrosine, soit en inhibant YARS1 ou le tRNA-TyrGUA, soit en bloquant le chargement de la tyrosine — rendait les cellules de cancer du foie beaucoup moins viables in vitro et chez la souris, révélant une vulnérabilité métabolique étroitement liée à leurs besoins élevés en production protéique.
Affaiblir les centrales énergétiques et l’équilibre lipidique
En combinant des mesures à l’échelle du génome de l’ARN, de la production protéique et des métabolites, l’équipe a identifié deux cibles particulièrement sensibles à la restriction en tyrosine. L’une, NDUFB8, est une composante du complexe I mitochondrial, un élément central de la machinerie de génération d’énergie de la cellule. L’autre, SCD1, aide à convertir les graisses saturées en graisses mono-insaturées, plus sûres à stocker dans les membranes cellulaires et les gouttelettes lipidiques. Lorsque la tyrosine dédiée à la traduction était limitée, la production de NDUFB8 et de SCD1 chutait, tandis que leurs niveaux d’ARN restaient globalement inchangés — preuve claire que c’est la traduction, et non l’expression génique, qui était affectée. Cela conduisait à un assemblage défectueux du complexe I, à une respiration cellulaire réduite, à un excès d’espèces réactives de l’oxygène et à un basculement des lipides des formes mono-insaturées vers des formes poly-insaturées plus fragiles et facilement oxydables.
Contraindre les cellules cancéreuses à une mort ferrique
Les dommages mitochondriaux combinés et l’instabilité lipophile poussaient les cellules du cancer du foie vers la ferroptose, une forme de mort cellulaire dépendante du fer et provoquée par la peroxydation lipidique. Les tumeurs tentaient de se défendre en augmentant les bloqueurs naturels de la ferroptose tels que GPX4 et des molécules apparentées, mais un large criblage CRISPR a montré que désactiver ces protecteurs rendait la restriction en tyrosine encore plus létale. Dans des modèles cellulaires et murins, associer des stratégies limitant la tyrosine à des médicaments inhibant GPX4 ou BCL2 — ou à des traitements existants du cancer du foie comme le sorafénib et le vénétoclax — produisait un meilleur contrôle tumoral, des charges tumorales réduites et une survie prolongée.
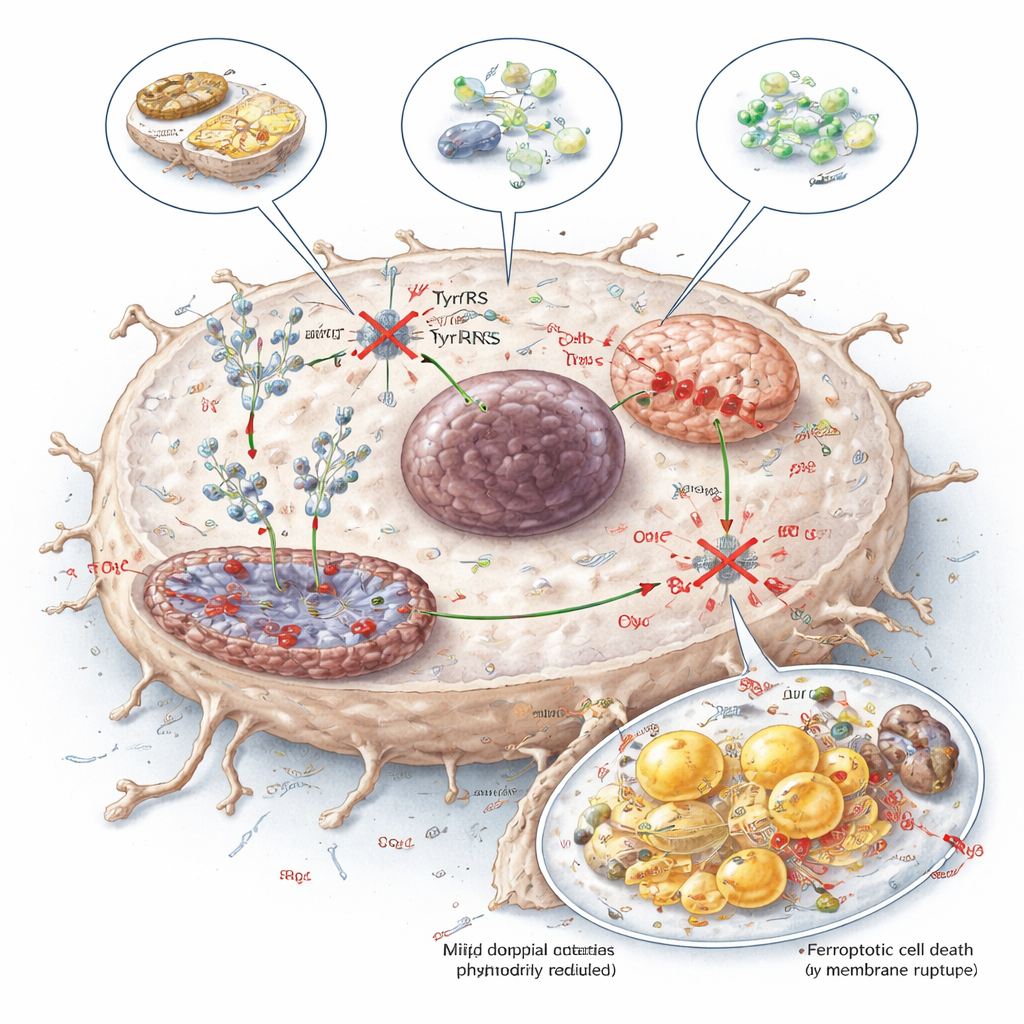
Transformer une faiblesse métabolique en thérapie
Pour explorer des moyens pratiques d’exploiter cette faiblesse, les chercheurs ont testé trois approches : un régime restreint en tyrosine, une enzyme (TAL) qui dégrade enzymatiquement la tyrosine, et une petite molécule appelée tyrosinol qui concurrence la tyrosine pour la liaison à YARS1. Les trois réduisaient la disponibilité de la tyrosine pour la synthèse protéique, abaissaient les niveaux de NDUFB8 et SCD1, altéraient la fonction mitochondriale et augmentaient la ferroptose dans les tumeurs hépatiques, tout en montrant des effets gérables sur les tissus normaux chez la souris. Pour un non-spécialiste, le message est que les cancers du foie semblent dépendre de la tyrosine non seulement comme nutriment, mais comme carburant précis pour leur machinerie de fabrication des protéines. Cibler cette dépendance — par l’alimentation, des enzymes ou des médicaments — offre une voie prometteuse pour affaiblir les tumeurs et renforcer l’efficacité des traitements existants.
Citation: Zhang, H., Wang, Z., Zhao, Y. et al. Targeting tRNA-dependent tyrosine usage unveils a metabolic vulnerability in hepatocellular carcinoma. Nat Commun 17, 2244 (2026). https://doi.org/10.1038/s41467-026-70112-z
Mots-clés: cancer du foie, métabolisme des acides aminés, tyrosine, mitochondries, ferroptose