Clear Sky Science · fr
Identification systématique des interactions entre structures ARN spécifiques de variants et petites molécules, illustrée par les quadruplexes G de l’ARN
Pourquoi de minuscules changements dans l’ARN comptent pour les médicaments de demain
La plupart d’entre nous héritent de petites différences dans notre ADN qui nous rendent uniques. Ces variations infinitésimales peuvent remodeler subtilement les plis des molécules d’ARN à l’intérieur de nos cellules. La nouvelle étude présente une méthode permettant d’observer comment ces ajustements génétiques modifient l’affinité de médicaments expérimentaux ciblant l’ARN. Cela importe parce que le même médicament peut se comporter très différemment d’une personne à l’autre, notamment en cas de cancer ou de maladie génétique.
Une nouvelle façon de voir où les médicaments touchent l’ARN
De nombreux développeurs de médicaments s’intéressent désormais à l’ARN, et pas seulement aux protéines, comme cibles thérapeutiques. De petites molécules peuvent se fixer sur des conformations d’ARN particulières et influencer la lecture des gènes, mais jusqu’ici la plupart des méthodes ne fonctionnaient que sur une séquence « de référence ». Elles ignoraient en grande partie les innombrables substitutions d’une seule lettre observées chez de vrais patients. Les auteurs ont créé une approche à haut débit appelée BIVID-MaP qui peut tester simultanément des milliers de variantes d’ARN et localiser où une petite molécule se lie à chacune d’elles, avec une résolution d’un seul nucléotide. 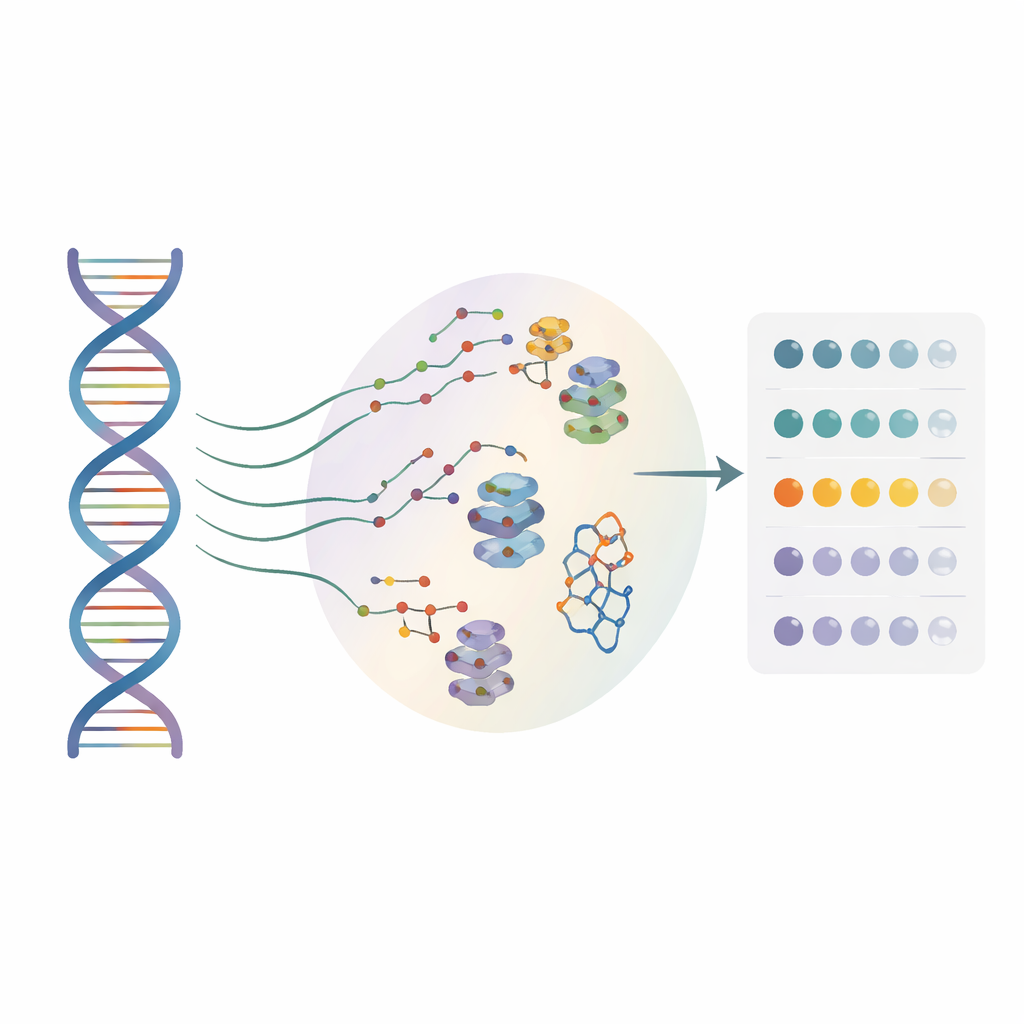
Transformer des marquages chimiques en un signal lisible
BIVID-MaP fonctionne en trois étapes principales. D’abord, l’équipe attache une étiquette réactive à une petite molécule qui se lie à l’ARN. Lorsque ce composé marqué s’insère dans sa structure d’ARN préférée, comme un quadruplex G compact formé par des séquences riches en guanines, l’étiquette forme une liaison chimique permanente avec une base d’ARN voisine. Ensuite, une enzyme spéciale copie l’ARN modifié en ADN. Lorsqu’elle rencontre l’une de ces marques chimiques, elle a tendance à « sauter » une base, créant une petite délétion dans la copie. Enfin, un séquençage profond lit ces signatures de délétion à travers des millions de molécules. Parce que presque toute la séquence environnante est préservée, les délétions peuvent être attribuées avec précision à des variants génétiques spécifiques dans un pool mixte.
Valider la méthode sur un cas-test contrôlé
Pour confirmer que BIVID-MaP détecte réellement la liaison spécifique à un variant, les chercheurs ont étudié un segment d’ARN du gène CD44 qui forme normalement un quadruplex G. Un changement unique de G en A perturbe cette structure. Dans un mélange contenant les deux versions, seule la forme intacte a montré de forts signaux de délétion près de la région repliée lorsqu’elle était exposée à une sonde dérivée de la berbérine, et des essais indépendants ont confirmé une liaison plus forte à cet endroit. Le mutant, incapable de former la même conformation, a produit bien moins de délétions et une liaison plus faible. D’autres techniques de cartographie courantes ont soit manqué cette différence, soit produit un bruit de fond déroutant, soulignant la sensibilité et la spécificité améliorées de la nouvelle approche.
Balayer les mutations liées au cancer à travers de nombreux gènes
L’équipe a ensuite monté l’échelle. Ils ont construit une bibliothèque d’ARN composée des régions non traduites 5′ (5′ UTR) de 283 gènes liés au cancer, chacune appariée à des mutations somatiques réelles rapportées dans les tumeurs. En utilisant une sonde qui reconnaît des structures analogues aux quadruplexes G, BIVID-MaP a mis en évidence de nombreuses mutations qui renforçaient ou affaiblissaient la liaison des petites molécules. Dans des gènes tels que DAXX et ING2, des substitutions d’une seule lettre dans des segments riches en guanine modifiaient nettement la liaison, en accord avec des tests biophysiques indépendants de formation de quadruplexes G et des mesures directes de liaison par spectrométrie de masse. Dans certains cas, des mutations en dehors des tracts évidents de G ont néanmoins modifié la liaison en changeant subtilement la probabilité d’appariement des bases voisines, remodelant l’« ensemble » structural sans altérer grossièrement le repli global prédit. 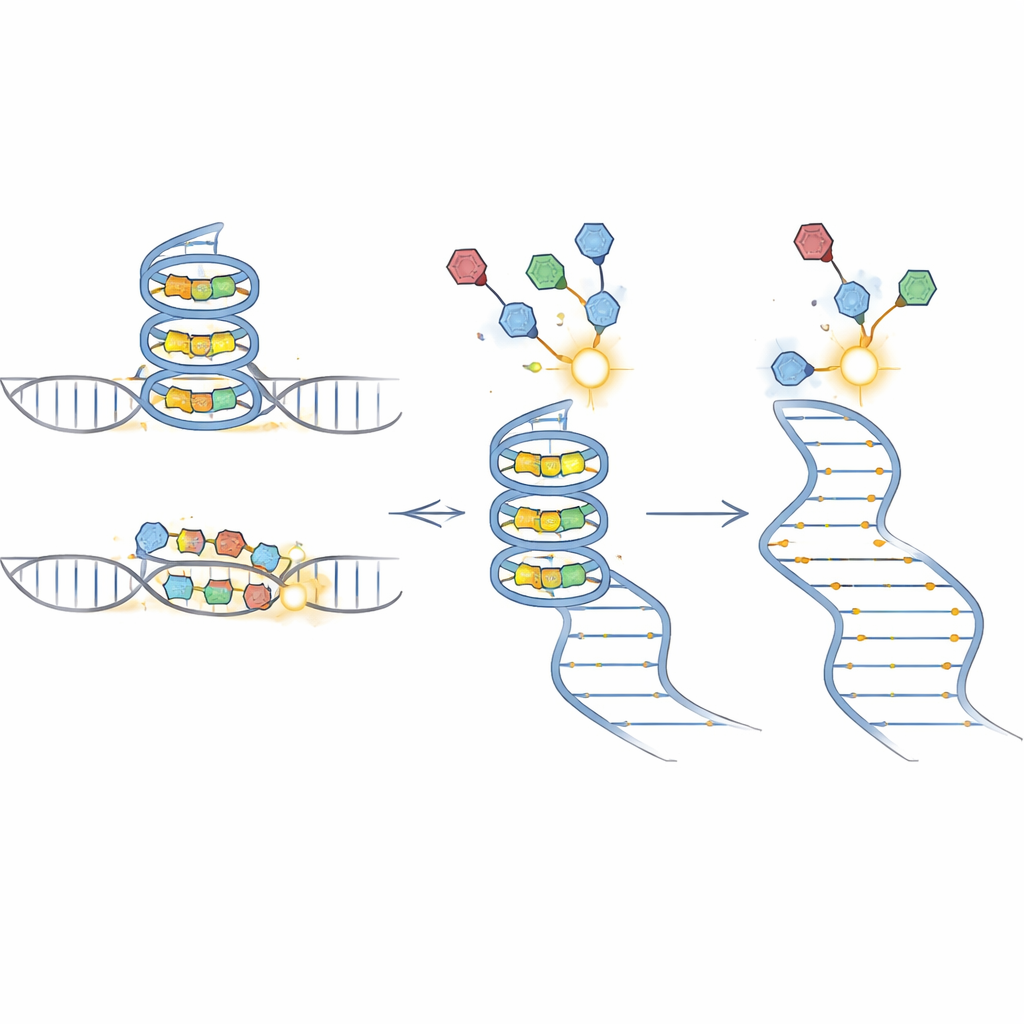
Ce que les prédictions informatiques manquent
Il est important de noter que les outils existants de prédiction de structure ARN et de quadruplexes G ont souvent échoué à prévoir les changements révélés par BIVID-MaP. Certains variants qui modifiaient à peine les scores computationnels engendraient de grandes différences réelles de liaison. D’autres semblaient affecter la liaison à une famille de composés ciblant les quadruplexes G, tandis que certaines mutations avaient des effets spécifiques à un médicament. Cela montre que des variants d’un seul nucléotide peuvent moduler le paysage des plis de l’ARN et des contacts médicamenteux d’une manière difficile à déduire à partir de la seule séquence.
Ce que cela signifie pour les médicaments ARN personnalisés
Les auteurs concluent que BIVID-MaP offre une voie puissante pour cartographier comment des différences génétiques individuelles remodelent les structures ARN et leurs interactions avec les petites molécules. En convertissant des modifications chimiques locales en signatures de délétion précises, la méthode peut sonder des milliers de variants en parallèle et mettre en évidence ceux qui modifient de façon significative la liaison aux médicaments. À long terme, de telles cartes pourraient orienter la conception de médicaments ciblant l’ARN plus efficaces et plus sûrs pour des patient·e·s hétérogènes, et révéler des structures ARN jusque-là cachées susceptibles de servir de nouvelles cibles médicamenteuses.
Citation: Miyashita, E., Onizuka, K., Chen, Y. et al. Systematic identification of variant-specific RNA structure-small molecule interactions exemplified by RNA G-quadruplexes. Nat Commun 17, 2243 (2026). https://doi.org/10.1038/s41467-026-70097-9
Mots-clés: Médicaments ciblant l’ARN, Quadruplex G, variants génétiques, liaison de petites molécules, mutations cancéreuses