Clear Sky Science · fr
Optimisation de l’organisation spatiale des anneaux FtsZ pour une constriction à grande échelle dans des cellules synthétiques
Pourquoi les petits anneaux comptent pour construire des cellules synthétiques
Imaginez construire une cellule artificielle simple capable de croître et de se diviser seule. Pour y parvenir, les scientifiques doivent apprendre à pincer une membrane souple, semblable à une bulle de savon, de façon contrôlée en n’utilisant qu’un petit nombre de composants biologiques. Cette étude montre comment une protéine bactérienne peut être aidée à former de grands anneaux stables sur d’immenses bulles lipidiques, permettant à ces « cellules » modèles de se contracter presque jusqu’à la division. Elle révèle quel type d’architecture protéique est nécessaire pour plier et remodeler une membrane à l’échelle d’une cellule entière.
Emprunter l’outillage de la division naturelle
De nombreuses bactéries se divisent en utilisant une protéine appelée FtsZ, un lointain cousin de la tubuline qui compose le squelette interne de nos propres cellules. FtsZ s’assemble en filaments qui se rassemblent en un anneau au milieu de la cellule, marquant l’endroit où celle‑ci se scindera. Dans les bactéries vivantes, une foule de protéines auxiliaires attache cet anneau à la membrane interne, le positionne au milieu et le relie à des enzymes qui remodèlent la paroi cellulaire. Les tentatives précédentes en laboratoire pour recréer cette machinerie dans des vésicules de taille cellulaire avaient réussi à former des anneaux et à provoquer de petites déformations de la membrane, mais pas une constriction progressive et lisse remodelant une grande vésicule en deux moitiés presque séparées.
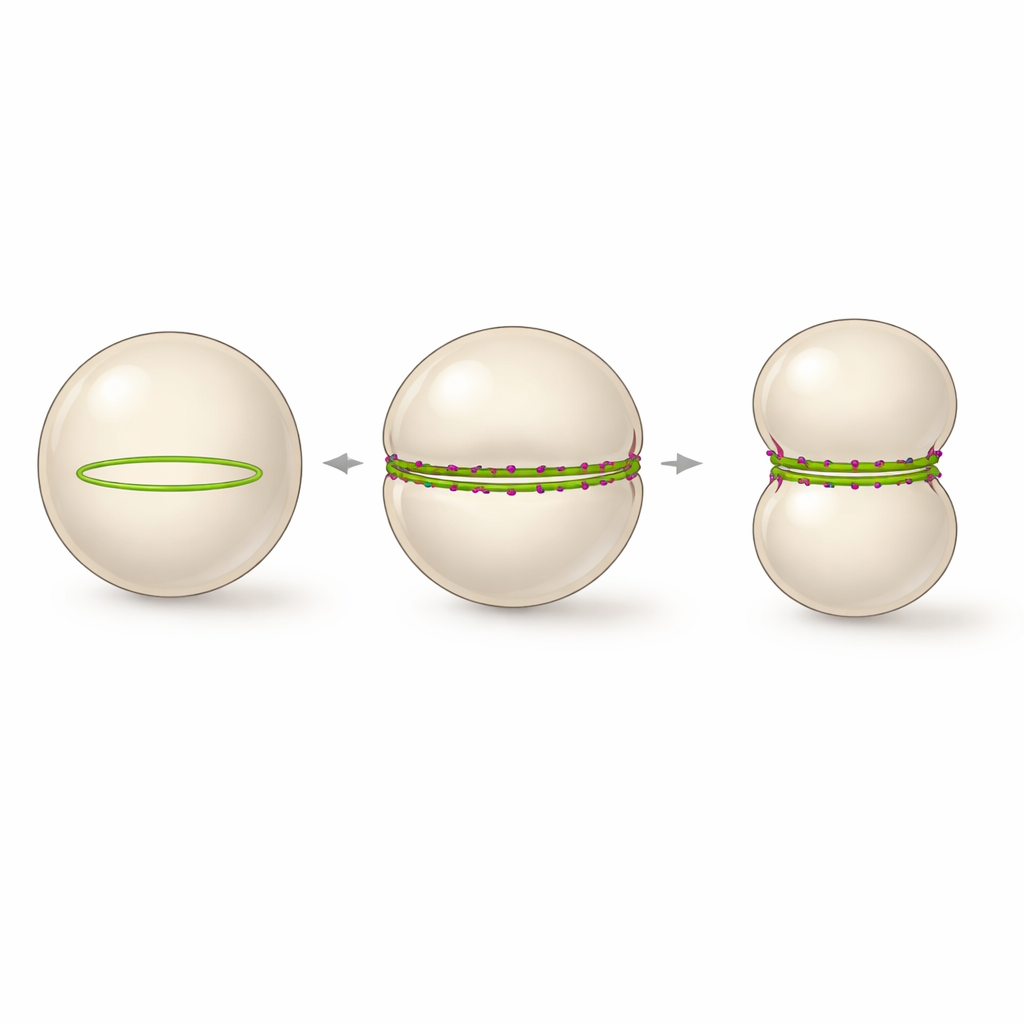
Une approche minimaliste d’une coque en division
Les auteurs se sont demandé s’ils pouvaient réduire ce système à seulement deux éléments : une version de FtsZ capable de se fixer directement aux membranes, et une courte queue chargée positivement d’une autre protéine de division, FtsN. Ils ont encapsulé ces composants à l’intérieur de grandes vésicules uniloculaires — des sphères creuses de lipides ressemblant à des cellules simplifiées — et leur ont fourni la molécule d’énergie GTP ainsi qu’un analogue de GTP à action lente pour régler la dynamique protéique. Sans la queue de FtsN, FtsZ formait de nombreux petits anneaux et taches qui ne provoquaient que des enfoncements locaux. Avec un excès du fragment de FtsN (appelé cytoFtsN), ces petits anneaux se réorganisaient en un seul grand anneau qui entourait la vésicule près de son équateur et pouvait se contracter sur plusieurs heures.
D’un réseau embrouillé à un anneau contractile unique
Pour comprendre comment ce petit peptide modifie si radicalement le comportement, l’équipe a observé les filaments de FtsZ sur des membranes supports plates à l’aide d’une microscopie haute résolution. Normalement, FtsZ sur de telles surfaces forme des vortex tourbillonnants et courbés. L’ajout de quantités croissantes de cytoFtsN effaçait progressivement ces spirales et les remplaçait par des faisceaux plus droits et mieux alignés. L’analyse quantitative des images a confirmé que le réseau devenait plus cohérent et ordonné à mesure que la concentration en peptide augmentait. Des expériences de récupération de fluorescence ont montré que les sous‑unités au sein de ces faisceaux s’échangeaient plus lentement, indiquant que le peptide stabilise les filaments et réduit leur dynamique de remaniement.

« Velcro » électrostatique qui verrouille les filaments
Des mesures biochimiques ont révélé que cytoFtsN et FtsZ interagissent principalement par des charges électriques opposées : FtsZ est globalement négatif, tandis que le peptide porte des grappes de charges positives. À des niveaux de sel plus faibles, le peptide se liait plus fortement, favorisait la formation de faisceaux de FtsZ plus épais en solution et ralentissait la dégradation des filaments en atténuant l’activité de consommation de GTP de la protéine. Lorsque les chercheurs modifiaient des résidus clés porteurs de charges positives dans le peptide, ou augmentaient la concentration en sel pour écrêter l’attraction électrostatique, les effets d’assemblage en faisceaux et de réorganisation disparaissaient. Cela suggère un mécanisme physique simple dans lequel le peptide chargé positivement agit comme un « Velcro » moléculaire, réduisant la répulsion entre filaments FtsZ pour qu’ils puissent s’aligner côte à côte en faisceaux rigides.
Comment un anneau unique reconfigure une grande vésicule
À l’intérieur des vésicules, ce rassemblement stabilisé par le peptide a une conséquence frappante. Au lieu de nombreux petits anneaux courbés, les faisceaux redressés de FtsZ sont contraints de suivre la grande courbure de la vésicule et s’assemblent en un anneau continu qui parcourt toute la circonférence. L’imagerie en time‑lapse a montré que chaque fois qu’un tel anneau complètement fermé se formait, la vésicule se déformait de façon fiable d’une sphère en une forme en haltère, avec une taille resserrée là où se trouvait l’anneau. Le processus a pu être suivi en temps réel alors que le diamètre de la vésicule diminuait et que la constriction s’approfondissait, frôlant la séparation du compartiment en deux, bien que la scission finale n’ait pas été atteinte. Les auteurs proposent qu’un anneau FtsZ stable, traversant l’équateur et avec un renouvellement ralenti mais toujours actif, constitue l’architecture minimale nécessaire pour conduire une constriction membranaire à grande échelle dans une cellule synthétique.
Ce que cela signifie pour la vie synthétique future
En montrant qu’une variante de FtsZ ancrée à la membrane plus un court peptide cationique peuvent remodeler de grandes vésicules lipidiques presque jusqu’à la division, ce travail définit une règle de conception claire pour les cellules artificielles : un anneau protéique unique et cohérent, de taille adaptée à la cellule et mécaniquement stable dans le temps, suffit à pincer une frontière souple à l’échelle cellulaire. Des facteurs plus complexes peuvent encore être nécessaires pour couper complètement la membrane, mais l’étude démontre que la constriction contrôlée à grande échelle ne requiert pas toute la panoplie des protéines de division bactériennes. Au contraire, un réglage fin de l’organisation et de la dynamique des filaments peut transformer un échafaudage protéique simple en un anneau contractile efficace, rapprochant d’un pas les cellules synthétiques véritablement auto‑divisantes.
Citation: Panevska, A., Šakanović, A., Paccione, G. et al. Optimizing spatial organization of FtsZ rings for large-scale constriction in synthetic cells. Nat Commun 17, 2320 (2026). https://doi.org/10.1038/s41467-026-70091-1
Mots-clés: division de cellules synthétiques, anneau FtsZ, constriction membranaire, divisome minimal, auto-organisation du cytosquelette