Clear Sky Science · fr
La protéomique subcellulaire révèle un plan d’intégration de l’endosymbionte chez le trypanosomatide Angomonas deanei
Partenaires cachés à l’intérieur des êtres unicellulaires
De nombreux organismes unicellulaires ne sont pas vraiment seuls. Certains abritent des bactéries qui vivent à l’intérieur d’eux comme des locataires permanents, échangeant nourriture et services dans des relations qui évoquent l’origine de nos propres mitochondries. Cette étude explore un tel partenariat chez Angomonas deanei, un parasite microscopique d’insectes, pour montrer comment une bactérie autrefois libre est devenue profondément intégrée au fonctionnement interne de la cellule hôte.
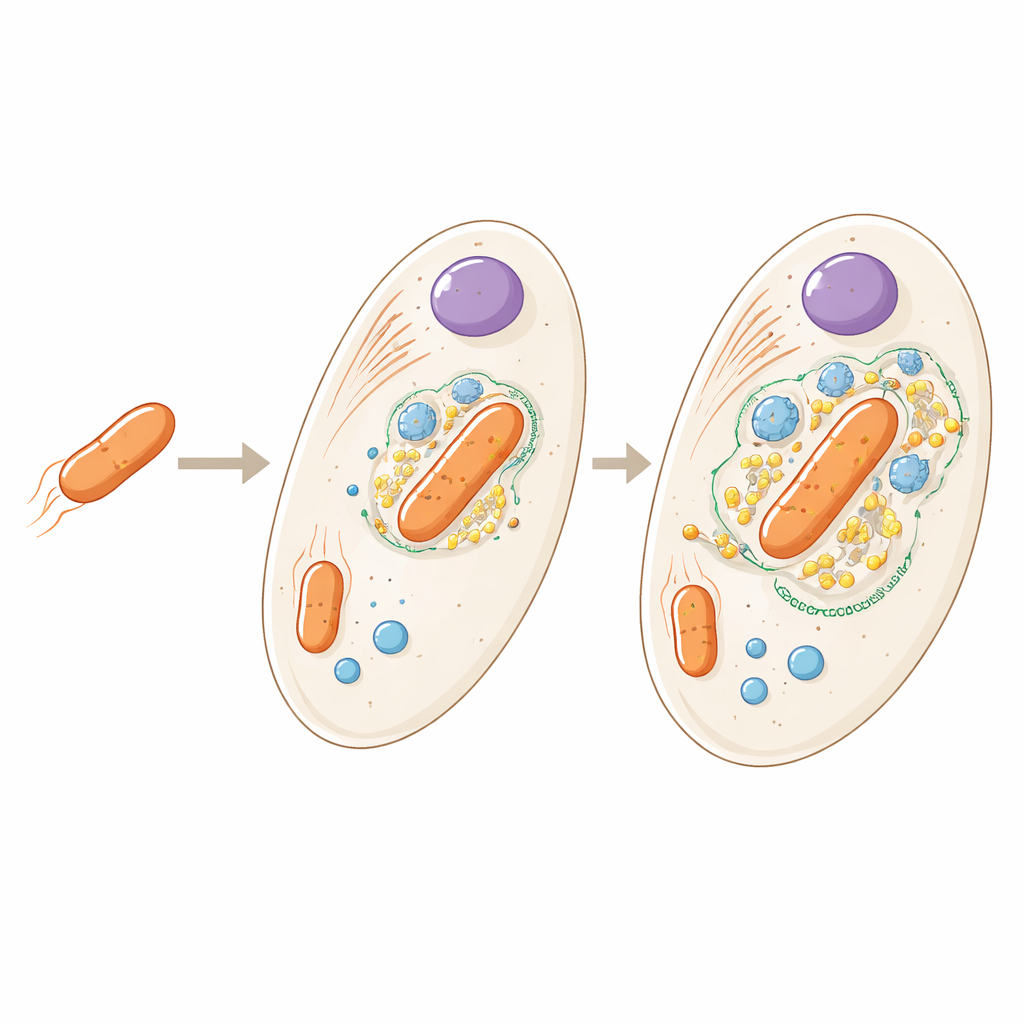
Du pensionnaire à la pièce intégrée
La bactérie vivant à l’intérieur d’Angomonas deanei est une parente lointaine des microbes du sol libres, mais ici elle existe à raison d’un exemplaire par cellule hôte et ne peut plus survivre seule. Des travaux antérieurs ont montré que l’hôte produit des protéines particulières qui pénètrent dans la bactérie et contribuent même à contrôler son cycle de division. La nouvelle étude pose une question plus large : si l’on cartographie l’ensemble de la cellule, où se trouvent exactement toutes les protéines de l’hôte et de la bactérie, et qu’est‑ce que cela révèle sur le degré d’intégration entre les deux partenaires ?
Cartographier la ville intérieure de la cellule
Pour répondre, les chercheurs ont ouvert doucement un grand nombre de cellules afin de préserver en grande partie les structures internes. Ils ont ensuite séparé ces fragments en les centrifugeant à différentes vitesses et ont identifié des milliers de protéines dans chaque fraction par spectrométrie de masse haute résolution. En comparant la manière dont les protéines se regroupaient dans les fractions, et en croisant ces données avec des marqueurs connus et la microscopie en fluorescence, ils ont créé un « annuaire » détaillé de la cellule, assignant près de 3 000 protéines à 21 régions distinctes telles que le noyau, la mitochondrie, des corps de stockage spécialisés et l’endosymbionte bactérien lui‑même.
Des outils de l’hôte ciblant la bactérie hébergée
Dans cet atlas, l’équipe a mis au jour un ensemble de protéines d’origine hôte qui accompagnaient systématiquement l’endosymbionte, étendant la collection connue de protéines dites ciblant l’endosymbionte. Un exemple nouvellement confirmé, baptisé ETP10, enrobe la bactérie de la même manière qu’une protéine décrite précédemment, suggérant un échafaudage de facteurs hôtes entourant le partenaire microbien. Un autre petit groupe de protéines partageait un comportement physique inhabituel avec une protéine de type dynamine déjà connue pour pincer la bactérie lors de sa division. Ensemble, ces résultats suggèrent l’existence d’une machinerie spécialisée, construite par l’hôte, dédiée au positionnement, à la mise en forme et à la reproduction de l’endosymbionte dans la cellule.
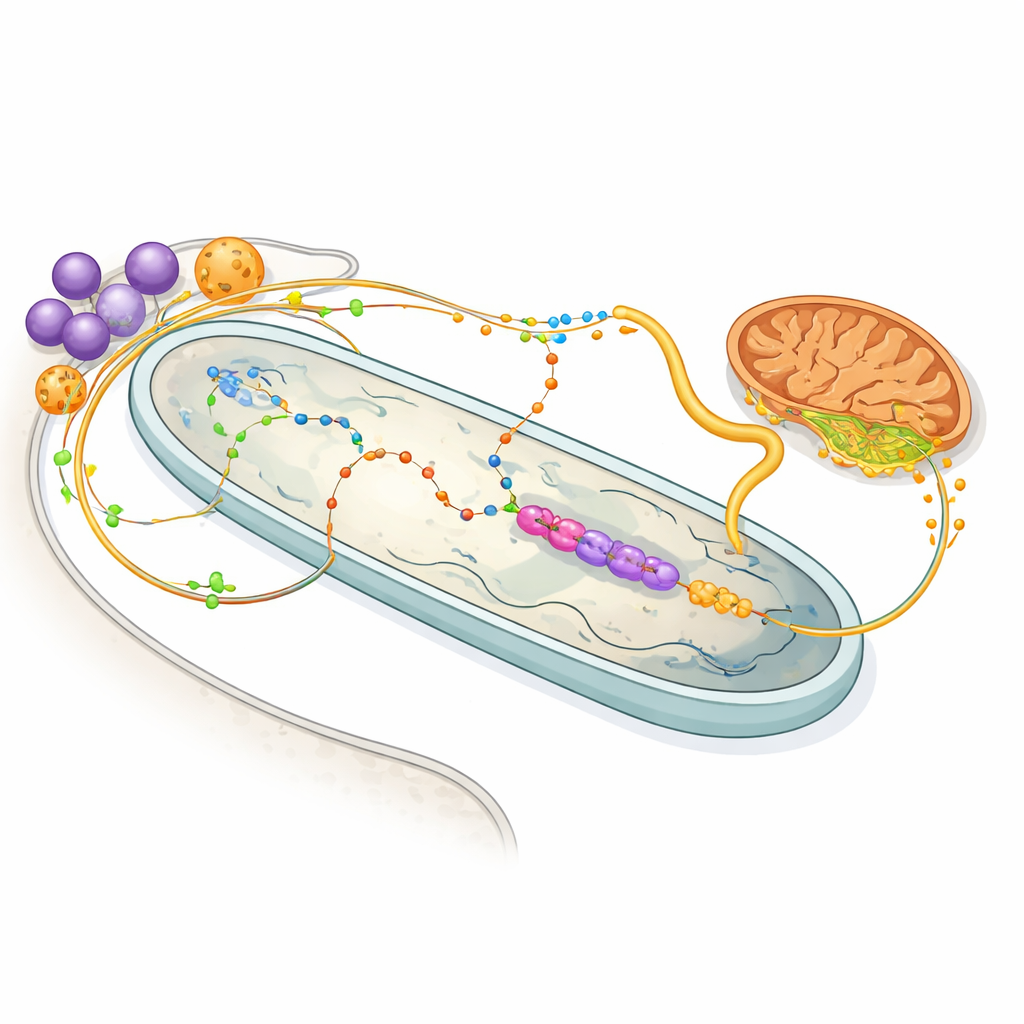
Partage d’énergie et routes d’échanges chimiques
La carte protéique éclaire aussi l’intense trafic moléculaire entre l’hôte et la bactérie. Des enzymes des glycosomes de l’hôte — organites gérant le métabolisme des sucres et des acides aminés — semblent configurées pour fournir à la bactérie l’acide aminé proline et le composé 2‑oxoglutarate, deux sources d’énergie précieuses. À l’intérieur de la bactérie, un ensemble épuré d’enzymes utilise le 2‑oxoglutarate pour générer du NADH, qui alimente une chaîne respiratoire minimale, puis renvoie du succinate à la mitochondrie de l’hôte. D’autres voies montrent que la bactérie réalise la plupart des étapes de la synthèse de l’hème, un pigment vital pour l’hôte, tout en fournissant des éléments essentiels pour la synthèse des nucléotides. En pratique, chaque partenaire s’est déchargé de tâches métaboliques spécifiques sur l’autre, créant un système partagé et interdépendant.
Nouvelles voies de communication au sein de la cellule
Au‑delà du métabolisme, l’étude révèle des liens physiques et probablement de signalisation entre l’endosymbionte et d’autres organites. Un groupe distinct de protéines hôtes forme ce que les auteurs appellent un cluster de « sites de contact », enrichi en composants de l’enveloppe nucléaire et du réticulum endoplasmique qui co‑sédimentent physiquement avec la bactérie. Deux types d’organites de stockage — les glycosomes et les acidocalcisomes — apparaissent en deux populations : certains restent libres dans le cytoplasme, tandis que d’autres accompagnent systématiquement la bactérie. La microscopie confirme que des sous‑ensembles de ces organites se nichent étroitement contre l’endosymbionte. Les acidocalcisomes sont connus comme réservoirs de calcium et de phosphate ; leur proximité suggère donc une voie bidirectionnelle de signalisation et de trafic ionique reliant la bactérie, ces stocks et le réticulum endoplasmique voisin.
Un plan montrant la fusion de vies au sein d’une cellule
Pris dans leur ensemble, ces travaux fournissent un plan riche et à l’échelle cellulaire de la manière dont une bactérie peut devenir fonctionnellement fusionnée à son hôte sans s’être encore transformée en un organite complet comme la mitochondrie. Angomonas deanei dépend de son endosymbionte pour des nutriments clés, tandis que la bactérie dépend, en retour, de protéines fabriquées par l’hôte et de molécules riches en énergie, et elle est attachée aux organites de l’hôte pour la communication et le contrôle. Pour le grand public, la conclusion est que l’évolution peut progressivement câbler la coopération entre des formes de vie très différentes, étape par étape, jusqu’à rendre leur séparation impossible. Ce système offre un instantané vivant de ce processus en action, aidant les scientifiques à mieux comprendre comment des cellules complexes comme la nôtre sont autrefois apparues à partir de débuts plus simples.
Citation: Hammond, M., Chmelová, Ľ., van Geelen-Kuenzel, N.A. et al. Subcellular proteomics reveals a blueprint for endosymbiont integration in trypanosomatid Angomonas deanei. Nat Commun 17, 2241 (2026). https://doi.org/10.1038/s41467-026-70084-0
Mots-clés: endosymbiose, métabolisme cellulaire, évolution des organites, biologie des protistes, interactions hôte‑microbe