Clear Sky Science · fr
Le mode de vie d’Acinetobacter baumannii inclut la colonisation des sols riches en végétaux en décomposition et une dispersion par voie aérienne
Pourquoi la vie sauvage de ce germe hospitalier vous concerne
Acinetobacter baumannii est surtout connu comme un germe hospitalier difficile à éliminer, capable de résister à de nombreux antibiotiques. Cette étude montre que le même microbe mène aussi une vie riche en extérieur — dans le sol, les végétaux en décomposition, les animaux et même dans l’air. En révélant ses sources et ses modes de dispersion, ce travail aide à expliquer pourquoi cette bactérie est si résistante et pourquoi elle réapparaît régulièrement dans les hôpitaux du monde entier.

Vie cachée dans les champs, les rivières et les nids d’oiseaux
Les chercheurs sont partis d’un indice inattendu : des poussins de cigogne blanche en Pologne portaient souvent A. baumannii dans leurs voies aériennes supérieures, loin de tout hôpital. En suivant l’alimentation et l’environnement des oiseaux, l’équipe a retracé la bactérie non pas vers les insectes ou les poissons, mais principalement vers de petits mammifères, des vers de terre et — surtout — des sols humides riches en matière végétale en décomposition le long des rivières et dans des tas de compost. Les sols forestiers, même en bordure de ruisseaux, hébergeaient rarement la bactérie, tandis que certains berges fluviales hors des forêts faisaient parfois office de « points chauds » où coexistaient de nombreuses souches différentes.
Des plantes en décomposition à l’air libre
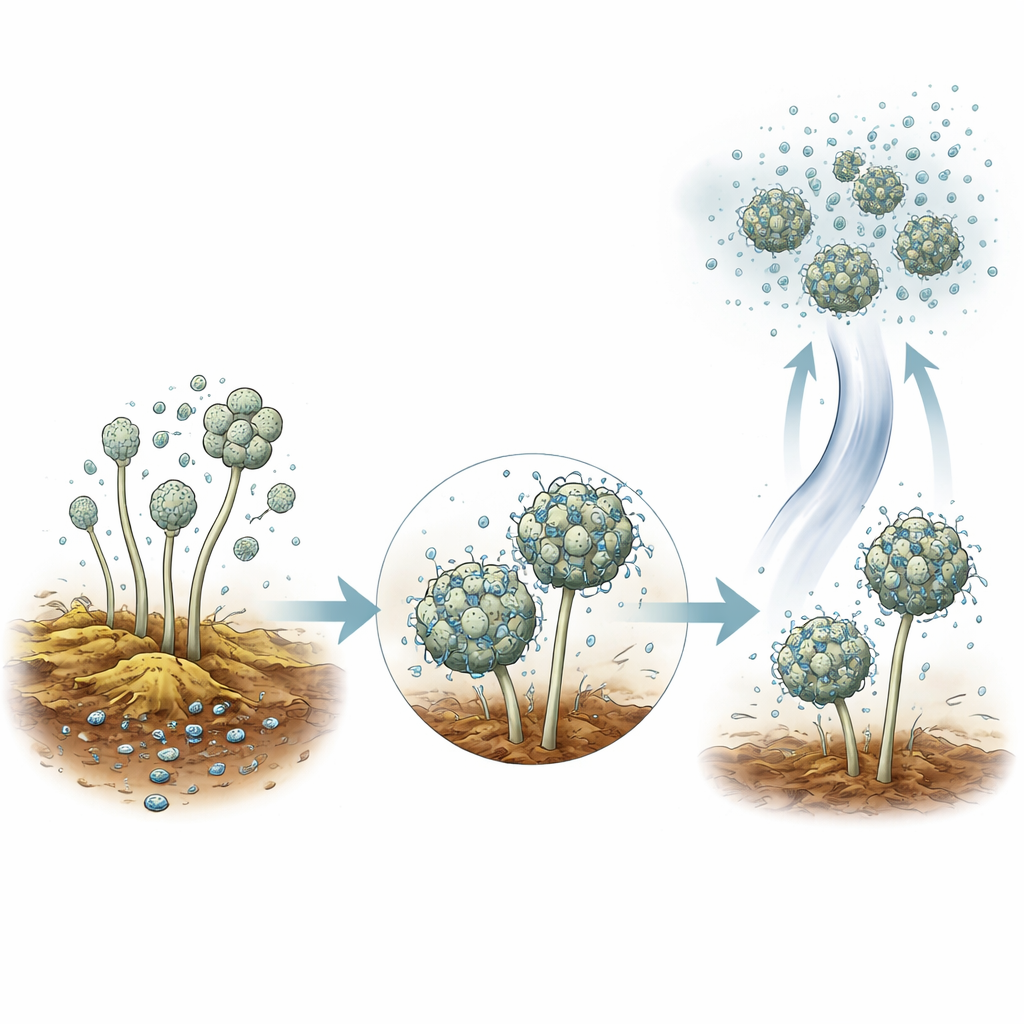
Des expériences de terrain soigneuses ont montré qu’A. baumannii est attiré par la matière végétale en décomposition. Lorsque les auteurs ont placé des résidus végétaux stérilisés dans des jardins, le matériau a été colonisé en quelques semaines — même lorsqu’il était surélevé au‑dessus du sol et accessible uniquement par l’air. Des pièges à air positionnés juste au‑dessus de tas de compost actifs ont également capturé la bactérie. En laboratoire, l’équipe a constaté qu’A. baumannii adhère volontiers aux spores de moisissures courantes comme Aspergillus et Penicillium. Les bactéries enrobaient progressivement les spores et ralentissaient même leur capacité à germer. Comme les spores fongiques se dispersent facilement dans l’air depuis le compost et les sols, ce partenariat étroit offre un moyen simple pour la bactérie de s’embarquer dans l’atmosphère.
Voyageurs globaux aux racines anciennes
Pour comprendre le lien entre ces souches sauvages et les souches hospitalières, l’équipe a séquencé 401 nouveaux génomes provenant de cigognes, sols, plantes, vers, rongeurs et autres sources, et les a comparés à des centaines de génomes disponibles publiquement. L’arbre généalogique obtenu a révélé une dispersion remarquable : des isolats environnementaux, animaux et cliniques humains étaient éparpillés sur les mêmes branches, souvent séparés par seulement quelques modifications de l’ADN. Certains proches apparentés presque identiques ont été trouvés sur différents continents, ce qui implique que les mêmes lignées ont traversé les océans en quelques décennies seulement. Sur la base du taux d’accumulation des mutations, les auteurs estiment qu’A. baumannii en tant qu’espèce est étonnamment jeune — de l’ordre de 15 000 ans — et qu’il a connu une diversification rapide à l’époque où l’homme a commencé les cultures à grande échelle et le défrichement des forêts.
Une vaste boîte à outils génétique, mais peu d’empreinte humaine dans la nature
En combinant tous les génomes, les chercheurs ont estimé que l’ensemble génétique combiné de l’espèce — le pan‑génome — contient environ 51 000 familles de gènes distinctes, soit plus du double des estimations précédentes. Cette énorme boîte à outils génétique sous‑tend probablement sa capacité à s’adapter à la sécheresse extrême, aux radiations, aux désinfectants et aux antibiotiques. Pourtant, la plupart des isolats sauvages et des sols ne portaient qu’un petit nombre de gènes de résistance reconnus et peu d’éléments d’ADN mobiles, contrairement aux souches hospitalières qui regorgent de telles caractéristiques. Ce schéma suggère que les populations naturelles échantillonnées sont encore relativement peu affectées par l’usage moderne des antibiotiques, offrant une vue « de référence » de l’espèce avant son adaptation complète aux milieux hospitaliers.
Ce que cela signifie pour les hôpitaux et la santé publique
L’étude présente A. baumannii non pas comme un problème purement fabriqué par l’homme, mais comme une bactérie naturellement aéroportée, associée aux plantes et aux sols, qui n’a commencé que récemment à exploiter les hôpitaux et les installations d’élevage comme nouveaux habitats. Son association avec les champignons, sa tolérance aux conditions difficiles et sa grande diversité génétique la rendent apte aux voyages atmosphériques de longue distance et à une évolution rapide. Pour le grand public, la conclusion est que la lutte contre les infections ne peut pas se limiter à la transmission patient à patient à l’intérieur des hôpitaux. Les pics saisonniers, les environnements intérieurs contaminés par des moisissures, les installations de compostage et les changements d’usage des terres influent tous sur le moment et la manière dont ce germe résilient pénètre les milieux humains — et comprendre son mode de vie extérieur est essentiel pour anticiper l’émergence future de souches résistantes aux médicaments.
Citation: Wilharm, G., Skiebe, E., Michalska, A. et al. Acinetobacter baumannii’s lifestyle includes soil-dwelling colonization of decaying plant material and airborne spread. Nat Commun 17, 2316 (2026). https://doi.org/10.1038/s41467-026-70072-4
Mots-clés: Acinetobacter baumannii, bactéries aéroportées, microbiome du sol, résistance aux antibiotiques, One Health