Clear Sky Science · fr
La distribution dynamique des amplifications génétiques en tandem dans une population hétéro-résistante d’Escherichia coli révélée par un séquençage ultra-profond en longues lectures
Poches cachées de survie
Lorsque les médecins traitent des infections bactériennes par des antibiotiques, ils supposent que l'ensemble de la population microbienne réagira de la même façon. Mais parfois, une infime fraction résiste discrètement, survit au traitement et prépare le terrain pour un échec ou une rechute. Cette étude dévoile comment surviennent ces rares survivants et comment leur fréquence évolue dans le temps chez Escherichia coli, et présente une méthode puissante pour observer ces changements génétiques se produire cellule par cellule.
Petites répétitions génétiques, grandes conséquences
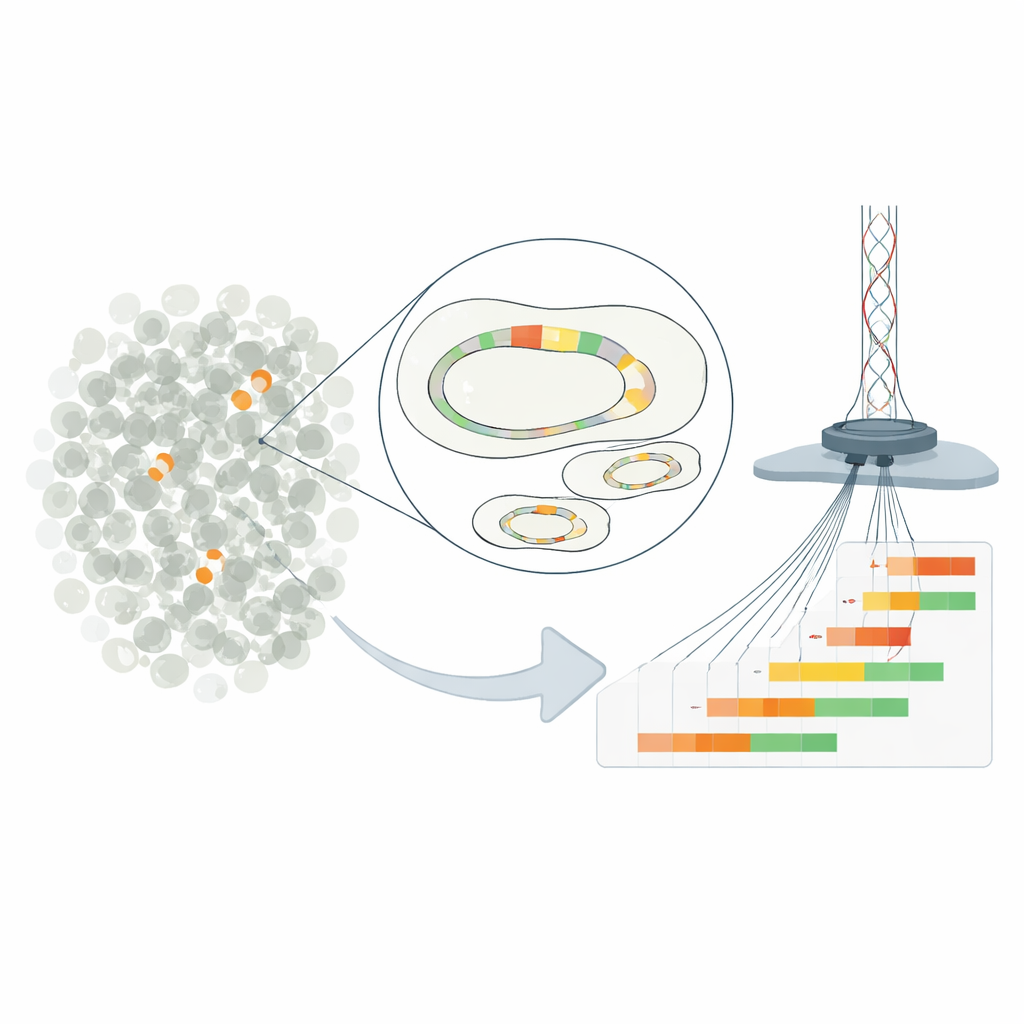
Le travail porte sur la « hétéro-résistance », une situation où la plupart des bactéries d’un échantillon semblent sensibles à un médicament, tandis qu’une minorité peut supporter des doses beaucoup plus élevées. Dans la souche d’E. coli étudiée, ce phénomène provient de copies répétées d’un gène de résistance porté par un plasmide — un petit cercle d’ADN séparé du chromosome principal. En dupliquant un court segment d’ADN contenant un gène de bêta-lactamase, les bactéries peuvent augmenter la production d’une enzyme qui dégrade l’antibiotique piperacilline-tazobactam. Plus une cellule porte de répétitions, plus elle produit d’enzyme et meilleures sont ses chances de survie en présence du médicament.
Lire les cercles d’ADN avec un niveau de détail sans précédent
Les méthodes traditionnelles ne peuvent estimer que le nombre moyen de copies de gènes sur l’ensemble d’une population bactérienne, masquant la riche diversité entre cellules individuelles. Pour contourner cela, les chercheurs ont modifié le plasmide clinique de sorte qu’il puisse être coupé en un endroit précis puis isolé du reste du génome. Ils ont utilisé un séquençage Nanopore ultra-profond en longues lectures pour lire les molécules plasmidiques entières d’un bout à l’autre, comptant exactement combien d’unités répétées de résistance chacune contenait. Cette approche a atteint une résolution allant jusqu’à une cellule sur 100 000, révélant des plasmides portant de zéro à plus d’une douzaine de copies coexistant dans la même culture. Des contrôles par d’autres techniques ont confirmé que, en moyenne, la nouvelle méthode rapportait des nombres de copies précis.
Comment les antibiotiques reconfigurent la population
Avec cet outil, l’équipe a suivi ce qui se passait lorsqu’elle exposait des cultures d’E. coli à des doses croissantes de piperacilline-tazobactam, puis retirait le médicament. À mesure que le niveau d’antibiotique augmentait, la distribution globale a basculé vers des plasmides portant davantage de copies du gène de résistance, mais les cellules avec moins de copies n’ont jamais totalement disparu. Lorsque le médicament a été retiré et que les bactéries ont été cultivées pendant des centaines de générations, la population est revenue progressivement vers des nombres de copies plus faibles et n’est jamais redevenue complètement identique à l’état initial. Des tests de croissance séparés ont montré que chaque copie supplémentaire du gène conférait une augmentation mesurable de la tolérance au médicament, liant étroitement les distributions génétiques observées au profil d’hétéro-résistance visible dans les tests de laboratoire standard.

Protection par les voisins et coûts discrets
Pour expliquer pourquoi les cellules à faible nombre de copies persistaient même sous un traitement intensif, les auteurs ont construit un modèle mathématique combinant la croissance bactérienne, la dégradation de l’antibiotique et les événements aléatoires qui ajoutent ou retirent des copies de gènes. Les simulations ont montré que la « résistance indirecte » joue un rôle clé : les cellules fortement résistantes sécrètent suffisamment de bêta-lactamase pour abaisser la concentration de médicament dans l’environnement partagé, protégeant ainsi par ricochet les voisins moins résistants. Tant que les copies supplémentaires n’imposent qu’un faible coût de croissance en l’absence de médicament, cet effet protecteur contribue à maintenir une large répartition des nombres de copies, ralentissant le retour à une population entièrement sensible. Le modèle a aussi montré comment une adaptation ordinaire au milieu de culture — des mutations indépendantes qui améliorent la croissance — peut verrouiller certains états de nombre de copies en rendant certaines sous-populations plus aptes que d’autres.
Pourquoi cela compte pour les patients et au-delà
Pour les non-spécialistes, le message est qu’une culture bactérienne n’est pas un ennemi uniforme : c’est un mélange en constante évolution d’individus ayant des capacités différentes à survivre aux antibiotiques. En comptant directement les copies de gènes sur des milliers de molécules d’ADN uniques, cette étude relie de manière quantitative cette diversité cachée à une résistance pertinente pour le traitement. De telles connaissances pourraient améliorer l’utilisation du séquençage génomique pour prédire des hétéro-résistances difficiles à détecter, aider à identifier des souches bactériennes particulièrement susceptibles de causer des échecs thérapeutiques et orienter la conception de meilleurs tests diagnostiques. Comme les amplifications géniques en tandem favorisent aussi une adaptation rapide chez les virus, les tumeurs et d’autres organismes, la même stratégie pourrait être adaptée bien au-delà d’E. coli, offrant une nouvelle fenêtre sur la façon dont des fragments répétés d’ADN aident les organismes à échapper aux menaces.
Citation: Jonsson, S., Guliaev, A., Berryhill, B.A. et al. The dynamic distribution of genetic tandem amplifications in a heteroresistant Escherichia coli population revealed by ultra-deep long read sequencing. Nat Commun 17, 2113 (2026). https://doi.org/10.1038/s41467-026-70044-8
Mots-clés: hétéro-résistance aux antibiotiques, amplification génique, Escherichia coli, séquençage long-read, bêta-lactamase