Clear Sky Science · fr
La dynamique à l’échelle d’une seule molécule révèle que la liaison de l’ATP seule alimente le translocateur de substrat d’un transporteur ABC
Pourquoi les petites pompes cellulaires comptent
Chaque cellule de votre corps dépend de machines microscopiques qui déplacent des molécules à travers des membranes, influençant tout, de l’absorption des nutriments à la défense immunitaire. Une grande classe de ces machines, appelées transporteurs ABC, utilise le carburant chimique cellulaire ATP pour pousser des cargaisons à contre-gradient. Pourtant, pendant des décennies, les scientifiques ont débattu d’une question fondamentale : l’acte simple de liaison de l’ATP suffit‑il à alimenter l’étape de transport, ou l’énergie n’est‑elle libérée que lorsque l’ATP est hydrolysé ? Cette étude zoome sur un seul transporteur, molécule par molécule, pour trancher le débat.
Observer un transporteur à la fois
Plutôt que de mesurer le comportement combiné de millions de molécules, les chercheurs ont construit un dispositif leur permettant de suivre des événements de transport individuels en temps réel. Ils se sont concentrés sur TmrAB, un cousin bactérien du transporteur humain TAP qui charge des peptides immunitaires pour présentation aux lymphocytes T cytotoxiques. TmrAB est ancré dans une membrane et transporte de courts fragments protéiques (peptides) d’un côté à l’autre en utilisant l’ATP. Pour voir chaque étape de transport, l’équipe a piégé une seule molécule de TmrAB dans une bulle membranaire artificielle (une liposome) et a enfermé à l’intérieur de cette bulle une protéine « capteur » spécialement conçue qui modifie sa fluorescence lorsqu’elle capture un peptide. À l’aide d’un microscope très sensible, ils ont pu observer, sous forme de sauts brefs dans le signal lumineux, les instants exacts où un peptide après l’autre arrivait à l’intérieur de la bulle.
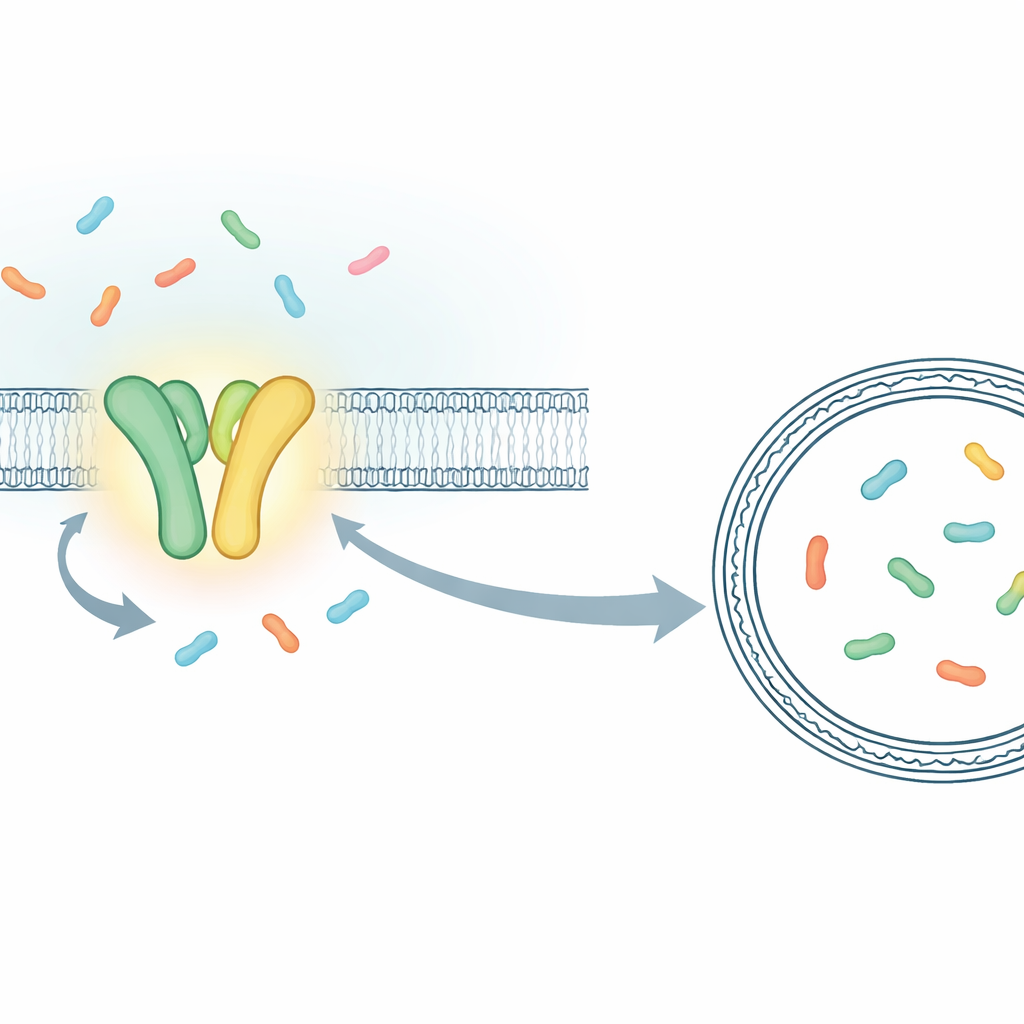
Prouver qu’une liaison d’ATP déplace un peptide
Avec ce test monocellulaire en main, les chercheurs ont comparé le TmrAB normal à une version modifiée à turnover lent dont les cycles sont étirés dans le temps. La variante lente a permis de distinguer des événements individuels qui autrement se confondraient. Ils ont montré que lorsque l’ATP et les peptides étaient présents simultanément, le capteur à l’intérieur de la liposome basculait de son état « vide » à son état « chargé » par étapes discrètes, chacune correspondant au transport d’un seul peptide. En analysant la vitesse à laquelle le capteur se refermait autour des peptides et en estimant le minuscule volume à l’intérieur de chaque liposome, ils ont même pu traduire ces changements de lumière en concentrations approximatives de peptides. Les chiffres correspondaient à ce qu’on attendrait si un puis deux peptides s’accumulaient dans des bulles d’environ 100 nanomètres de diamètre, confirmant qu’ils comptaient bien les événements de transport un par un.
La liaison de l’ATP seule déclenche l’interrupteur moléculaire
La controverse clé concerne les ions magnésium (Mg2+), qui accompagnent normalement l’ATP dans les cellules et sont connus pour être nécessaires à une hydrolyse efficace de l’ATP. Certains modèles suggéraient que le Mg2+ pourrait aussi être nécessaire à la liaison de l’ATP ou à la fermeture du transporteur. Pour démêler ces rôles, les chercheurs ont éliminé le Mg2+ à l’aide d’un chélateur tout en fournissant de l’ATP. Dans ces conditions, tant le transporteur normal que la version lente ont pu effectuer exactement une étape de transport de peptide par molécule, puis se sont arrêtés. Ce comportement indique que l’ATP peut encore se lier et forcer le transporteur à passer d’une conformation tournée vers l’intérieur à une conformation tournée vers l’extérieur et déplacer un peptide, même en l’absence de Mg2+. Cependant, sans Mg2+ le transporteur ne peut pas hydrolyser efficacement l’ATP, et ne peut donc pas se réinitialiser pour un nouveau cycle.
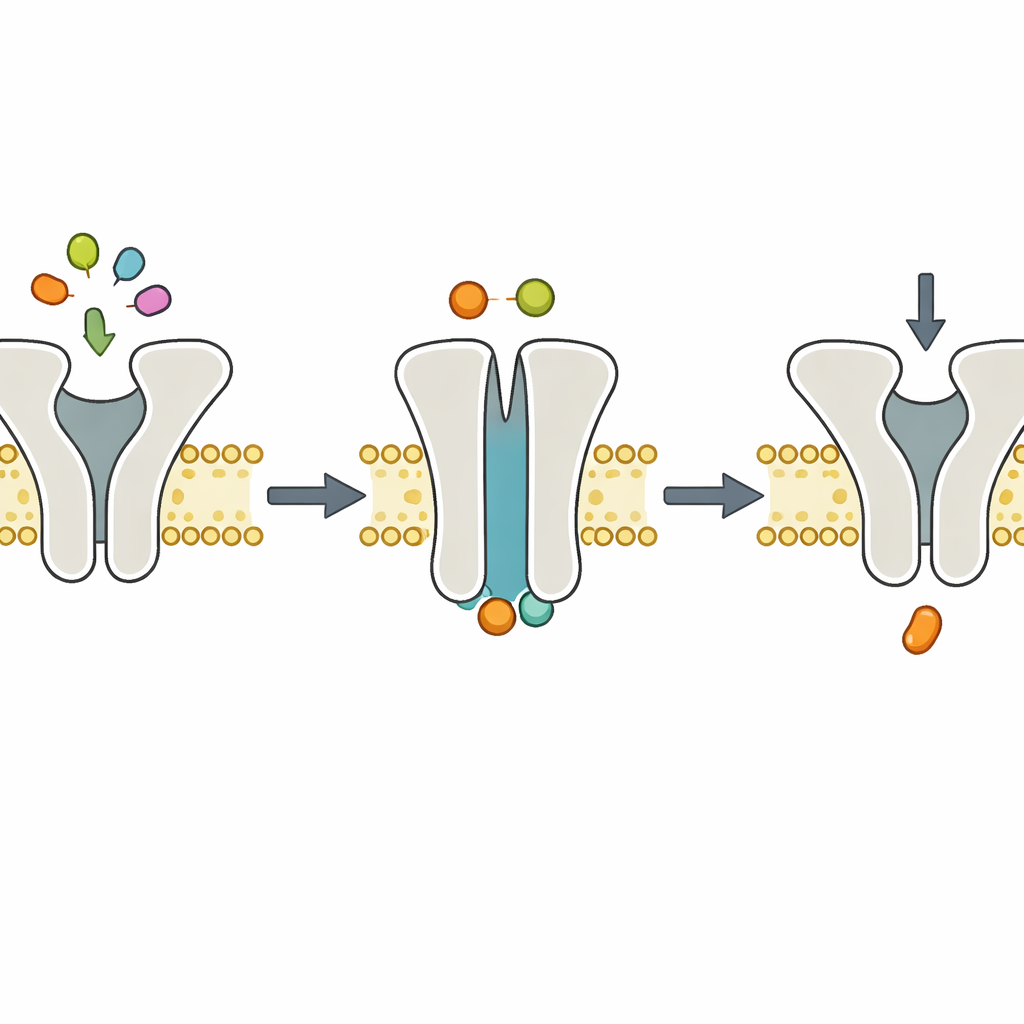
Des clichés structuraux étayent la dynamique
Pour voir à quoi ressemble la machine pendant cette étape sans Mg2+, l’équipe a eu recours à la cryo‑microscopie électronique, qui image des molécules vitrifiées à une résolution quasi atomique. Ils ont reconstitué TmrAB dans des nanodisques lipidiques, ajouté de l’ATP sans Mg2+ et congelé les complexes. Les structures obtenues montraient TmrAB dans une conformation tournée vers l’extérieur, « occluse », avec l’ATP coincé dans ses deux poches de liaison internes, mais sans Mg2+ visible. Ces clichés étaient essentiellement indiscernables des structures antérieures obtenues avec ATP et Mg2+ présents. Associées à des essais biochimiques montrant que l’hydrolyse de l’ATP s’interrompt complètement sans Mg2+, les images soutiennent une division du travail simple : la liaison de l’ATP entraîne le changement conformationnel qui déplace le peptide, tandis que l’hydrolyse de l’ATP dépendante du Mg2+ réalise l’étape de récupération.
Une image plus claire du fonctionnement des pompes cellulaires
En observant des transporteurs uniques et en résolvant leurs structures, ce travail tranche une question de longue date sur les transporteurs ABC : le coup mécanique qui déplace un peptide est déclenché par la liaison de l’ATP elle‑même, et non par la décomposition chimique ultérieure de l’ATP. Le Mg2+ intervient principalement pour permettre l’hydrolyse de l’ATP, ce qui réinitialise le transporteur afin qu’il puisse fonctionner à nouveau. Au‑delà d’éclaircir un aspect fondamental de la biologie cellulaire, cette approche monocellulaire offre une feuille de route pour disséquer d’autres machines membranaires qui sous‑tendent l’immunité, la résistance aux médicaments et de nombreuses maladies : une molécule et une étape de transport à la fois.
Citation: Nocker, C., Pečak, M., Nocker, T. et al. Single-molecule dynamics reveal ATP binding alone powers substrate translocation by an ABC transporter. Nat Commun 17, 3038 (2026). https://doi.org/10.1038/s41467-026-70021-1
Mots-clés: Transporteurs ABC, Liaison de l’ATP, FRET monocellulaire, Transport membranaire, TAP et TmrAB