Clear Sky Science · fr
Nanoparticules au bleu de Prusse ciblant la PANoptose médiée par le PANoptosome multiple pour le traitement des lésions d’ischémie-reperfusion myocardique
Pourquoi il est important de protéger le cœur en convalescence
Lorsqu’une personne fait une crise cardiaque, les médecins s’efforcent de rouvrir l’artère obstruée et de rétablir le flux sanguin. Cette étape qui sauve des vies comporte toutefois un coût caché : le retour soudain d’oxygène peut lui-même blesser le cœur, tuer des cellules et favoriser l’insuffisance cardiaque. Cette étude explore une nanomédecine inventive visant à protéger le cœur pendant cette fenêtre vulnérable en bloquant simultanément plusieurs voies de mort cellulaire interconnectées, ce qui pourrait permettre des récupérations plus douces après un infarctus.
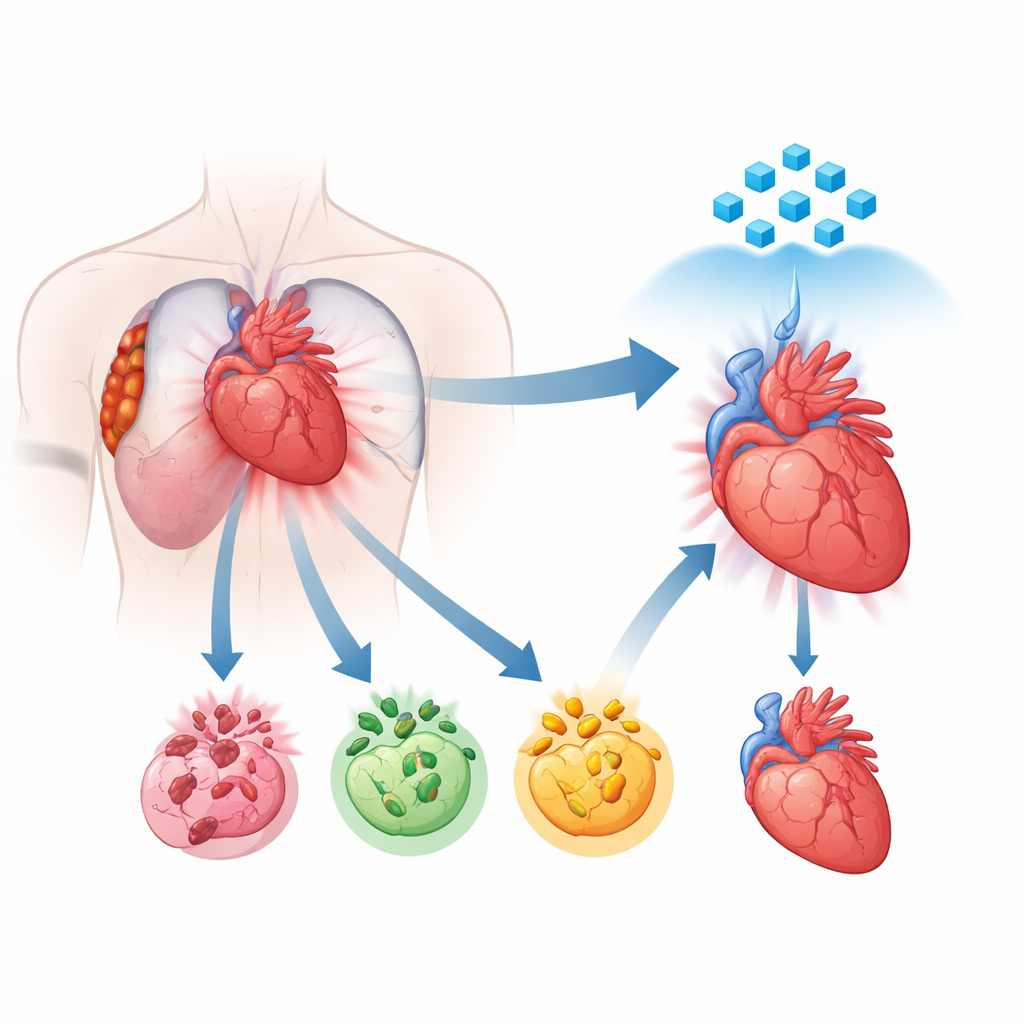
Une nouvelle vision de la mort des cellules cardiaques
Pendant des années, les chercheurs ont su que les cellules cardiaques endommagées peuvent mourir selon différentes voies programmées, notamment l’apoptose, la nécroptose et la pyroptose. Chacune suit son propre scénario moléculaire, mais des preuves croissantes montrent que ces voies n’opèrent pas isolément. Elles communiquent entre elles et peuvent fusionner en un processus combiné et incontrôlé appelé PANoptose. Dans cet état, plusieurs programmes de mort s’activent ensemble, rendant frustrantes les thérapies qui ne bloquent qu’une seule voie. Les auteurs ont utilisé le séquençage d’ARN de noyau isolé sur des tissus cardiaques humains de patients ayant récemment eu un infarctus pour cartographier où et dans quelle mesure ces programmes de mort sont activés. Ils ont constaté que, dans les régions les plus endommagées, les cellules musculaires cardiaques montraient une bascule puissante vers ce mode de mort combiné, désignant la PANoptose comme un moteur central des lésions.
Concevoir un petit outil multifonction pour le cœur blessé
Pour lutter contre un processus aussi complexe, l’équipe s’est tournée vers le bleu de Prusse, un composé médical anciennement approuvé surtout connu comme antidote à certains empoisonnements métalliques. À l’échelle nanométrique, les particules de bleu de Prusse se comportent comme de minuscules robots catalytiques capables d’éteindre des molécules nocives et d’influencer le comportement cellulaire. Par des simulations informatiques, les chercheurs ont montré que ces nanoparticules pouvaient se lier directement à trois points d’assemblage protéiques clés—RIPK1, ZBP1 et AIM2—qui contribuent à monter la machinerie moléculaire de la PANoptose. En se liant à ces points de contrôle de différentes manières, les particules devraient interférer avec la construction des complexes inducteurs de mort qui coordonnent les trois voies de mort cellulaire.
Diriger les nanoparticules directement vers le tissu cardiaque lésé
Les nanoparticules ne fonctionnent que si elles atteignent le bon endroit, aussi l’équipe a-t-elle enrobé les particules de bleu de Prusse d’enveloppes naturelles prélevées sur des plaquettes, les cellules sanguines qui se concentrent sur les vaisseaux endommagés. Ce revêtement a créé PB@PM, un vecteur biomimétique qui circule comme une plaquette mais délivre une charge thérapeutique. Chez des souris soumises à un infarctus contrôlé puis à la réouverture de l’artère, l’imagerie a montré que PB@PM s’accumulait beaucoup plus fortement dans la région cardiaque lésée que les particules non enrobées, tout en évitant en grande partie les organes sains. Fait important, les particules enrobées ont été bien tolérées : les analyses de sang et les examens tissulaires n’ont pas révélé de toxicité évidente, soutenant leur potentiel pour un développement ultérieur.
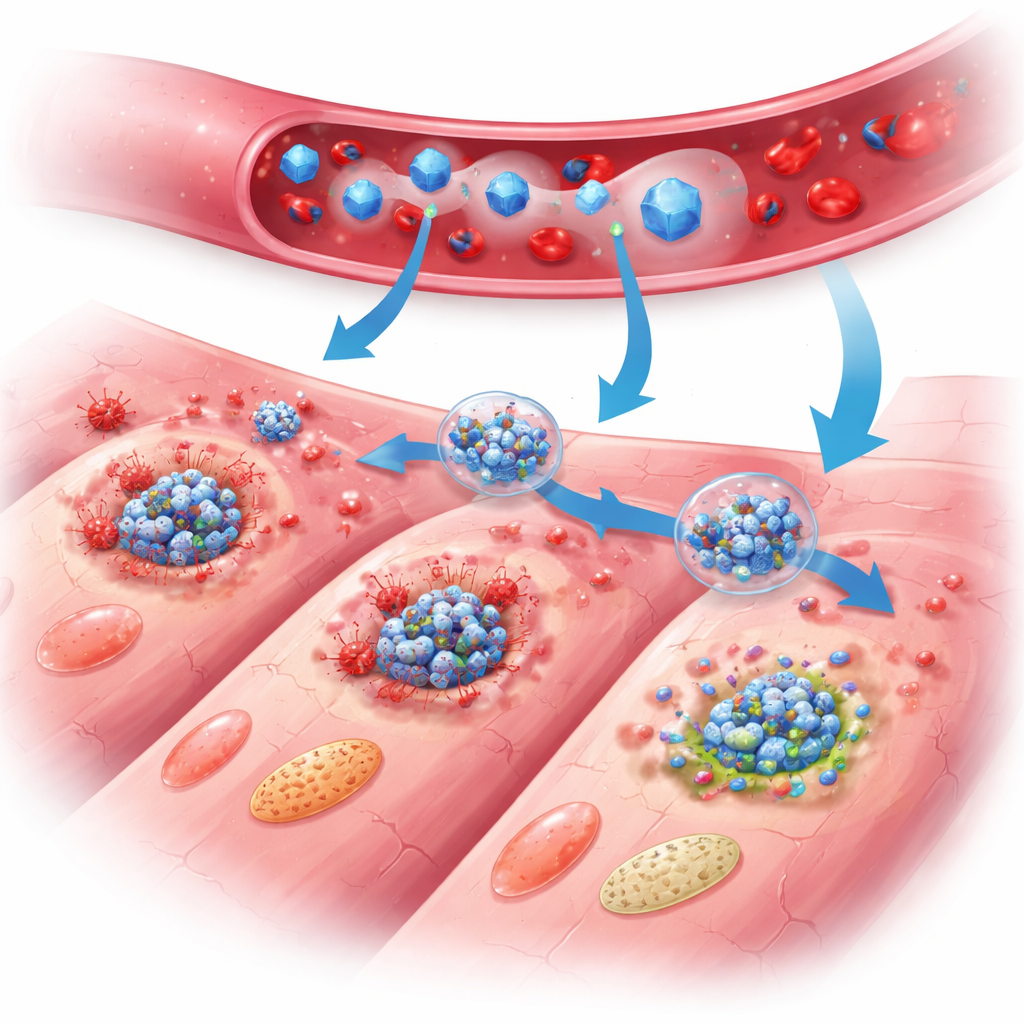
Comment le nano‑bouclier protège le cœur
Chez les souris traitées, les bénéfices de PB@PM se sont manifestés sur plusieurs jours et semaines. La fonction d’éjection cardiaque s’est améliorée, la taille de la cicatrice a diminué et la paroi cardiaque s’est amincie moins que chez les animaux non traités. Des études tissulaires détaillées ont révélé moins de cellules cardiaques mourantes, des cellules inflammatoires plus calmes et un tissu de réparation mieux structuré avec une croissance vasculaire plus saine et moins d’agrandissement anormal des cellules survivantes. Au niveau moléculaire, des profils d’expression génique étendus et des mesures protéiques ont montré que PB@PM a apaisé simultanément les trois principales voies de mort programmée, perturbé l’assemblage des complexes multi‑protéiques de la PANoptose et réduit les niveaux de molécules de signalisation qui alimentent l’inflammation. Les particules ont aussi neutralisé des espèces réactives de l’oxygène dommageables, stabilisé les mitochondries—les centrales énergétiques de la cellule—et rétabli un métabolisme énergétique plus normal, supprimant des déclencheurs clés qui pousseraient autrement les cellules vers l’autodestruction.
Ce que cela pourrait signifier pour les soins futurs des infarctus
En résumé, ce travail montre qu’une nanoparticule ingénieusement conçue peut agir comme un bouclier multi‑faces pour le cœur, atténuant un enchevêtrement de signaux de mort destructeurs plutôt que de courir après une voie à la fois. En ciblant le tissu cardiaque lésé, en se liant aux protéines de contrôle centrales et en réduisant le stress oxydatif et inflammatoire, PB@PM a nettement réduit la réaction en chaîne de perte cellulaire et de cicatrisation qui suit souvent la réouverture d’une artère obstruée. Bien que de nombreux tests restent à réaliser avant que cette stratégie puisse atteindre les patients, l’étude offre une preuve de concept que cibler la PANoptose dans son ensemble—et le faire avec des particules intelligentes d’inspiration biologique—pourrait ouvrir un nouveau chapitre dans la protection du cœur après un infarctus.
Citation: Xu, L., Jiang, L., Wu, R. et al. Prussian blue nanoparticles targeting multiple PANoptosome-mediated PANoptosis for myocardial ischemia-reperfusion injury therapy. Nat Commun 17, 2329 (2026). https://doi.org/10.1038/s41467-026-70012-2
Mots-clés: ischémie-reperfusion myocardique, thérapie par nanoparticules, mort cellulaire programmée, inflammation cardiaque, protection mitochondriale