Clear Sky Science · fr
La RPA stimule directement la processivité de l'hélicase Mer3 pour assurer la formation normale des croisements en méiose
Comment les cellules brassent l’ADN pour produire des ovules et des spermatozoïdes sains
Chaque fois qu'une plante, un animal ou un humain produit des ovules ou des spermatozoïdes, ses cellules doivent remélanger les chromosomes afin que chaque descendant reçoive un nouvel assortiment d'ADN parental. Ce remaniement génétique repose sur des échanges d'ADN précisément placés, ou croisements, entre paires de chromosomes. L'étude présentée dévoile comment deux protéines clés, Mer3 et RPA, coopèrent comme une machine microscopique pour garantir que ces croisements se forment de manière efficace et sûre — un processus aux implications pour la fertilité, l'évolution et peut‑être même le cancer.
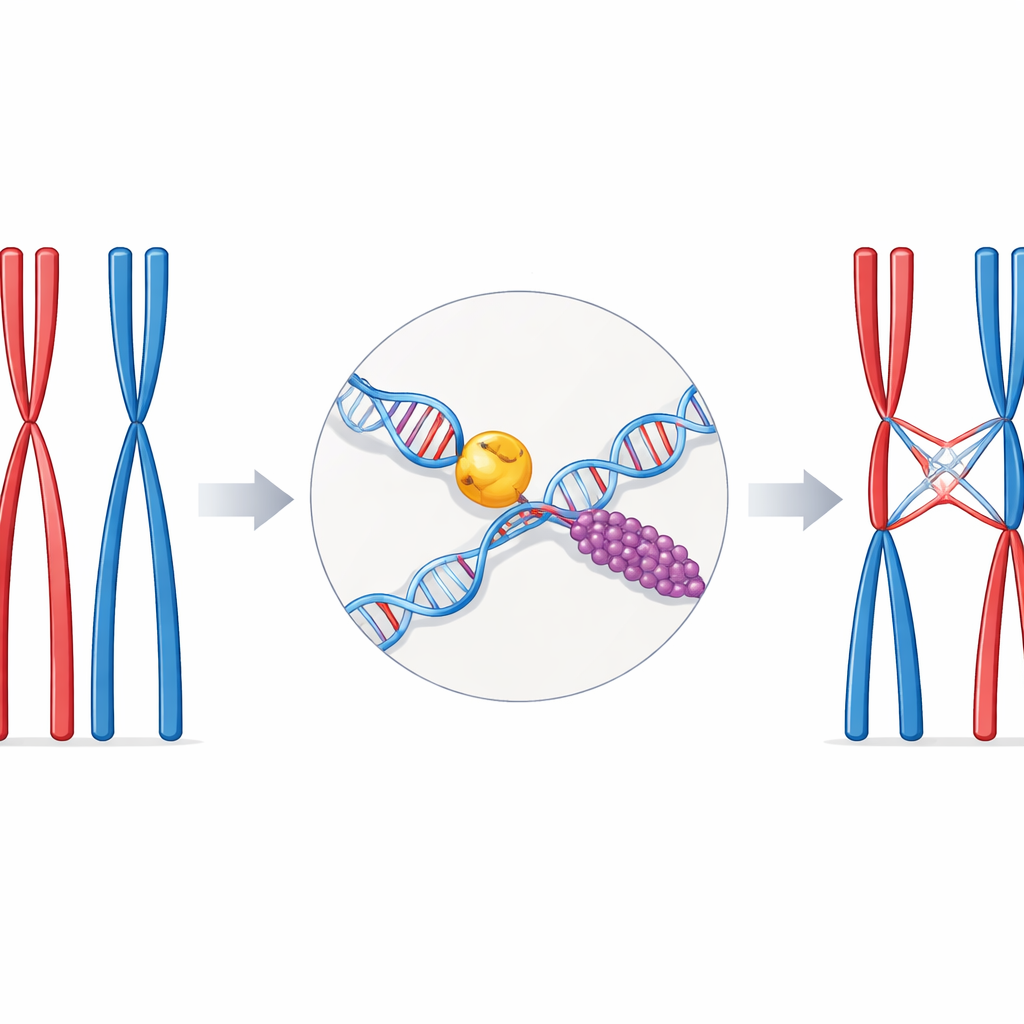
Un équilibre délicat dans la reproduction sexuée
Lors de la division cellulaire particulière appelée méiose, les chromosomes se présentent par paires correspondantes, l'une provenant de chaque parent. Pour que ces paires se séparent correctement, elles doivent être reliées physiquement en quelques points bien choisis le long de leur longueur. Ces liens sont les croisements — des segments où les brins d'ADN d'un chromosome sont échangés avec ceux de son partenaire. Avoir trop peu de croisements expose au mauvais partage des chromosomes et à l'infertilité ; en avoir trop ou en avoir de mal placés peut endommager le génome. Les cellules s'appuient donc sur des voies de réparation spécialisées et des protéines auxiliaires pour transformer une cassure d'ADN potentiellement dangereuse en un croisement correctement contrôlé.
Rencontrez Mer3 et RPA, une équipe de dérouleurs d'ADN
Les chercheurs se sont concentrés sur Mer3, un moteur moléculaire qui déroule l'ADN et favorise la formation des croisements. Son équivalent humain, HFM1, est connu pour son importance dans la fertilité. Ils ont découvert que Mer3 se lie directement à RPA, un complexe protéique qui enrobe normalement l'ADN simple brin exposé pour le protéger et recruter d'autres facteurs de réparation. Grâce à des tests biochimiques, de la modélisation structurale et des essais d'interaction, l'équipe a cartographié un site d'accrochage spécifique où une courte queue de Mer3 s'emboîte dans une rainure d'une sous‑unité de RPA. Cette interface est conservée de la levure aux mammifères, ce qui suggère qu'il s'agit d'une solution évolutive ancienne réutilisée pour contrôler la réparation de l'ADN pendant la méiose.
Observer un moteur d'ADN individuel en action
Pour voir ce que fait concrètement ce partenariat, les scientifiques ont utilisé des pinces magnétiques sur molécule unique — un instrument qui maintient une seule épingle d'ADN comme un petit ressort et mesure comment une seule molécule de Mer3 la déroule au fil du temps. Ils ont constaté que Mer3 se déplace le long de l'ADN à une vitesse constante même seul. Mais dans des conditions reproduisant la faible tension physique à l'intérieur des cellules, Mer3 a tendance à lâcher l'ADN après n'avoir déroulé qu'un court segment. Lorsqu'une petite quantité de RPA est présente, Mer3 devient soudain beaucoup plus persistant : il peut dérouler des segments d'ADN beaucoup plus longs sans se détacher, en particulier quand l'ADN a tendance à se replier sur lui‑même. Une version mutante de Mer3, conçue pour perturber la queue de liaison à RPA, ne gagne pas cette puissance de tenue supplémentaire, révélant que le contact direct avec RPA renforce la processivité de Mer3.
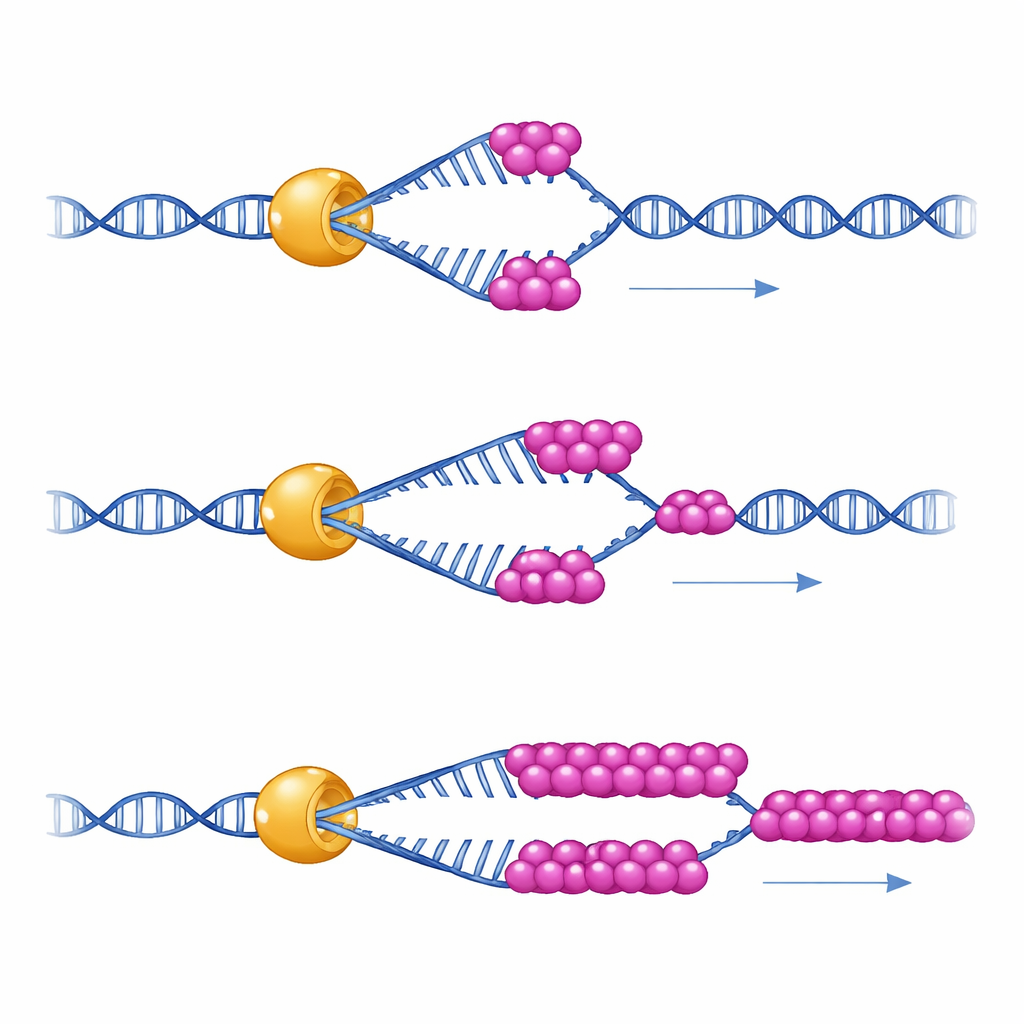
Conséquences pour les croisements dans les cellules vivantes
L'équipe s'est ensuite demandé ce qui se passe dans des cellules de levure réelles lorsque Mer3 ne peut plus bien s'accrocher à RPA. Ils ont remplacé le gène MER3 normal par le mutant incapable de lier RPA et ont suivi la méiose. Ces cellules pouvaient encore se diviser et former des spores, mais leur fertilité a diminué et le nombre global de croisements le long de certaines régions chromosomiques a chuté. Des analyses détaillées de l'ADN ont montré davantage d'événements de réparation se terminant en non‑croisements et une accumulation d'intermédiaires de recombinaison non résolus. Une cartographie à l'échelle du génome de la localisation de Mer3 a révélé que la protéine mutante était moins stabilisée sur les sites où surviennent les cassures programmées de l'ADN, même si son association précoce avec les axes chromosomiques paraissait normale. En d'autres termes, sans une liaison forte à RPA, Mer3 ne reste pas assez longtemps aux sites de cassure pour les orienter de façon fiable vers des issues de type croisement.
Ce que cela signifie pour la fertilité et la stabilité du génome
Pris ensemble, les résultats montrent que RPA fait plus que simplement enrober l'ADN libre ; il module directement le comportement d'une hélicase méiotique clé. En s'accrochant à RPA, Mer3 devient un dérouleur d'ADN plus déterminé, capable d'étendre et de stabiliser les structures d'ADN jointes qui mûrissent en croisements. Lorsque cette interaction est affaiblie, les cellules se tournent vers des issues de réparation plus sûres mais moins utiles et laissent davantage d'intermédiaires non résolus, compromettant subtilement la ségrégation chromosomique. Comme les mêmes acteurs moléculaires existent chez l'humain — et que des mutations de HFM1 sont associées à l'infertilité — ce travail fournit un cadre mécaniste expliquant comment de petits changements à une interface protéique peuvent se répercuter jusqu'à influencer la santé reproductive et la diversité génétique des générations futures.
Citation: Altmannova, V., Orlić, L., Carrasco, C. et al. RPA directly stimulates Mer3 helicase processivity to ensure normal crossover formation in meiosis. Nat Commun 17, 2621 (2026). https://doi.org/10.1038/s41467-026-69985-x
Mots-clés: méiose, recombinaison génétique, hélicase de l'ADN, fertilité, croisement chromosomique