Clear Sky Science · fr
Dérégulation de la réponse aux dommages de l’ADN par des oligonucléotides antisens phosphorothioates
Quand des thérapies géniques utiles induisent en erreur l’équipe de réparation de la cellule
Les oligonucléotides antisens, ou ASO, constituent une classe montante de médicaments de précision conçus pour activer ou désactiver des gènes individuels. Ils sont déjà utilisés pour traiter certaines maladies génétiques rares et sont testés pour de nombreuses autres pathologies. Cette étude révèle un effet indésirable inattendu d’une modification chimique courante utilisée pour rendre ces médicaments plus stables : dans certaines conditions, elle peut faire croire à la cellule que son ADN est endommagé, bloquant la machinerie de réparation et mettant en péril à long terme l’intégrité du génome.
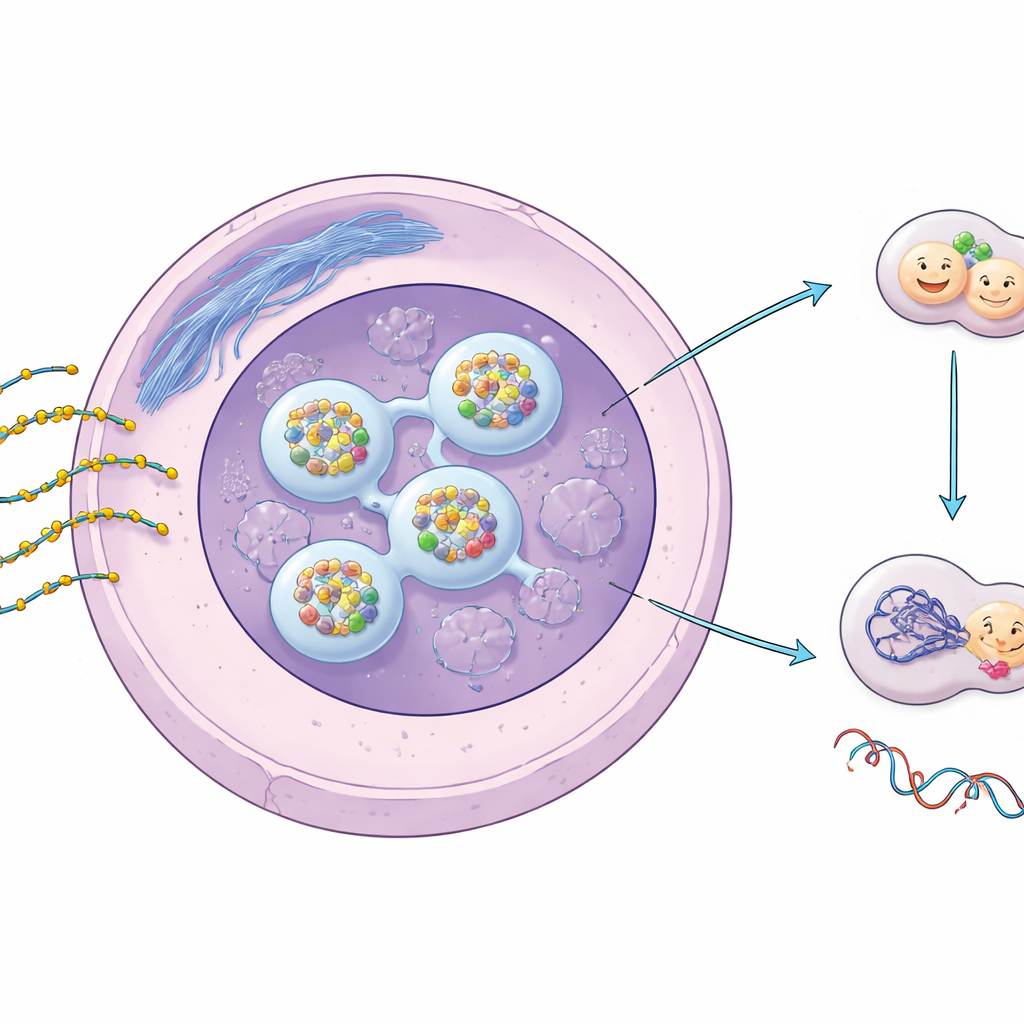
Interrupteurs géniques conçus et leur amélioration chimique
Les ASO sont de courts brins simples de matériel génétique conçus pour reconnaître et se lier à des messages ARN spécifiques à l’intérieur de nos cellules, les silenceant ou les modifiant. Pour survivre dans l’organisme et pénétrer efficacement dans les cellules, la plupart des ASO thérapeutiques portent une modification phosphorothioate (PS), dans laquelle un atome de soufre remplace un atome d’oxygène dans l’épine dorsale du brin. Ce petit changement augmente considérablement leur stabilité et leur propension à interagir avec des protéines. Des travaux antérieurs ont montré que les PS‑ASO s’accumulent en points distincts dans le noyau et peuvent perturber certaines structures nucléaires, mais ce que cela implique pour la réparation de l’ADN et la sécurité à long terme restait incertain.
Gouttelettes artificielles qui imitent de vrais sites de réparation de l’ADN
Les auteurs ont suivi des PS‑ASO marqués par fluorescence dans des cellules humaines et ont constaté qu’à des doses expérimentales couramment utilisées, ils s’accumulent rapidement dans le noyau et nucléent de nouvelles structures sphériques appelées corps PS. Ces corps se forment de manière dépendante de la concentration et se comportent comme des gouttelettes liquides qui fusionnent, se dissolvent et dépendent de forces moléculaires faibles — caractéristiques de la séparation de phase liquide–liquide. Crucialement, elles ne se situent pas aux endroits où surviennent réellement des cassures d’ADN et ne contiennent pas les marqueurs habituels d’ADN brisé. Au lieu de cela, l’étude montre que des enzymes clés de réparation de l’ADN — notamment DNA‑PKcs, ATM, ATR et PARP1 — se lient directement aux PS‑ASO et s’enrichissent fortement à l’intérieur de ces gouttelettes artificielles, alors même que l’ADN sous‑jacent est intact.
Faux positifs qui activent les signaux de dommage de la cellule
Une fois assemblées, les gouttelettes nucléées par les ASO font plus que piéger passivement des protéines : elles activent les enzymes de réparation. En moins d’une heure après l’entrée des ASO, les enzymes présentes dans ces gouttelettes sont activées et commencent à modifier la chromatine voisine, marquant les histones par des modifications chimiques normalement observées après un véritable dommage à l’ADN. Cela déclenche la réponse complète aux dommages de l’ADN — recrutement de facteurs de réparation supplémentaires, activation de la signalisation des points de contrôle et réduction de l’activité des moteurs du cycle cellulaire appelés CDK. En conséquence, les cellules ralentissent ou arrêtent leur progression dans des phases clés du cycle cellulaire, en particulier au point où elles vérifient normalement l’intégrité de l’ADN avant de se diviser. Chez la souris, après une administration d’ASO cliniquement pertinente, les chercheurs ont également observé une augmentation de la signalisation de dommage de l’ADN dans les régions présentant une uptake d’ASO plus élevée, indiquant que ces effets ne se limitent pas aux cultures cellulaires.
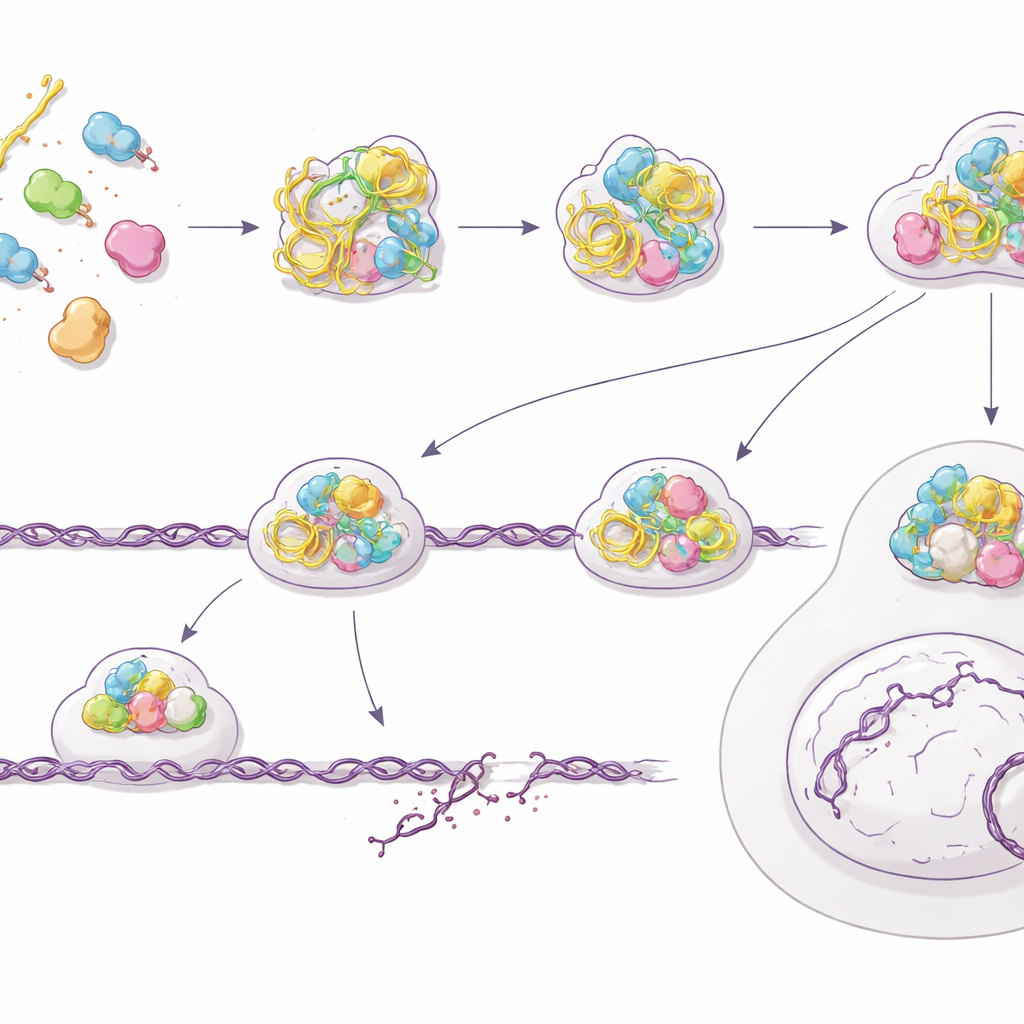
Réparation défaillante et accumulation croissante de cassures d’ADN
Paradoxalement, alors que le système d’alarme de la cellule retentit, sa capacité réelle à réparer des cassures dangereuses de l’ADN se dégrade. L’équipe a montré que des cellules pré‑traitées avec des PS‑ASO peinent à réparer les dommages après irradiation et accumulent même davantage de cassures spontanées, mesurées par des essais en comète et des foyers de réparation persistants. Un examen plus approfondi d’une des voies de réparation les plus précises de la cellule — la recombinaison homologue — a révélé le problème : des acteurs clés tels que BRCA2 et RAD51 ne s’assemblent pas correctement aux extrémités d’ADN rompues, tandis que des marqueurs précoces de traitement de ces extrémités apparaissent encore. En utilisant un système rapporteur génétique, les auteurs ont quantifié une chute d’environ 60 % de l’efficacité de la recombinaison homologue après exposition aux PS‑ASO. Les cellules deviennent globalement moins viables et nettement plus sensibles aux radiations, cohérent avec un système de réparation qui est signalé mais mal déployé.
Conséquences pour l’avenir des médicaments ciblant les gènes
Dans l’ensemble, l’étude suggère que les ASO modifiés par PS peuvent nucléer des gouttelettes liquides artificielles dans le noyau qui concentrent et activent des enzymes de réparation de l’ADN même en l’absence de dommages à réparer. Cette fausse alarme chronique perturbe les choix normaux de réparation, en particulier la recombinaison homologue précise, entraînant des lésions d’ADN persistantes, l’activation des points de contrôle et la mort cellulaire. Bien que les effets les plus marqués soient observés à des niveaux nucléaires élevés d’ASO typiques des expériences de transfection, une activation subtile de la signalisation de dommage est détectable même à des doses plus faibles, proches de celles utilisées en thérapeutique. Pour les patients et les développeurs de médicaments, le message est clair : les caractéristiques chimiques qui rendent les ASO efficaces comme médicaments peuvent, dans certains contextes, interférer avec la protection la plus fondamentale de la cellule — sa capacité à maintenir un génome stable — soulignant la nécessité de concevoir des architectures de brin plus sûres et de surveiller les voies de réparation de l’ADN pendant la thérapie.
Citation: Hjelmgren, L., Zhou, Q., Schmidli, S. et al. Dysregulation of the DNA damage response by phosphorothioate antisense oligonucleotides. Nat Commun 17, 2111 (2026). https://doi.org/10.1038/s41467-026-69980-2
Mots-clés: oligonucléotides antisens, réponse aux dommages de l’ADN, séparation de phase liquide, réparation homologue, stabilité du génome