Clear Sky Science · fr
Des mimétiques chiraux du peptidoglycane ciblent la biosynthèse de la paroi bactérienne pour intervenir contre les pathogènes
Une nouvelle manière de traquer les germes dangereux
Les infections résistantes aux antibiotiques augmentent dans le monde, et les médecins manquent encore d’outils capables de repérer et d’attaquer précisément les bactéries dangereuses sans nuire à nos propres cellules. Cette étude présente un « leurre » moléculaire astucieux qui imite un élément constitutif clé de la paroi bactérienne. Ces molécules conçues peuvent à la fois révéler les infections pour l’imagerie et transporter des antibiotiques directement vers les microbes, offrant une stratégie nouvelle pour lutter contre les agents pathogènes difficiles à traiter.
Imiter l’armure bactérienne
Les bactéries sont enveloppées d’un maillage solide appelé paroi cellulaire, construit à partir de sucres et d’acides aminés inhabituels en miroir que nos propres cellules n’utilisent guère. Les chercheurs ont tiré parti de cette différence en créant de longues chaînes à base de sucres décorées d’une forme miroir spécifique d’alanine, un acide aminé courant. Ces chaînes, appelées mimétiques chiral du peptidoglycane, sont conçues pour ressembler étroitement aux ingrédients naturels que les bactéries utilisent pour bâtir leurs parois, mais sont absentes des tissus mammifères. En ajustant finement la quantité d’alanine de configuration D attachée, l’équipe a produit des versions qui favorisent nettement les bactéries plutôt que les cellules humaines.
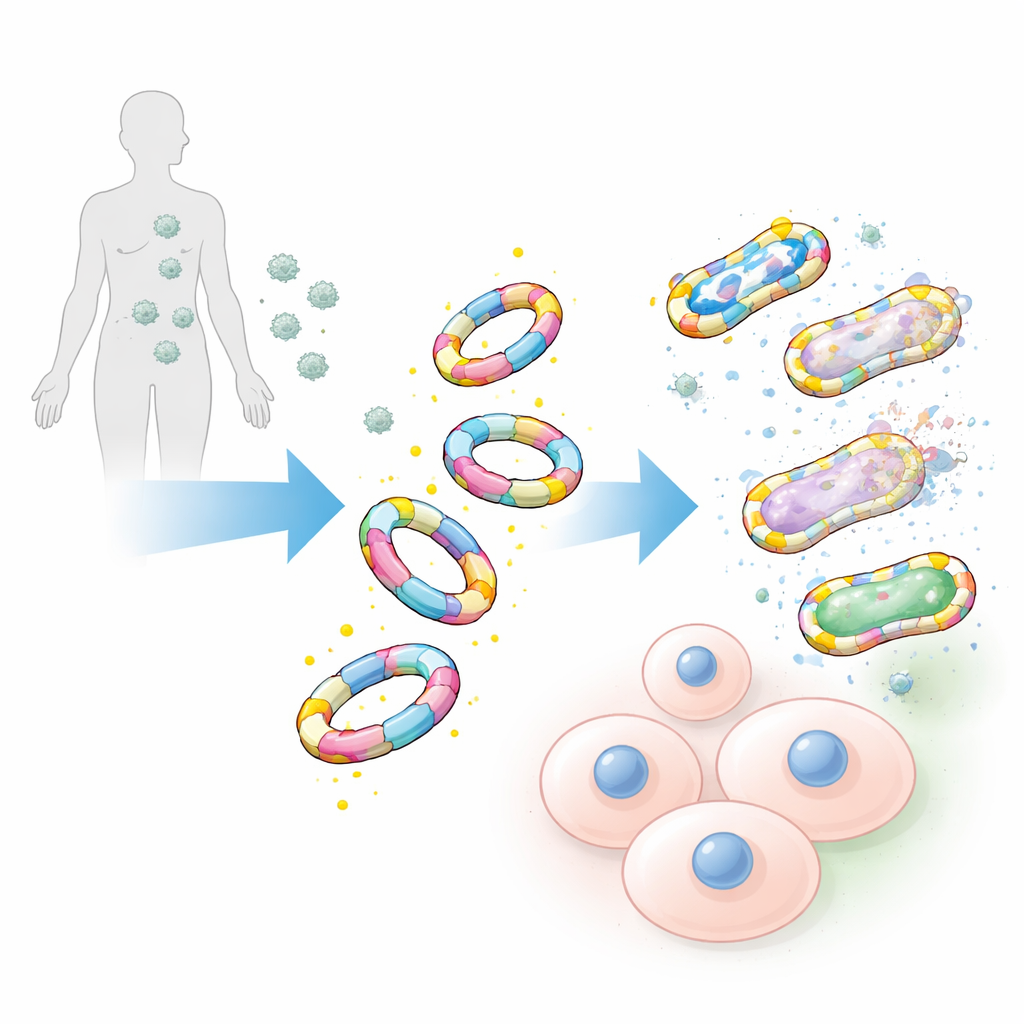
S’ancrer sur les bactéries, pas sur nos cellules
Testés contre un large éventail de pathogènes, y compris des souches hospitalières notoires comme Staphylococcus aureus résistant à la méthicilline et d’autres bactéries du groupe ESKAPE, les mimétiques décorés d’alanine D se sont liés aux surfaces bactériennes avec une efficacité remarquable. Leurs homologues en miroir constitués de l’alanine sous forme L, ainsi que les seules chaînes de sucre d’origine, n’ont montré qu’une fixation faible ou négligeable. L’équipe a également comparé ces grands mimétiques à des sondes chimiques traditionnelles plus petites basées sur des molécules uniques d’alanine D. Même lorsque les petites sondes étaient rendues extrêmement lumineuses, elles marquaient encore bien moins de bactéries et donnaient des signaux plus faibles, ce qui souligne la puissance du design plus volumineux et plus réaliste.
Détourner la chaîne d’assemblage de la paroi
Pour comprendre pourquoi la reconnaissance est si forte, les scientifiques ont examiné comment les mimétiques interagissent avec la machinerie de construction de la paroi bactérienne. Ils ont constaté que les chaînes à base d’alanine D ne se contentent pas d’adhérer à l’extérieur ; elles sont assimilées comme si elles étaient de véritables éléments de construction et intégrées aux mêmes étapes enzymatiques qui joignent normalement les composants de la paroi. L’analyse chimique a détecté de nouveaux intermédiaires qui n’apparaissent que lorsque ces mimétiques sont présents, et des simulations informatiques ont montré que des enzymes clés de construction de la paroi saisissent les mimétiques encore plus fermement que les substrats naturels. Au fil de plusieurs cycles de croissance bactérienne, les mimétiques s’accumulent dans la paroi, en déformant progressivement sa structure et en la rendant perméable.
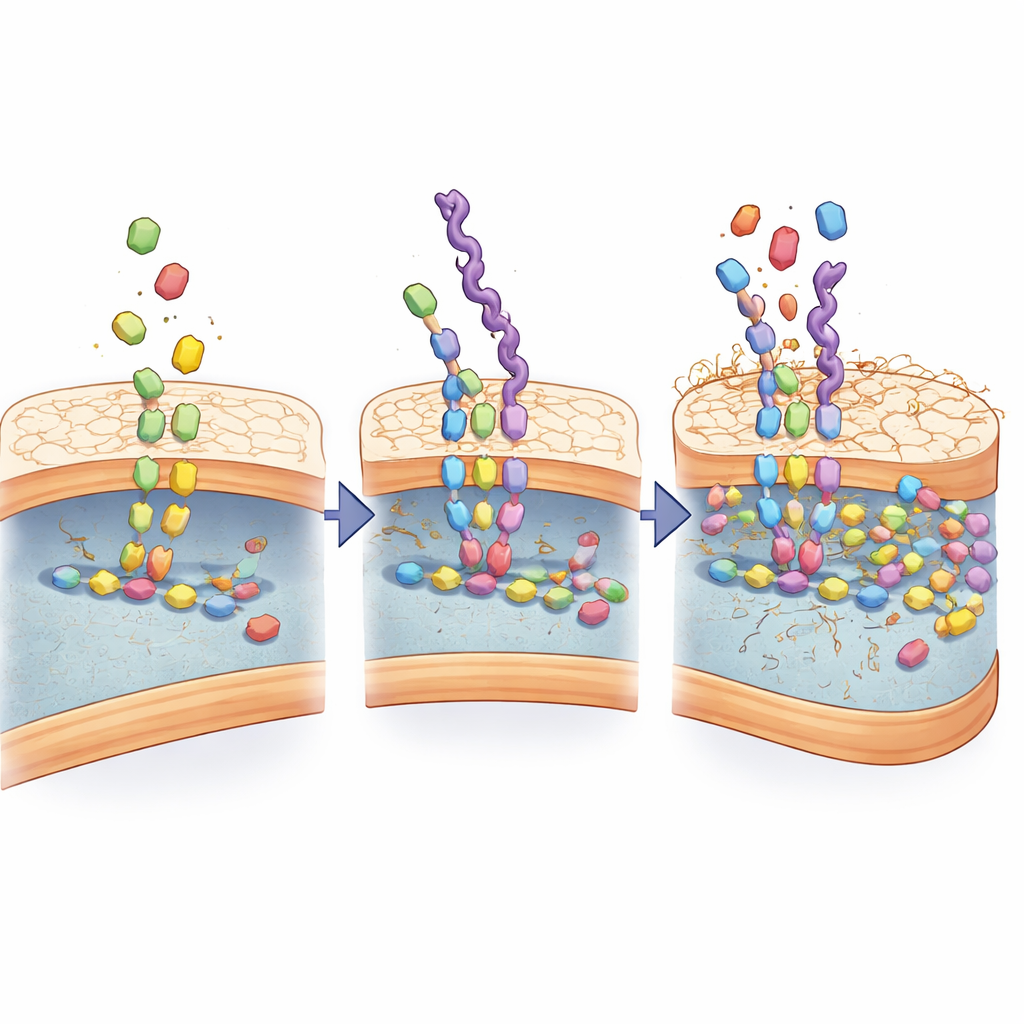
Transformer les mimétiques en vecteurs intelligents de médicaments
Parce que ces chaînes s’assemblent naturellement en petites particules en milieu aqueux et portent de nombreux points d’accrochage chimiques, l’équipe les a utilisées comme échafaudages pour des colorants d’imagerie et des antibiotiques. Des versions fluorescentes ont clairement délimité les bactéries en cultures cellulaires, tout en interagissant à peine avec des cellules mammifères cultivées à proximité. Les chercheurs ont ensuite chargé l’antibiotique tétracycline dans les particules à base de mimétiques. Dans des tests en laboratoire, cet emballage a rendu la tétracycline plusieurs fois plus efficace, tuant même des souches résistantes à des doses beaucoup plus faibles que le médicament libre. La microscopie a révélé que les mimétiques chargés d’antibiotique s’aggloméraient sur les bactéries, pénétraient leurs enveloppes et provoquaient une mortalité cellulaire étendue par rapport aux formulations non ciblées.
Combattre les infections dans l’organisme
Les essais les plus exigeants ont été réalisés sur des modèles murins d’abcès cutanés localisés et d’infections abdominales potentiellement mortelles. Dans les plaies infectées, les mimétiques fluorescents ont ciblé des bactéries profondément situées dans les tissus et, lorsqu’ils transportaient de la tétracycline, ont presque complètement éradiqué les microbes. Cela a entraîné une cicatrisation plus rapide, une peau neuve plus épaisse, un dépôt de collagène plus ordonné et une angiogenèse accrue. Dans les modèles d’infection systémique, les mimétiques se sont accumulés spécifiquement dans des organes infectés tels que la rate et les poumons, où ils ont fortement réduit les charges bactériennes lorsqu’ils étaient chargés d’antibiotique. Fait important, des doses élevées de mimétiques seuls ont montré une bonne tolérance, sans atteinte évidente des principaux organes ni perturbation de la biochimie sanguine.
Ce que cela pourrait signifier pour les traitements futurs
En construisant un proche analogue chimique des propres ingrédients de la paroi bactérienne, ce travail démontre une nouvelle manière de « se fondre » dans le métabolisme d’un pathogène au lieu de simplement l’attaquer depuis l’extérieur. Ces mimétiques chiraux servent à la fois de balises de haute précision pour l’imagerie et de véhicules intelligents qui dirigent les antibiotiques directement vers leurs cibles microbiennes, y compris les souches résistantes, tout en épargnant les cellules mammifères. S’ils sont traduits en outils cliniques, de telles plates-formes biomimétiques pourraient aider les médecins à voir exactement où les infections se cachent et à les traiter plus efficacement avec des doses de médicament plus faibles, offrant une arme prometteuse contre le défi croissant de la résistance aux antimicrobiens.
Citation: Deng, K., Zou, D., Zeng, Z. et al. Chiral peptidoglycan mimics target bacterial wall biosynthesis for pathogen intervention. Nat Commun 17, 3258 (2026). https://doi.org/10.1038/s41467-026-69967-z
Mots-clés: résistance aux antibiotiques, paroi cellulaire bactérienne, libération ciblée de médicaments, imagerie moléculaire, nanomédecine