Clear Sky Science · fr
Disséction multimodale de la pathologie TDP-43 spécifique aux types cellulaires dans le cortex moteur
Pourquoi cette recherche compte pour les personnes
La sclérose latérale amyotrophique (SLA) et la démence frontotemporale (DFT) sont des maladies cérébrales dévastatrices qui privent les personnes de mobilité, de la parole et de leur personnalité. La majorité des patients atteints de SLA et beaucoup de ceux atteints de DFT partagent un signe microscopique commun : des agrégats d’une protéine appelée TDP-43 s’accumulent là où ils n’ont pas leur place. Cette étude pose deux questions pratiques aux grandes implications pour les traitements futurs : quels types de cellules cérébrales sont précisément les plus touchés par les anomalies de TDP-43, et que dysfonctionne-t-il à l’intérieur de ces cellules au niveau de la régulation de l’ADN et de l’activité génique ?
Suivre les dégâts jusqu’au centre moteur du cerveau
Les chercheurs se sont concentrés sur le cortex moteur primaire, la bande de tissu cérébral qui contrôle le mouvement volontaire. En utilisant des échantillons cérébraux post-mortem donnés par des personnes atteintes de SLA, de SLA-DFT et par des témoins neurologiquement sains, ils ont isolé des noyaux cellulaires individuels et ont mesuré à la fois quels gènes étaient actifs et à quel point l’ADN local était compacté. Cette approche « multi-omique », appliquée à plus de 180 000 noyaux, leur a permis de trier les cellules en types précis : plusieurs classes de neurones excitateurs et inhibiteurs, ainsi que des cellules de soutien telles que les astrocytes, oligodendrocytes et microglies. Ils ont ensuite combiné ces données avec des cartes spatiales d’expression génique provenant d’un autre jeu de données humain pour replacer ces types cellulaires dans la structure stratifiée familière du cortex.
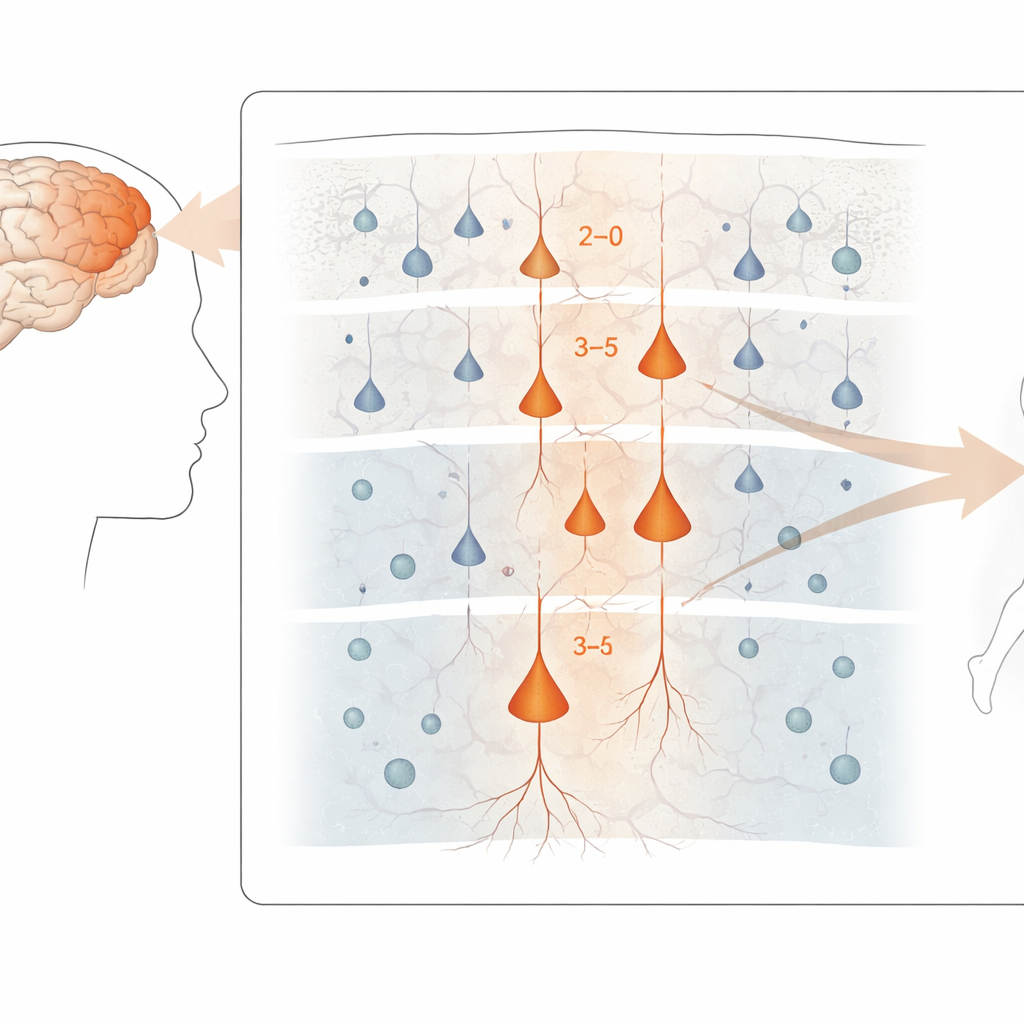
Identifier les neurones les plus vulnérables
Dans tout le cortex moteur, les changements d’expression génique liés à la maladie étaient les plus marqués dans les neurones excitateurs, les cellules qui propagent l’activité le long des circuits cérébraux. En particulier, les neurones des couches supérieures et moyennes qui se connectent à l’intérieur du cortex, ainsi que certains neurones des couches profondes qui envoient des signaux hors du cortex — y compris les grandes cellules « de Betz » qui contrôlent les motoneurones spinaux — ont montré les altérations les plus prononcées. En revanche, les interneurones inhibiteurs et de nombreuses cellules gliales étaient moins affectés au niveau de l’expression génique, bien que certaines présentent des changements plus subtils. Malgré ce tumulte moléculaire, la composition globale des principaux types cellulaires dans le tissu était étonnamment similaire entre patients et témoins, ce qui suggère que le problème tient davantage au fonctionnement des cellules qu’à une simple perte numérique.
Comment TDP-43 remodelle l’activité génique de l’intérieur
Pour distinguer les effets directement causés par TDP-43 d’autres processus pathologiques, l’équipe a utilisé une stratégie astucieuse de tri. Ils ont marqué les noyaux avec des anticorps contre TDP-43 et un marqueur neuronal, puis ont employé la cytométrie en flux pour séparer les neurones dont les noyaux avaient perdu TDP-43 (signe de pathologie) de ceux qui le conservaient. Le séquençage de plus de 12 000 de ces noyaux a révélé que la perte de TDP-43 survient massivement dans les neurones excitateurs, en particulier dans des sous-types spécifiques des couches 2–3, 3–5, 5 et 6. Dans ces neurones vulnérables, des centaines de gènes étaient déréglés, y compris de nombreux gènes déjà associés à la SLA. Des signatures moléculaires classiques du dysfonctionnement de TDP-43 — comme l’apparition de segments « cryptiques » supplémentaires dans les transcrits des gènes STMN2 et KALRN, et des changements dans les sites de clivage et de polyadénylation des ARN — étaient clairement enrichies dans les noyaux déficients en TDP-43.
Remodelage épigénétique : tous les changements ne proviennent pas de TDP-43
Parce qu’ils ont mesuré à la fois l’activité génique et l’ouverture de la chromatine dans les mêmes noyaux, les auteurs ont pu déterminer quels changements s’associaient à des modifications de l’emballage de l’ADN. Ils ont trouvé des dizaines de milliers de sites dans le génome où l’accessibilité locale de la chromatine suivait l’expression génique. Nombre des gènes altérés dans la SLA et la SLA-DFT se trouvaient dans de telles régions, indiquant qu’une part du profil de la maladie reflète un remodelage épigénétique plus large plutôt que des conséquences directes de la perte de TDP-43. Fait intéressant, ces changements liés à la chromatine convergaient souvent vers des voies de signalisation impliquées dans la communication cellulaire et le guidage axonal, et ils étaient particulièrement marqués dans certains neurones excitateurs et dans les oligodendrocytes. Lorsque l’équipe a comparé les altérations géniques liées à la pathologie TDP-43 avec celles liées aux changements de chromatine, elles se sont révélées partiellement superposées mais pour l’essentiel constituant des couches distinctes de perturbation.
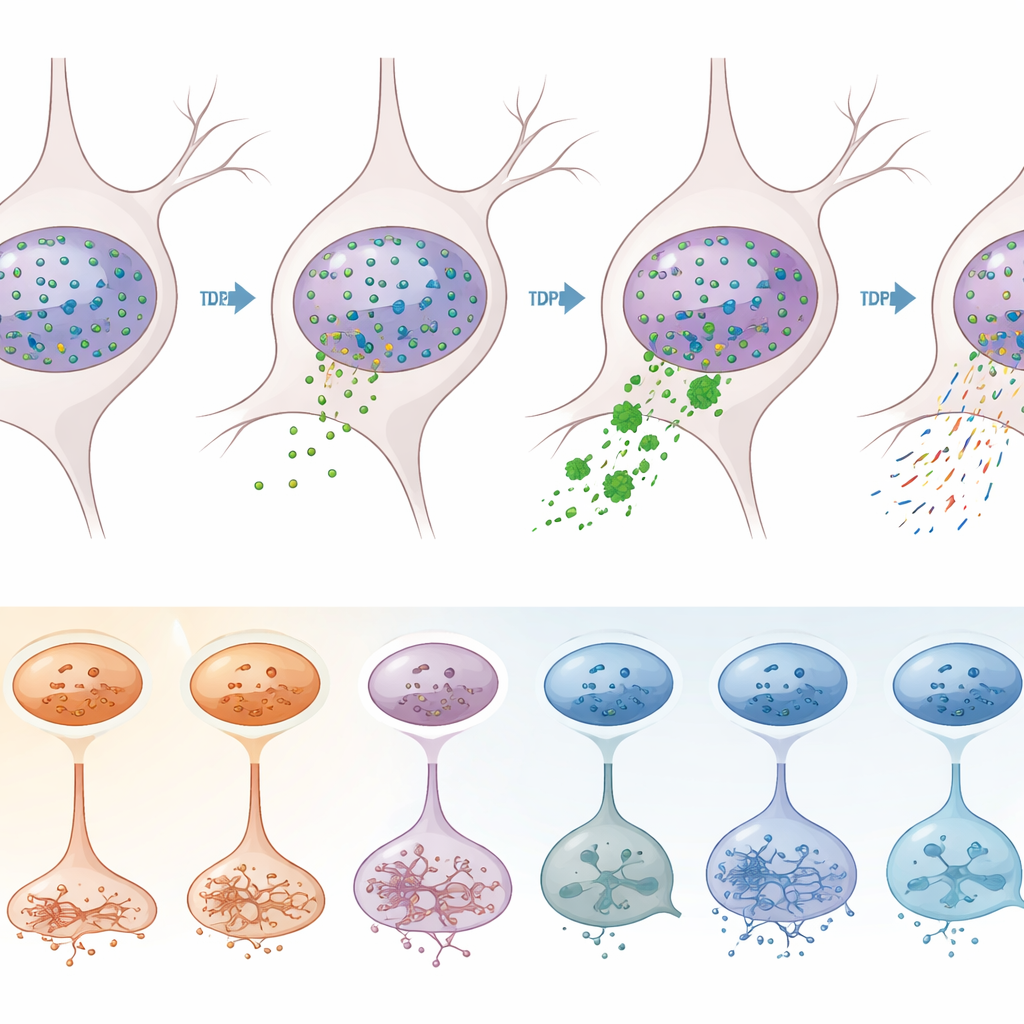
Ce que cela implique pour les thérapies futures
Pour un lecteur non spécialiste, le message clé est que la SLA et la SLA-DFT n’endommagent pas le cortex moteur de manière uniforme. Elles frappent plutôt des types précis de neurones excitateurs et, dans une moindre mesure, certains types de cellules de soutien, en altérant leurs programmes géniques d’une manière qui dépend à la fois du mauvais comportement de TDP-43 et de changements plus larges dans la façon dont l’ADN est empaqueté et lu. Ces résultats suggèrent que des traitements efficaces pourraient devoir être à la fois spécifiques aux types cellulaires et aux voies : par exemple, restaurer la fonction de TDP-43 ou corriger ses erreurs d’épissage dans les neurones les plus vulnérables, tout en ciblant séparément les changements épigénétiques et de signalisation partagés par plusieurs types cellulaires. En cartographiant ce paysage complexe avec un haut degré de résolution, l’étude fournit une feuille de route pour concevoir des interventions plus précises visant à ralentir ou prévenir la perte du contrôle moteur dans la SLA et la SLA-DFT.
Citation: Ruf, W.P., Kühlwein, J.K., Meier, L. et al. Multi-modal dissection of cell-type specific TDP-43 pathology in the motor cortex. Nat Commun 17, 2406 (2026). https://doi.org/10.1038/s41467-026-69944-6
Mots-clés: SLA, démence frontotemporale, TDP-43, neurones du cortex moteur, multiomique sur noyaux uniques