Clear Sky Science · fr
Les cellules Th17 nécessitent le capteur de réparation de l’ADN xeroderma pigmentosum groupe C pour contrôler les dommages oxydatifs de l’ADN dans un modèle murin
Les gardiens de nos défenseurs immunitaires
Les cellules T auxiliaires de type 17, ou cellules Th17, sont un type particulier de globules blancs qui patrouillent aux niveaux des barrières de notre corps, comme l’intestin et la peau, pour repousser bactéries et champignons. Mais elles participent aussi aux maladies auto-immunes lorsque leurs réponses déraillent. Cette étude pose une question apparemment simple : comment ces cellules très actives protègent-elles leur propre ADN du stress chimique qu’elles génèrent en combattant les infections ? La réponse tourne autour d’un détecteur de dommages de l’ADN appelé XPC, surtout connu pour protéger les cellules de la peau contre la lumière solaire. Ici, les chercheurs montrent que XPC est aussi crucial pour maintenir les cellules Th17 en bonne santé, énergiques et efficaces.
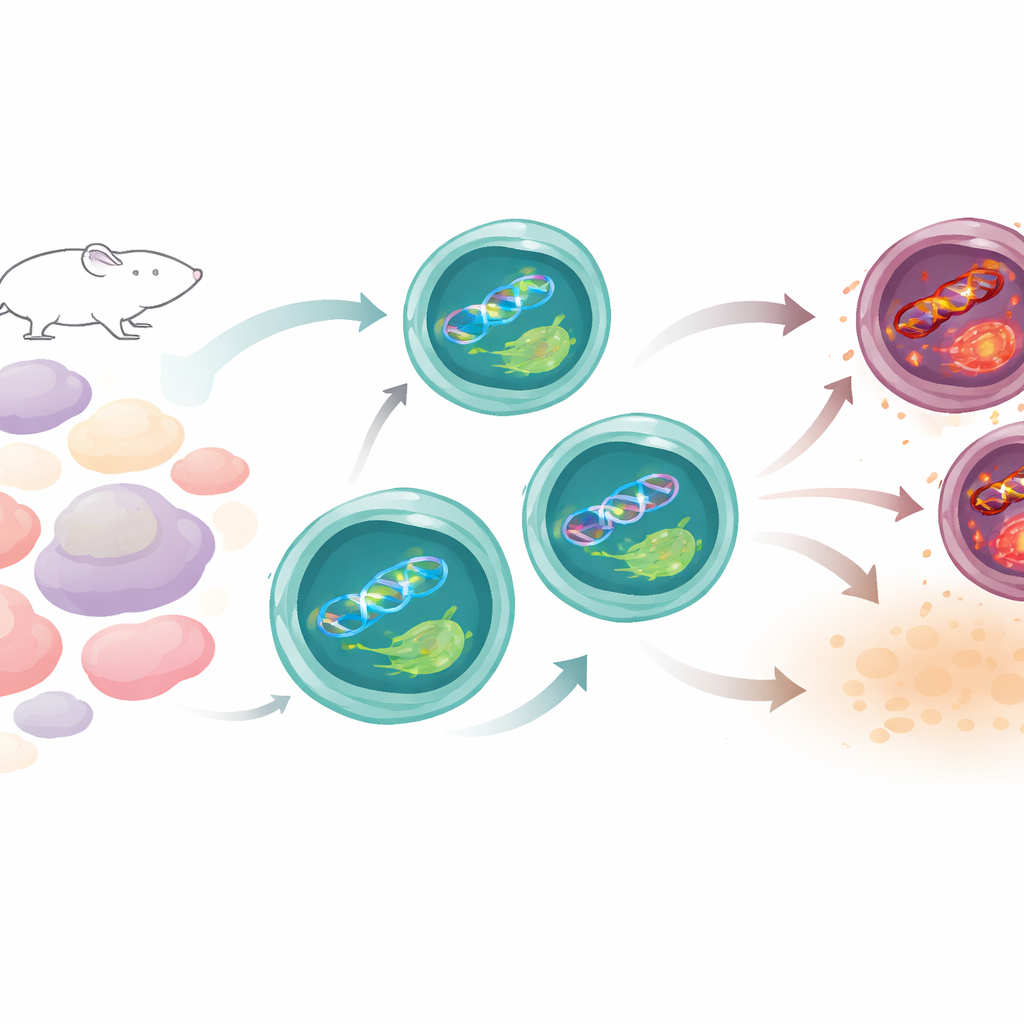
Comment les cellules Th17 maintiennent normalement l’équilibre
La vie des cellules Th17 est périlleuse. Pour fonctionner, elles accélèrent leur métabolisme et produisent des espèces réactives de l’oxygène — des molécules chimiquement réactives qui peuvent endommager l’ADN. L’équipe a comparé les cellules Th17 à d’autres types de cellules T chez la souris et a constaté que, malgré leur activité intense, les Th17 accumulent moins de dommages à l’ADN que nombre de leurs parentes. Un indice clé était que les gènes impliqués dans la réparation de l’ADN, en particulier ceux d’une voie qui répare habituellement les lésions induites par le soleil, étaient plus fortement exprimés dans les Th17. Parmi eux figurait XPC, une protéine qui scrute l’ADN à la recherche de dommages structuraux. Au fur et à mesure de la maturation des Th17, les niveaux de XPC augmentaient et se localisaient sur les sites endommagés du noyau, ce qui suggère qu’elle était en permanence en patrouille pour préserver l’intégrité génétique.
Que se passe-t-il lorsque le capteur d’ADN manque
Pour mesurer l’importance réelle de XPC, les chercheurs ont utilisé des souris modifiées pour être dépourvues de cette protéine. À première vue, leur système immunitaire paraissait globalement normal : les effectifs totaux de cellules T et de nombreuses sous-populations étaient inchangés. Mais en se focalisant sur les cellules Th17, un défaut frappant est apparu. En l’absence de XPC, beaucoup moins de cellules produisaient la molécule caractéristique des Th17, IL-17, et des marqueurs d’identité et des commutateurs de signalisation essentiels au programme Th17 étaient diminués. In vitro, les cellules T naïves issues de ces souris avaient du mal à devenir de véritables Th17. Dans un modèle standard où des cellules T transférées déclenchent une inflammation intestinale, les cellules T déficientes en XPC n’ont pas induit de colite, traduisant une capacité inflammatoire réduite. Parallèlement, les cellules T régulatrices, qui tempèrent les réponses immunitaires, sont devenues plus abondantes, ce qui suggère un déplacement de l’équilibre entre agressivité et régulation.
Domages de l’ADN, centrales énergétiques et stress chimique
En creusant davantage, l’équipe a découvert que les Th17 dépourvues de XPC portaient davantage de bris de brins d’ADN et de bases d’ADN oxydées, signature d’une attaque par des espèces réactives de l’oxygène. Les gènes qui détectent habituellement les dommages de l’ADN et arrêtent le cycle cellulaire étaient également réduits, ce qui suggère un système d’alarme affaibli. Le métabolisme énergétique des cellules était remodelé : elles perdaient une partie de leur capacité à utiliser les voies glycémiques à combustion rapide et dépendaient davantage de leurs mitochondries, les petites centrales à l’intérieur des cellules. Pourtant ces mitochondries fuyaient plus d’espèces réactives de l’oxygène et montraient des signes de souffrance, créant un cercle vicieux de stress chimique croissant et d’atteintes ADN accrues. Remarquablement, traiter les cellules avec un antioxydant a restauré la production d’IL‑17 et réduit les dommages à l’ADN, établissant un lien direct entre stress oxydatif et dysfonction observée.
Un effort collectif pour réparer l’ADN endommagé
Au-delà de son rôle classique, XPC coopérait aussi avec une autre protéine réparatrice appelée OGG1, qui reconnaît une base d’ADN oxydée courante. Les chercheurs ont montré que ces deux protéines s’associent physiquement dans les Th17, aidant à coordonner l’élimination des bases endommagées. En l’absence de XPC, l’activité de clivage d’OGG1 augmentait en fait, comme pour compenser l’excès de dommages. Mais cette suractivité intervenait dans un contexte de stress oxydatif élevé et de réseaux de réparation perturbés, et elle n’était pas suffisante pour restaurer la fonction normale des Th17. Des analyses génétiques et structurelles suggèrent que XPC agit comme un hub reliant différentes voies de réparation et le contrôle redox, veillant à ce que les dommages soient non seulement détectés mais aussi traités de façon à permettre à la cellule de continuer à se diviser et à produire des molécules protectrices.
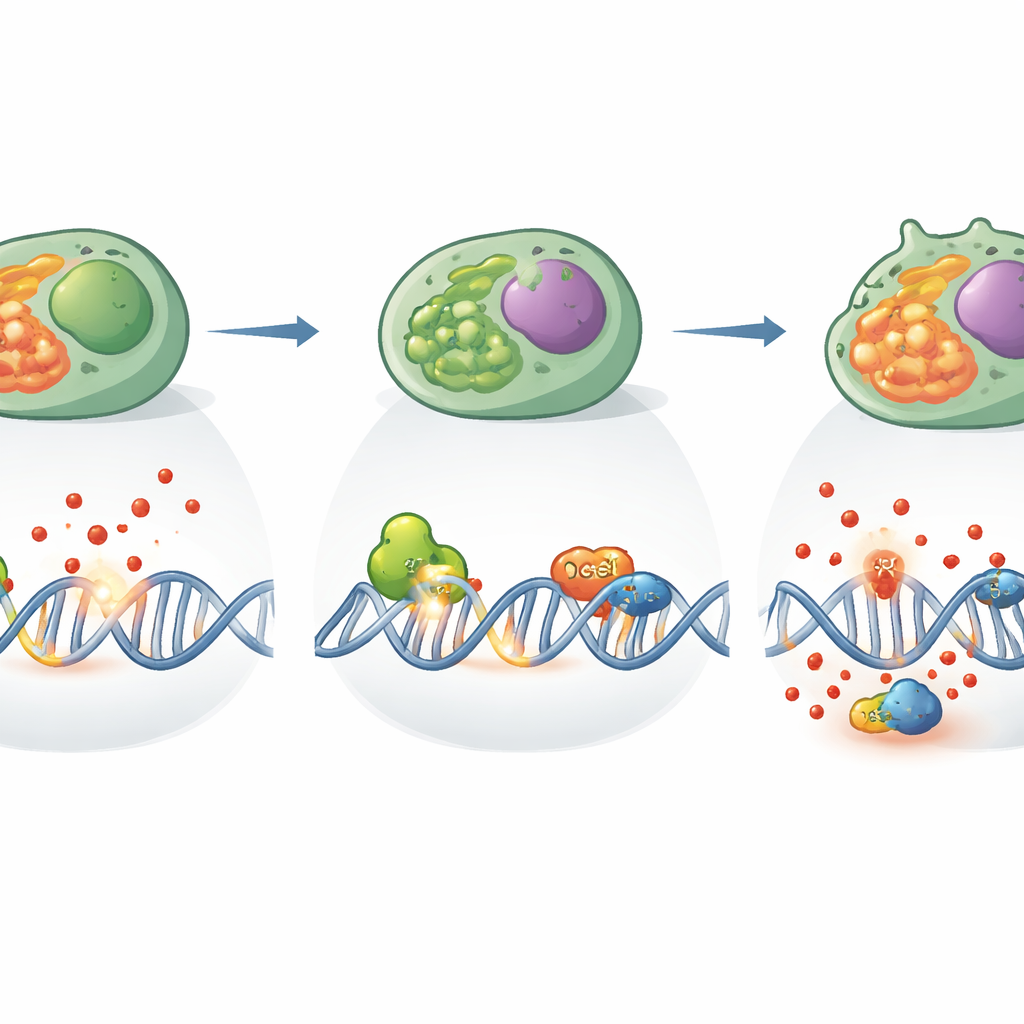
Pourquoi cela compte pour la maladie et la thérapie
Pour un lecteur non spécialiste, le message essentiel est que les cellules immunitaires ont besoin de gardes du corps internes pour rester en forme pendant qu’elles nous protègent. Cette étude révèle que XPC, connu pour protéger les cellules cutanées contre les UV, est aussi un gardien vital des Th17, préservant leur ADN et l’équilibre de leurs systèmes énergétiques face au stress oxydatif. En l’absence de XPC, les Th17 deviennent fragiles génétiquement et métaboliquement, produisent moins d’effecteurs inflammatoires et peuvent déplacer l’équilibre immunitaire vers la régulation plutôt que l’attaque. Étant donné le rôle central des Th17 dans des affections comme la maladie inflammatoire de l’intestin, le psoriasis et la sclérose en plaques, les voies contrôlées par XPC pourraient devenir de nouvelles cibles pour ajuster les réponses immunitaires — soit pour calmer une inflammation nuisible, soit pour renforcer la défense lorsqu’elle est trop faible — en modulant la façon dont ces cellules réparent leur ADN et gèrent le stress oxydatif.
Citation: Leite, J.A., Bos, N.N., Menezes-Silva, L. et al. Th17 cells require the DNA repair sensor xeroderma pigmentosum complementation Group C to control oxidative DNA damage in a murine model. Nat Commun 17, 3157 (2026). https://doi.org/10.1038/s41467-026-69914-y
Mots-clés: Cellules Th17, Réparation de l’ADN, Stress oxydatif, Protéine XPC, Maladie auto-immune