Clear Sky Science · fr
Le facteur d’initiation eucaryote 6 module la plasticité du carcinome pulmonaire à petites cellules via l’axe de signalisation intégrine-FAK
Pourquoi cette recherche sur le cancer du poumon est importante
Le carcinome pulmonaire à petites cellules (CPPC) est l’une des formes de cancer du poumon les plus mortelles. Il répond généralement bien à la chimiothérapie au départ, mais rechute presque toujours, rapidement et de manière agressive. Cette étude pose une question centrale : qu’est‑ce qui permet aux cellules de CPPC de « changer de personnalité » et de devenir résistantes aux médicaments, et peut‑on ralentir ou bloquer cette métamorphose ?
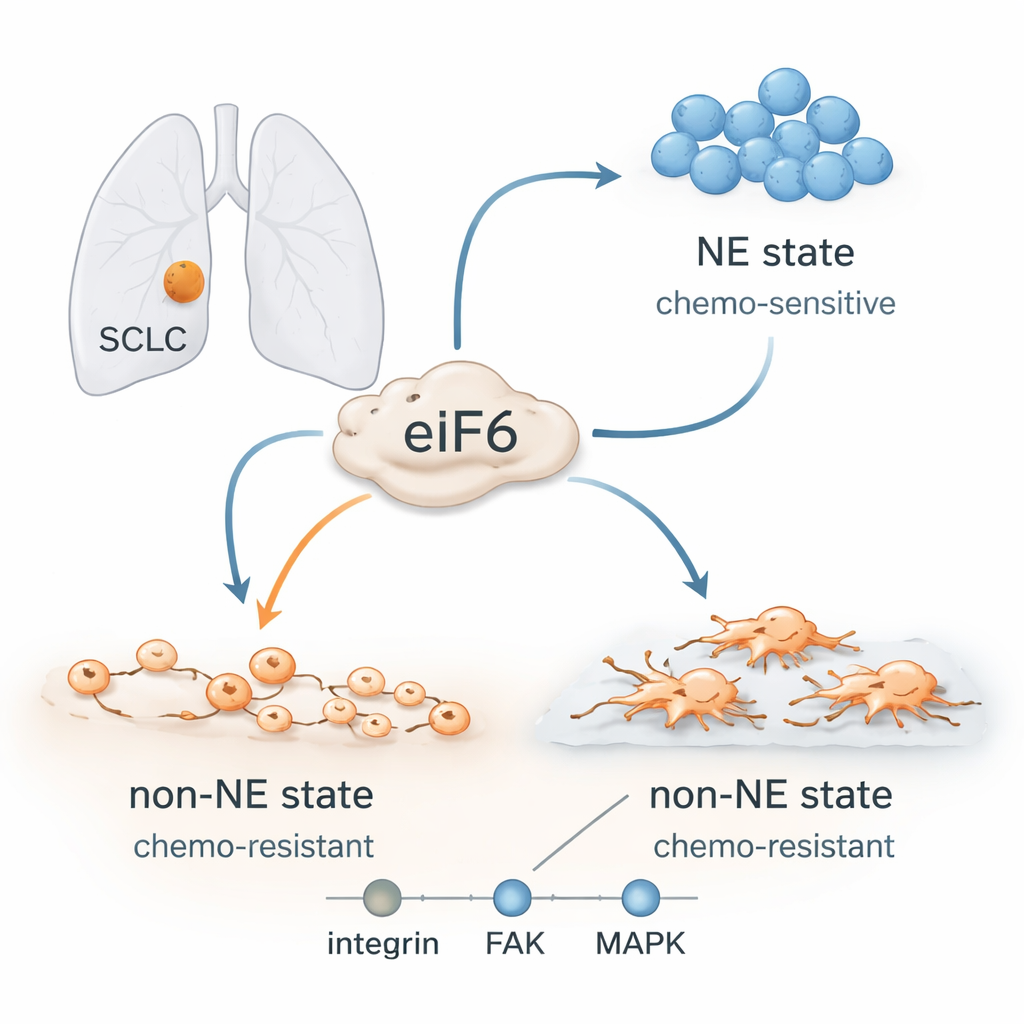
Des cellules cancéreuses qui changent de forme
Les cliniciens pensaient autrefois que le CPPC était une maladie homogène, mais il est maintenant clair que ces tumeurs contiennent différents types cellulaires. Certaines cellules possèdent une forte identité « neuroendocrine » : elles croissent en agrégats flottants serrés, répondent bien aux chimiothérapies à base de platine et sont riches en certaines protéines de type nerveux. D’autres perdent cette identité et adoptent un état « non neuroendocrine » : elles s’étalent, s’attachent aux tissus environnants, présentent des caractéristiques de cellules plus mobiles et invasives, et sont beaucoup plus difficiles à éliminer par les médicaments. Les tumeurs des patients évoluent souvent de l’état sensible vers l’état résistant pendant ou après le traitement, alors même que leur ADN change peu. Cela indique que des programmes cellulaires flexibles plutôt que de nouvelles mutations sont le moteur des rechutes.
Un facteur de traduction avec une double vie
Les auteurs se sont intéressés à une protéine appelée eIF6, surtout connue pour aider à assembler les ribosomes, les usines à protéines de la cellule. En étudiant des échantillons de patients, des modèles murins et plusieurs lignées cellulaires humaines de CPPC, ils ont constaté que les niveaux d’eIF6 augmentaient systématiquement lorsque les cellules basculaient vers l’état non neuroendocrine résistant aux médicaments. Fait surprenant, cette augmentation s’accompagnait d’une baisse globale de la production protéique en vrac, suggérant qu’eIF6 pourrait jouer un rôle au‑delà de sa fonction classique. Des analyses détaillées de l’association des ARNm aux ribosomes ont montré que les composants ribosomiques de base changeaient peu. En revanche, la sélection et le traitement des messages destinés à la traduction étaient remaniés lorsque les cellules changeaient d’identité.
Se détacher pour se raccorder aux signaux de survie
En creusant davantage, l’équipe a découvert que chez les cellules résistantes, eIF6 se détache en partie des ribosomes et s’associe à un centre de signalisation de surface construit autour des intégrines et d’une protéine appelée FAK (focal adhesion kinase). Les intégrines aident les cellules à détecter et à s’accrocher à leur environnement ; FAK relaie ces signaux vers l’intérieur, déclenchant souvent des voies qui favorisent le mouvement, la survie et la tolérance aux médicaments. Des expériences biochimiques d’affinité et des essais de proximité in situ ont montré qu’eIF6 interagit physiquement avec le partenaire intégrine CD104 et avec FAK, et que ces complexes sont plus abondants dans les cellules non neuroendocrines. Cet assemblage eIF6–intégrine–FAK renforce à son tour l’activité de la voie de signalisation MAPK, un moteur bien connu de la croissance et de la résistance au stress.
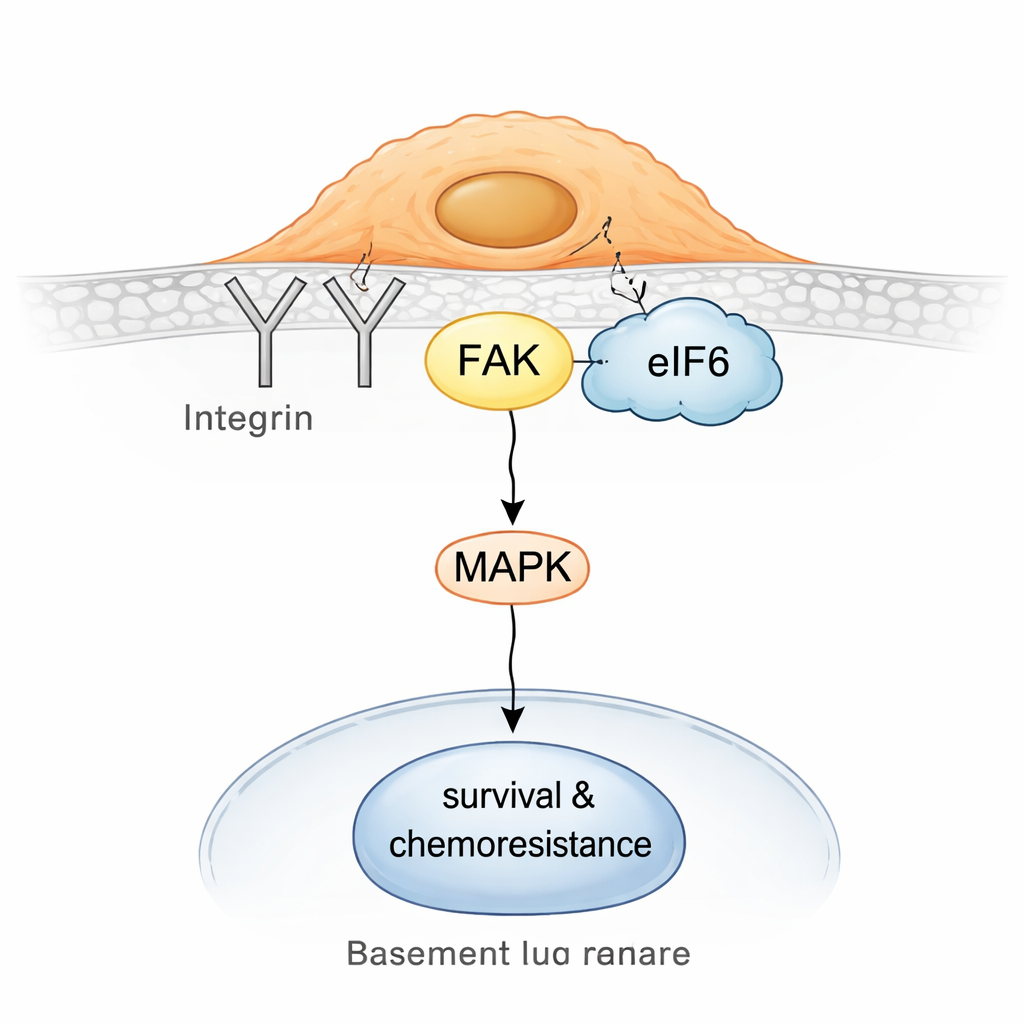
Rendre à nouveau les tumeurs résistantes vulnérables
Les chercheurs ont ensuite testé si la manipulation d’eIF6 pouvait modifier le comportement du CPPC. Lorsqu’ils ont réduit les niveaux d’eIF6 dans des cellules résistantes, les gènes associés à un programme mobile et formant des cicatrices (épithélial–mésenchymateux) ont été réprimés, tandis que des gènes neuroendocrines classiques ont été partiellement restaurés. Ces changements n’ont pas complètement fait revenir les cellules à l’état sensible, mais ils ont ralenti la transition vers l’état résistant. De manière cruciale, les cellules avec moins d’eIF6 sont devenues plus sensibles à la chimiothérapie standard carboplatine–étoposide en culture et dans des tumeurs murines, laissant moins de colonies survivantes et un rétrécissement tumoral plus durable. Comme il n’existe pas encore de médicaments spécifiques ciblant eIF6, l’équipe a testé des inhibiteurs de FAK déjà en développement clinique. Le blocage de la signalisation FAK a resensibilisé les cellules résistantes à la chimiothérapie et, chez la souris, le traitement combiné a donné le meilleur contrôle tumoral.
De l’éclairage en laboratoire à des outils futurs pour les patients
Enfin, les auteurs ont examiné des échantillons tumoraux de patients atteints de CPPC en stade limité ayant subi une chirurgie. En utilisant une méthode de marquage sensible qui illumine les protéines uniquement lorsqu’elles sont proches les unes des autres, ils ont mesuré la fréquence d’association d’eIF6 avec CD104 ou FAK à l’intérieur des cellules tumorales. Des niveaux élevés de ces complexes — plus encore que d’eIF6 seul — étaient corrélés à une récidive plus précoce et à une survie plus courte, en faisant des marqueurs pronostiques prometteurs. Pris ensemble, ces travaux révèlent qu’eIF6 peut « faire le travail d’appoint » en dehors des ribosomes pour aider à relier les cellules cancéreuses à des circuits de survie puissants. En cartographiant cet axe eIF6–intégrine–FAK, l’étude propose des moyens d’identifier les patients à risque accru de rechute et soutient l’association d’inhibiteurs de FAK avec la chimiothérapie pour contrer la plasticité dangereuse du CPPC.
Citation: Peng, H., Wang, Z., Wang, M. et al. Eukaryote initiation factor 6 modulates small-cell lung carcinoma plasticity via the integrin-FAK signaling axis. Nat Commun 17, 2048 (2026). https://doi.org/10.1038/s41467-026-69899-8
Mots-clés: carcinome pulmonaire à petites cellules, résistance aux médicaments, plasticité cellulaire, eIF6, signalisation intégrine FAK