Clear Sky Science · fr
Inhibition de la traduction dépendante du contexte comme modalité thérapeutique contre le cancer
Retourner les usines à protéines contre le cancer
Les cellules cancéreuses survivent en fabriquant en continu de grandes quantités de protéines « conductrices » à vie brève qui les maintiennent en croissance et en division. Cette étude explore une nouvelle façon de lutter contre le cancer en enrayant subtilement les machines de fabrication des protéines de la cellule — les ribosomes — uniquement lorsqu’elles essaient d’assembler des séquences protéiques particulières, en particulier celles présentes dans des oncogènes difficiles à cibler chimiquement comme MYC. Cette interférence sélective pourrait tuer les cellules tumorales tout en épargnant une grande partie de la synthèse protéique normale.
Comment les cellules fabriquent les protéines — et où ça peut dérailler
Toute cellule dépend des ribosomes, minuscules usines moléculaires qui lisent les messages génétiques (ARNm) et enchaînent les acides aminés pour former des protéines. La plupart des médicaments existants qui ciblent les ribosomes, comme les antibiotiques ou des anciens traitements anticancéreux, agissent comme des instruments grossiers : ils arrêtent la synthèse protéique de façon large, ce qui peut endommager les cellules saines et provoquer des effets secondaires sérieux. Les auteurs ont émis l’hypothèse que, parce que chaque chaîne protéique naissante a sa propre séquence et son caractère chimique distincts, il pourrait être possible de concevoir des petites molécules qui n’obstruent le ribosome que lorsqu’une séquence spécifique se trouve dans la machine, laissant le reste de la production protéique cellulaire en grande partie intact.
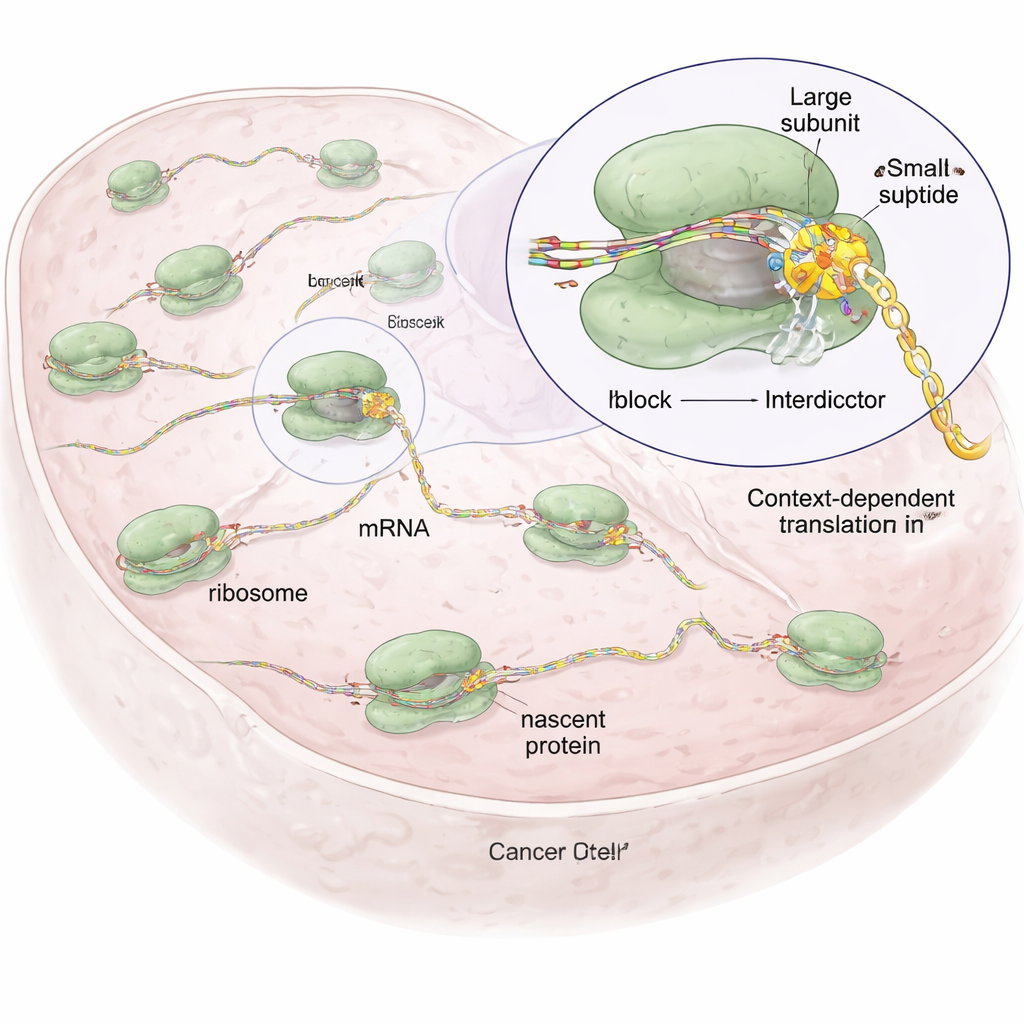
Molécules conçues qui n’arrêtent que certaines séquences protéiques
S’appuyant sur un composé naturel appelé anisomycine, qui se lie au cœur catalytique du ribosome où se forment les liaisons peptidiques, les chercheurs ont créé une famille de molécules synthétiques qu’ils appellent des « interdicteurs ». Elles partagent toutes un échafaudage central qui les ancre à l’intérieur du ribosome, mais diffèrent par des groupes latéraux orientés vers la chaîne protéique naissante. Ces groupes latéraux sont ajustés pour favoriser certains types d’acides aminés — par exemple, un interdicteur (IDB‑001) est attiré par des résidus chargés négativement, tandis qu’un autre (IDB‑002) préfère des résidus petits et hydrophobes. En utilisant une technique appelée profilage des ribosomes, qui cartographie globalement où les ribosomes marquent des pauses sur les ARNm à l’intérieur des cellules, l’équipe a montré que chaque composé provoque des arrêts sur des motifs courts distincts dans la chaîne naissante, souvent au résidu pénultième (−1), démontrant une action dépendante de la séquence plutôt qu’un arrêt indiscriminé.
Observer la rencontre médicament–ribosome atome par atome
Pour comprendre en détail la base physique de cette sélectivité, les auteurs ont figé des ribosomes humains en train de traduire des séquences peptidiques conçues et les ont imagés par cryo‑microscopie électronique à résolution quasi atomique. Ils ont observé l’interdicteur niché dans le site actif du ribosome, établissant des contacts précis avec les derniers acides aminés de la chaîne naissante. Dans une structure, un groupe latéral hydrophobe d’IDB‑002 est logé par de petits résidus non encombrants dans le peptide, ce qui explique pourquoi des chaînes latérales plus grosses y sont défavorisées. Dans une autre, la chaîne latérale acide d’un résidu dérivé de MYC se replie pour former un pont salin avec un groupe chargé positivement sur IDB‑001. La présence du médicament pousse aussi des bases d’ARN ribosomique voisines dans de nouvelles positions qui resserrent le site actif et bloquent partiellement l’entrée du prochain ARNt, contribuant à geler l’élongation sur ces séquences favorisées.
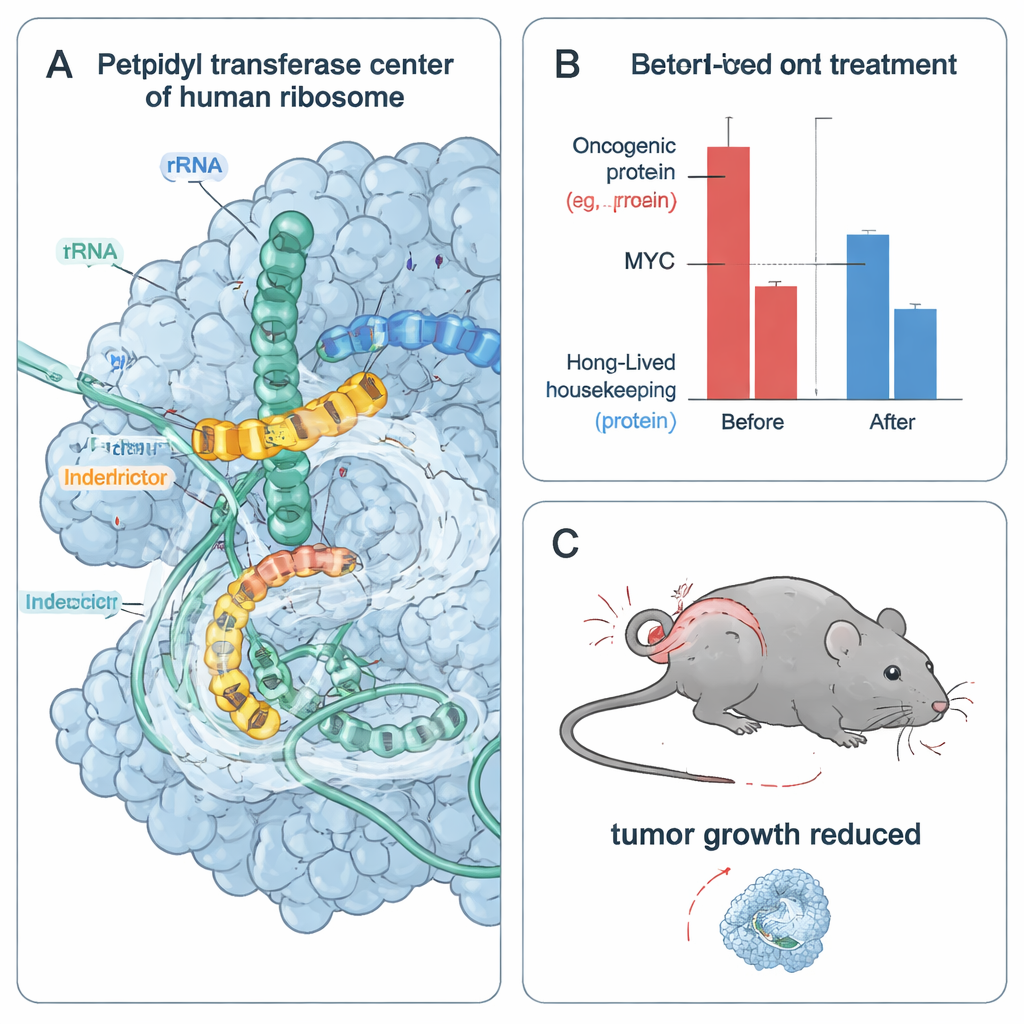
Des ribosomes bloqués aux cellules tumorales stressées et mourantes
Parce que les cellules cancéreuses en prolifération rapide dépendent fortement d’oncoprotéines à vie brève comme MYC et CCND1, l’équipe a testé l’effet des interdicteurs sur la survie des cellules tumorales. Dans plusieurs lignées cancéreuses dépendantes de MYC, IDB‑001 et IDB‑002 ont réduit la viabilité cellulaire à des concentrations nanomolaires à faibles micromolaires. Un analogue optimisé, IDB‑003, était encore plus puissant et adapté à l’administration orale. Dans les cellules, ces composés ont rapidement appauvri MYC et d’autres oncoprotéines à renouvellement rapide tout en laissant les protéines de ménage à plus longue durée de vie relativement stables sur la même fenêtre temporelle. Les médicaments ont également déclenché des réponses de stress cellulaires liées à des collisions de ribosomes, mais le blocage de ces voies de signalisation de stress n’a pas éliminé la perte de viabilité, ce qui suggère que la privation directe des protéines oncogéniques essentielles est un moteur majeur de la mort des cellules tumorales.
Preuve de concept dans un modèle difficile de cancer du sein
Pour vérifier si cette approche fonctionne chez l’animal, les auteurs ont traité des souris porteuses de tumeurs humaines du cancer du sein triple négatif avec IDB‑003 administré par voie orale. Sur 28 jours, les tumeurs des animaux traités ont crû beaucoup plus lentement que celles des témoins, avec jusqu’à 80 % d’inhibition de la croissance tumorale aux doses élevées et sans toxicité sévère rapportée dans cette étude. L’analyse de l’expression génique des tumeurs a montré une forte régulation à la baisse des programmes gérés par les cibles de MYC, compatible avec une activité réduite de MYC in vivo. Ensemble, ces résultats indiquent que l’arrêt sélectif des ribosomes sur des séquences protéiques spécifiques peut affaiblir des tumeurs dépendantes d’oncogènes instables tout en évitant potentiellement la toxicité large des inhibiteurs classiques de la traduction.
Pourquoi c’est important pour les traitements anticancéreux futurs
Ce travail introduit une nouvelle classe de petites molécules : des composés qui n’agissent pas en se liant à une protéine déjà formée, mais en l’interceptant au cours de sa synthèse et seulement lorsqu’une courte « étiquette d’adresse » séquentielle est présente. Parce que de nombreuses protéines promotrices de cancer sont flexibles, à vie brève ou dépourvues de poches évidentes pour des médicaments conventionnels, cibler leur synthèse directement au ribosome pourrait ouvrir la voie au traitement de tumeurs pilotées par des gènes actuellement « non drugables » comme MYC. L’étude suggère aussi qu’en modulant la chimie des interdicteurs, des médicaments futurs pourraient être conçus pour viser différents motifs de séquence et cibles pathologiques, étendant cette stratégie au‑delà de l’oncologie vers d’autres affections où diminuer des protéines spécifiques pourrait restaurer la santé.
Citation: Diamond, P.D., Sauer, P.V., Holm, M. et al. Context-dependent translation inhibition as a cancer therapeutic modality. Nat Commun 17, 1963 (2026). https://doi.org/10.1038/s41467-026-69891-2
Mots-clés: thérapie anticancéreuse ciblant les ribosomes, inhibition de la traduction, tumeurs dépendantes de MYC, petites molécules dépendantes du contexte, cancer du sein triple négatif