Clear Sky Science · fr
Ingénierie in situ de TRIM13 renforce la capacité anti‑inflammatoire des CAR‑M pour le traitement de la fibrose hépatique
Reprogrammer l’équipe de nettoyage du foie
La fibrose hépatique, un processus de cicatrisation qui peut évoluer vers la cirrhose et l’insuffisance hépatique, touche des millions de personnes et dispose aujourd’hui de peu de traitements efficaces. Cette étude explore une manière d’exploiter et de reprogrammer les propres cellules immunitaires du foie pour qu’elles n’enlèvent pas seulement les cellules productrices de cicatrices, mais apaisent aussi l’inflammation nocive, offrant potentiellement une thérapie plus sûre et plus puissante pour les maladies hépatiques chroniques.
Pourquoi l’arrêt de la cicatrisation hépatique est si difficile
Lorsque le foie est blessé de manière répétée — par des virus, l’alcool ou des troubles métaboliques — il tente de guérir en déposant du tissu cicatriciel. Des cellules spécialisées appelées cellules stellaires hépatiques basculent en un état « activé » et produisent des fibres résistantes, comme des bâtisseurs qui couleraient du béton. Avec le temps, cette cicatrisation, dite fibrose, déforme l’organe et altère sa fonction. Les macrophages, des cellules immunitaires, sont au cœur de ce processus. Dans un foie endommagé, ils peuvent agir comme une épée à double tranchant : dans un mode, ils favorisent l’inflammation et activent les stellates, tandis que dans un autre, plus réparateur, ils contribuent à décomposer la cicatrice et à restaurer l’équilibre.
Transformer les signaux nuisibles en signaux utiles
Les chercheurs se sont concentrés sur un signal de danger clé dans les foies abîmés : l’ADN mitochondrial qui fuit des cellules lésées. Les macrophages détectent cet ADN via une voie connue sous le nom cGAS‑STING, qui les oriente vers un état pro‑inflammatoire et pro‑fibrosant. Une protéine appelée TRIM13 aide normalement à contenir STING en la marquant pour destruction. L’équipe a émis l’hypothèse qu’augmenter TRIM13 à l’intérieur des macrophages hépatiques pourrait les faire basculer vers un mode apaisant et réparateur des tissus. Parallèlement, ils voulaient que ces cellules ciblent et suppriment directement les cellules stellaires productrices de cicatrices. Pour cela, ils ont utilisé le concept du récepteur antigénique chimérique (CAR), emprunté à l’immunothérapie contre le cancer : un récepteur synthétique qui permet aux cellules immunitaires de reconnaître une cible choisie — ici une protéine appelée FAP, abondante à la surface des stellates activées.
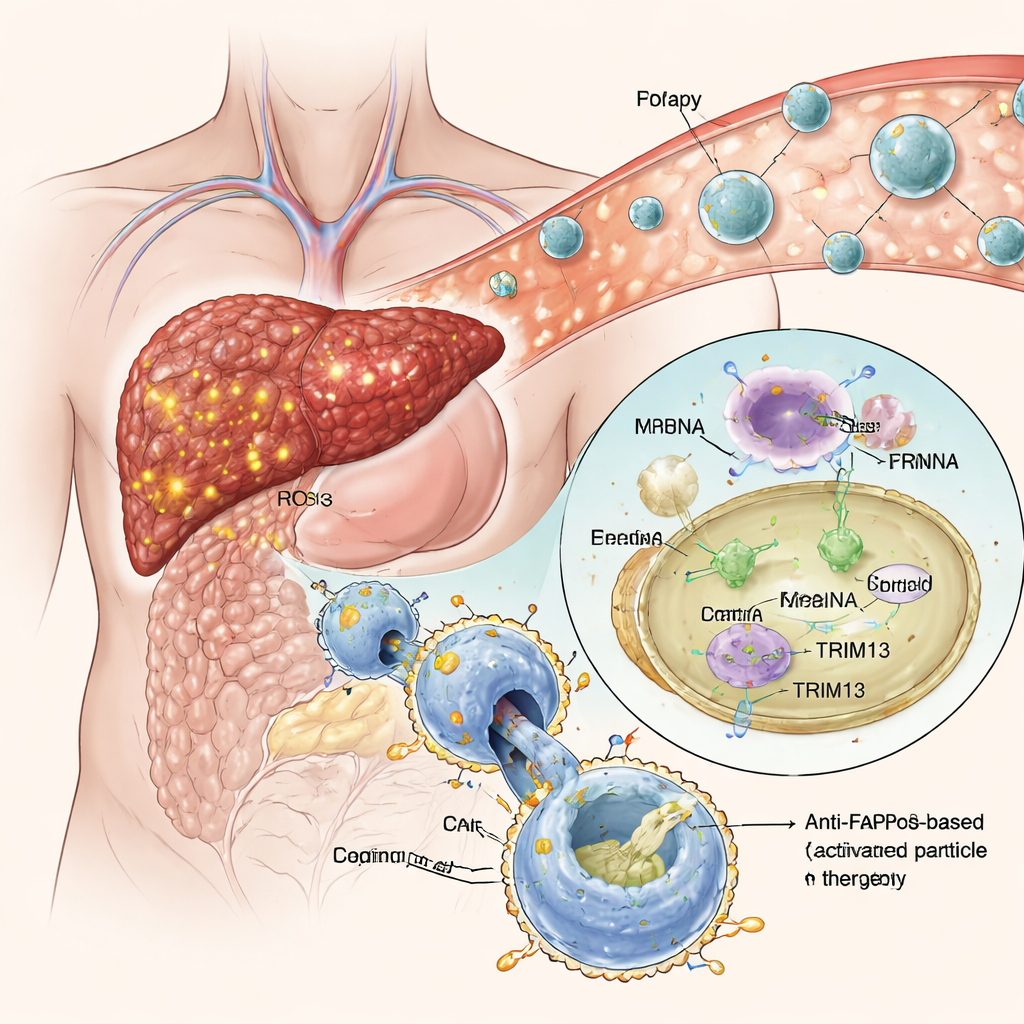
Nanoparticules intelligentes ciblant les tissus malades
Plutôt que d’ingénier les macrophages en dehors du corps, l’équipe a conçu des nanoparticules lipidiques « déclenchées par l’efférocytose » — de minuscules sphères lipidique transportant des instructions génétiques sous forme d’ARN messager (ARNm). Ces particules sont revêtues d’une forme déguisée de phosphatidylsérine, un signal naturel « mange‑moi » que les cellules mourantes affichent pour attirer les macrophages. Dans l’environnement fortement oxydatif du tissu hépatique fibrotique, ce déguisement est retiré et le signal est révélé, incitant les macrophages à engloutir les nanoparticules. Une fois à l’intérieur, l’ARNm est libéré et traduit par la cellule, conduisant à la production à la fois de TRIM13 et du CAR anti‑FAP. En cultures cellulaires, cette approche a réussi à orienter les macrophages vers un état anti‑inflammatoire tout en leur conférant un appétit fort et sélectif pour les cellules cicatrisantes FAP‑positives, sans altérer leur capacité normale à éliminer d’autres débris.
De foies malades à des foies en régénération chez la souris
L’équipe a ensuite testé cette stratégie dans des modèles murins de fibrose hépatique induite soit par une substance chimique toxique, soit par un régime riche en graisses et pauvre en nutriments. Les nanoparticules administrées systémiquement ont atteint efficacement le foie et, surtout chez les animaux fibrosés, ont été principalement internalisées par les macrophages. Là, les cellules modifiées ont montré une activité réduite de la voie STING et une production moindre de molécules inflammatoires, ainsi qu’une capacité accrue à tuer les cellules stellaires activées. Les analyses tissulaires ont révélé des baisses marquées de collagène et d’autres marqueurs de cicatrice, une matrice extracellulaire plus fine et plus normale, et une amélioration des tests sanguins de la fonction hépatique. Les foies des souris traitées présentaient davantage de cellules en prolifération et retrouvaient une architecture plus saine, suggérant une réparation réelle de l’organe plutôt qu’un simple atténuement temporaire de l’inflammation.
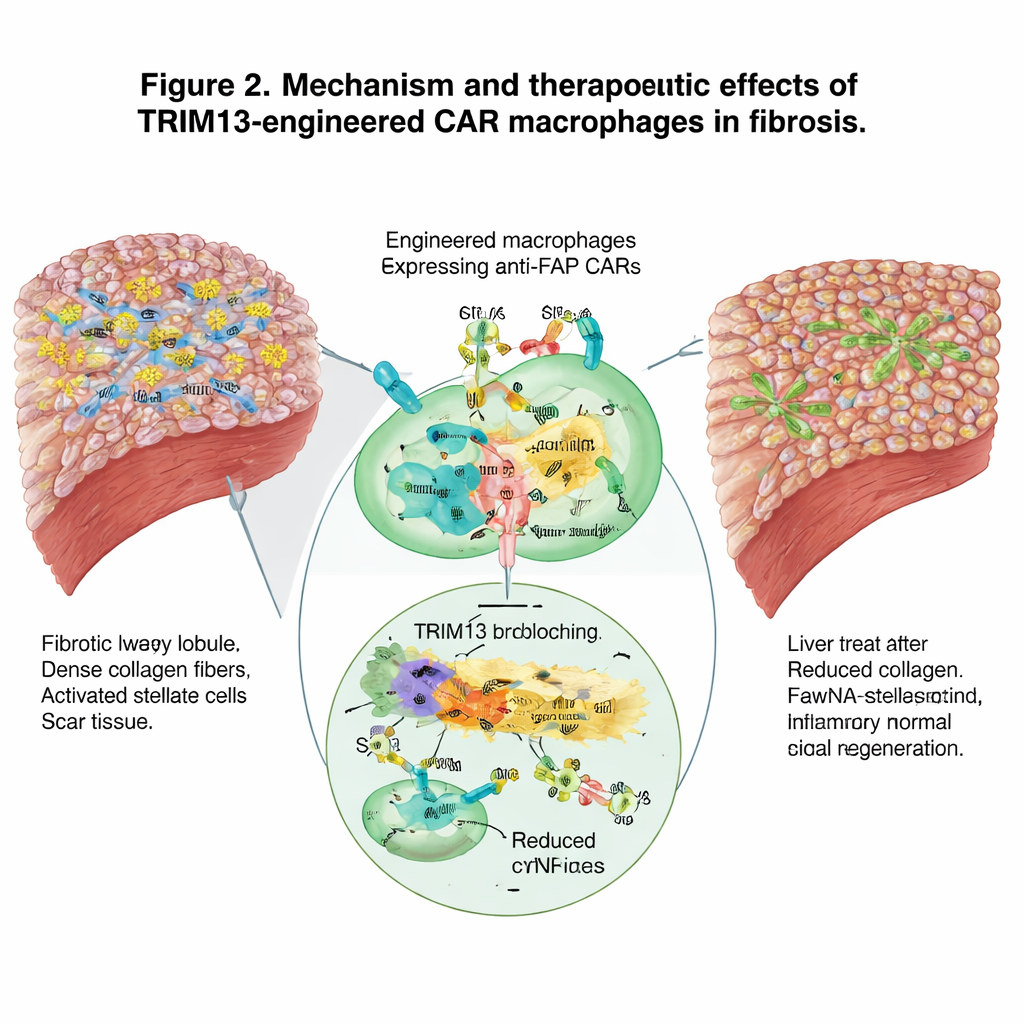
Mobiliser l’ensemble du système immunitaire
Au‑delà de l’élimination directe des cicatrices, les macrophages modifiés ont remodelé le paysage immunitaire plus large. Ils sont passés d’un profil agressif favorisant les lésions à un profil résolvant et réparateur, et ont réduit les signaux inflammatoires circulants. Parallèlement, en ingérant les cellules productrices de cicatrice, ils ont semblé former des « enseignants » pour le système immunitaire adaptatif, attirant des neutrophiles, des cellules dendritiques et des lymphocytes T et favorisant une réponse coordonnée contre le tissu fibreux. Le séquençage d’ARN unicellulaire des cellules immunitaires hépatiques a confirmé un recul des programmes géniques pro‑inflammatoires et une montée des capacités d’engloutissement et d’élimination des cellules et débris nuisibles.
Ce que cela pourrait signifier pour les patients
Pour un lecteur non spécialiste, la conclusion est que ce travail indique une voie pour « rééduquer » les cellules ramasseuses de déchets du foie afin qu’elles démantèlent la matrice cicatricielle tout en éteignant les signaux d’alarme chroniques qui entretiennent la lésion. En utilisant de courtes instructions ARNm à vie brève emballées dans des nanoparticules intelligentes, la thérapie évite de modifier les cellules de façon permanente et limite son action aux régions malades, ce qui pourrait réduire les effets secondaires. Bien que de nombreux tests supplémentaires soient nécessaires avant toute application humaine, cette stratégie trace un schéma prometteur pour traiter la fibrose hépatique — et potentiellement d’autres maladies fibreuses — en transformant le propre système immunitaire du corps, d’agent promoteur de cicatrisation en partenaire actif de la guérison.
Citation: Gao, J., Yang, Z., Song, Y. et al. TRIM13 in situ engineering boosts anti-inflammatory capacity of CAR-Ms for liver fibrosis therapy. Nat Commun 17, 2077 (2026). https://doi.org/10.1038/s41467-026-69858-3
Mots-clés: fibrose hépatique, thérapie par macrophages, libraison d’ARNm par nanoparticules, récepteur antigénique chimérique, TRIM13 voie STING