Clear Sky Science · fr
Maximiser l’utilisation de l’énergie et l’efficacité de lixiviation du lithium via une double oxydation électrochimique séquentielle et une phase de trempage-relaxation
Pourquoi les vieilles batteries de voiture comptent toujours
Les batteries lithium‑ion alimentent nos téléphones, ordinateurs portables et, de plus en plus, nos voitures. Mais à mesure que des millions de packs de véhicules électriques arrivent en fin de vie, ils génèrent une nouvelle catégorie de déchets — et une nouvelle opportunité. Le lithium et les autres métaux enfermés dans les batteries usagées ont de la valeur, mais leur récupération consomme beaucoup d’énergie. Cette étude explore une manière plus intelligente d’extraire le lithium en utilisant l’électricité de façon plus efficace, réduisant ainsi les coûts et l’impact environnemental tout en répondant à l’appétit croissant du monde pour les matériaux de batterie.
Transformer les batteries usagées en ressource
Aujourd’hui, la majeure partie du recyclage industriel des batteries lithium‑ion repose sur des produits chimiques agressifs ou des fours à haute température. Ces méthodes permettent de récupérer des métaux, mais gaspillent souvent de l’énergie et rendent difficile la séparation propre du lithium du nickel, du cobalt et du manganèse dans les batteries dites NCM. Les chercheurs se sont concentrés sur une voie plus récente et plus propre : utiliser un courant électrique dans de l’eau salée pour extraire le lithium du matériau de cathode usagé. Ils ont posé une question simple mais cruciale : peut‑on réorganiser le moment et la manière d’utiliser l’électricité pour que presque chaque watt contribue à extraire le lithium plutôt qu’à être perdu dans des réactions secondaires ?
Une danse en deux temps : puissance, puis calme
L’équipe a conçu un procédé en deux étapes qui combine une « poussée » active et un « trempage » calme. Dans la première étape, appelée double oxydation électrochimique, une tension constante est appliquée à une cellule contenant une cathode NCM usée et une solution de chlorure de sodium. Le courant extrait des ions lithium du solide vers le liquide tout en générant des espèces oxydantes puissantes dans la solution. Les scientifiques ont constaté que la majeure partie du travail utile se fait pendant la première heure : le lithium quitte rapidement la structure cristalline au début, mais ensuite une grande partie de l’énergie est gaspillée dans des réactions secondaires comme la formation de bulles d’oxygène.
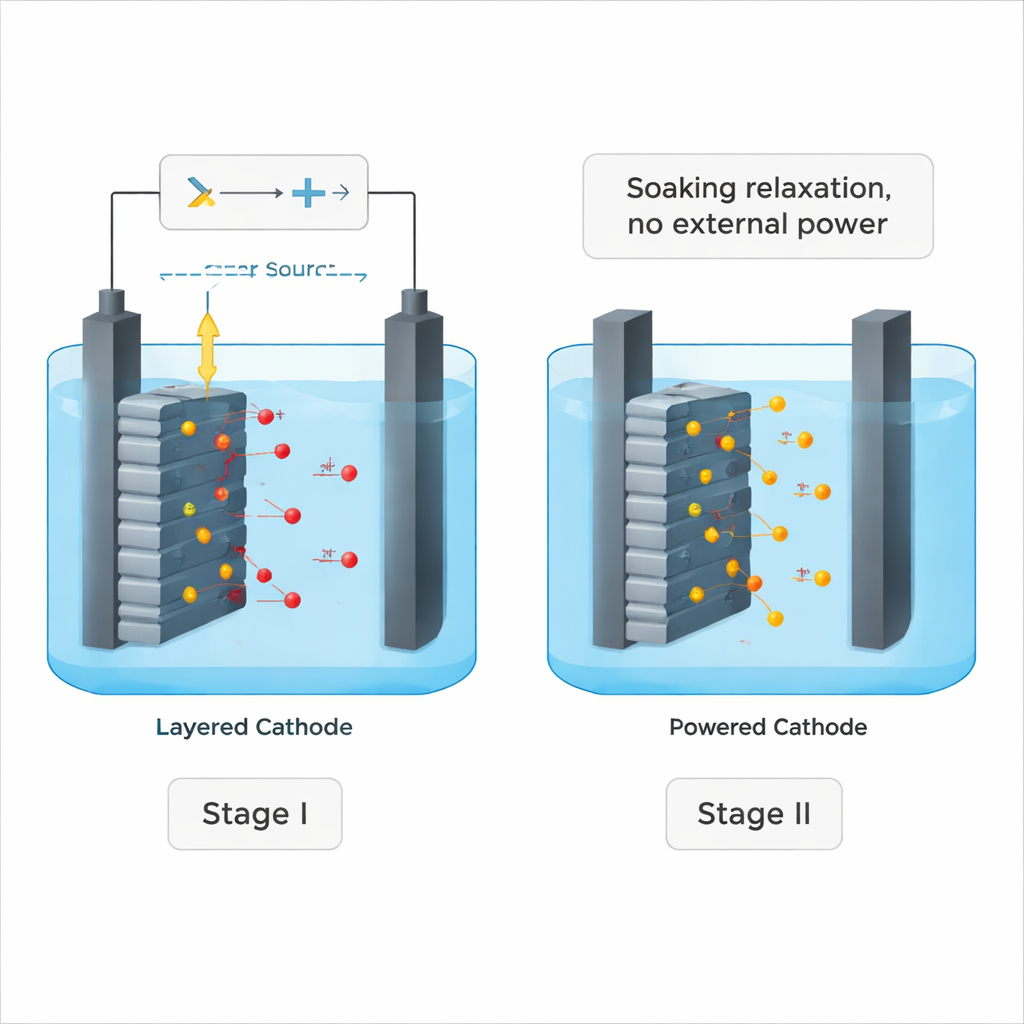
Laisser la chimie terminer le travail
Plutôt que de laisser le courant fonctionner de plus en plus longtemps, les chercheurs ont simplement coupé l’alimentation et laissé l’électrode tremper dans la solution salée désormais oxydante. De façon surprenante, le lithium a continué à se lixivier jusqu’à presque tout être retiré — atteignant environ 99 % de récupération pour du matériau NCM frais et autour de 98 % pour des cathodes réellement usées. Des mesures détaillées ont montré que des atomes d’oxygène à l’intérieur du cristal, temporairement poussés dans un état plus réactif pendant la phase sous tension, devenaient le moteur caché de cette seconde phase calme. Ces espèces d’oxygène « activées » favorisaient un échange lent : les ions lithium diffusaient vers le liquide pendant que des ions sodium (ou potassium) de la solution prenaient place dans les sites vides, le tout sans apport électrique supplémentaire.
Comment la structure cristalline se réarrange
À l’aide de microscopes électroniques, de diffraction des rayons X et de spectroscopies, l’équipe a observé les particules de cathode se fissurer, s’amincir et modifier leur empilement interne à mesure que le lithium s’en allait. Le matériau a traversé plusieurs empilements en couches connus en passant d’un état riche en lithium à un état pauvre en lithium, pour finir dans une forme enrichie en sodium qui maintenait la structure mais ne contenait plus beaucoup de lithium. Tout au long de ce processus, les atomes de nickel et de cobalt ont changé d’état d’oxydation pour garder l’équilibre électrique global du matériau, tandis que le manganèse est resté en grande partie inchangé, contribuant à stabiliser l’armature. Les chercheurs ont également montré que les ions potassium, qui perdent plus facilement leurs molécules d’eau que le sodium, pouvaient accélérer encore davantage l’étape d’échange ionique.
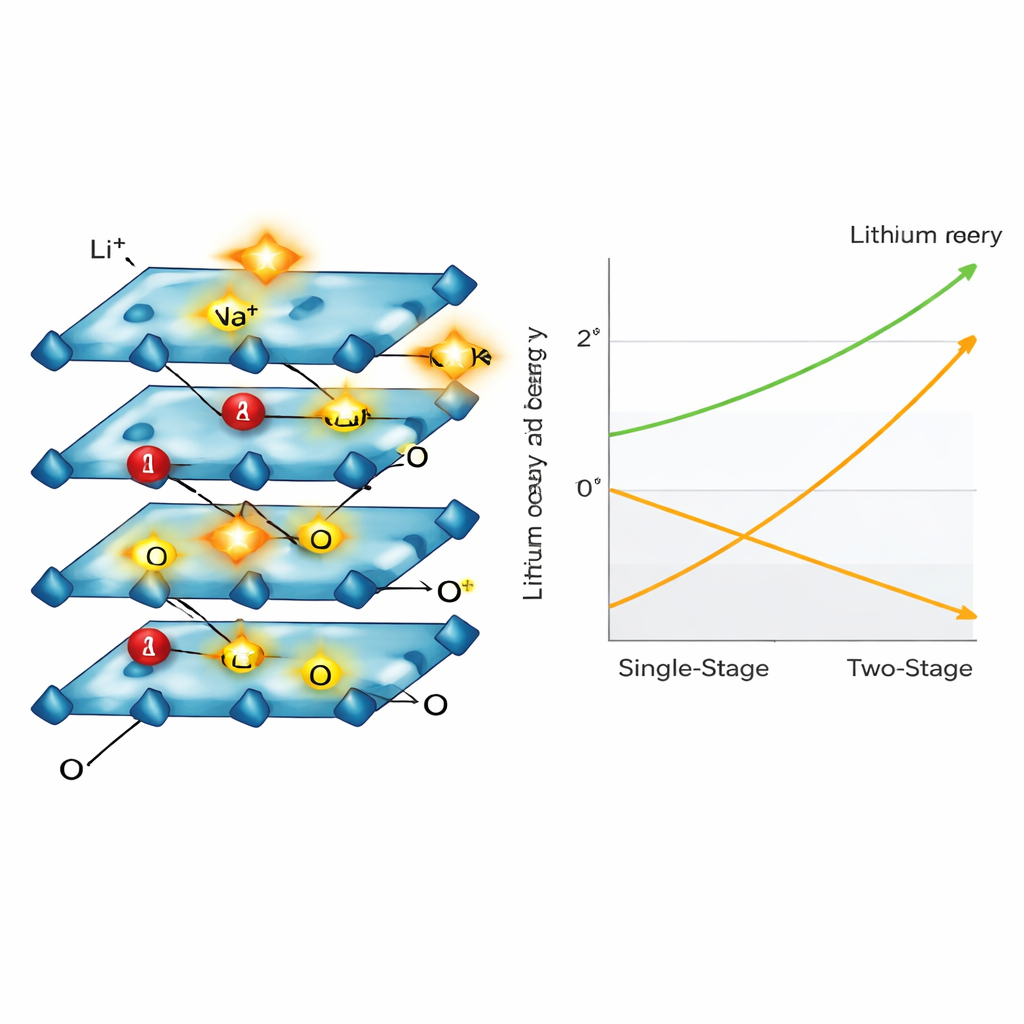
Du banc de laboratoire à l’atelier industriel
Pour vérifier si l’idée pouvait fonctionner en dehors du laboratoire, l’équipe a construit un pilote capable de traiter un demi‑kilogramme de déchets de batterie réels par lot. En utilisant leur méthode en deux étapes, ils ont récupéré plus de 98 % du lithium sous forme de carbonate de lithium de haute pureté, adapté à la fabrication de nouvelles batteries. Surtout, parce que l’alimentation électrique est coupée une fois que la « chimie intelligente » est lancée, le procédé a consommé environ deux fois moins d’énergie électrique qu’une méthode électrochimique monostade standard, économisant plus d’un cinquième du bénéfice d’exploitation total par tonne de matériau de cathode recyclé.
Ce que cela signifie pour les batteries de demain
En termes simples, l’étude montre que nous n’avons pas toujours besoin de continuer à injecter de l’électricité pour récupérer des matériaux précieux des vieilles batteries. Une poussée de puissance bien synchronisée peut préparer le matériau et la solution pour que le reste du travail se fasse de lui‑même, poussé par des forces chimiques internes. Si cette approche en deux étapes est adoptée à grande échelle, elle pourrait rendre le recyclage du lithium des batteries NCM usagées moins cher, plus propre et plus attractif pour l’industrie, contribuant à boucler le cycle de vie des batteries et à réduire la pression sur l’extraction de nouveau lithium.
Citation: Zhong, W., Gu, X., Feng, X. et al. Maximizing energy utilization and lithium leaching efficiency via sequential electrochemical dual-oxidation and soaking-relaxation. Nat Commun 17, 2050 (2026). https://doi.org/10.1038/s41467-026-69834-x
Mots-clés: recyclage du lithium, déchets de batteries, lixiviation économe en énergie, cathodes NCM, récupération électrochimique