Clear Sky Science · fr
Survie des cyanobactéries et atténuation des effets toxiques du Fe(II) dans un océan arquéen riche en silice
Mers anciennes et l’air que nous respirons
Des milliards d’années avant l’apparition des animaux ou des plantes, de minuscules microbes photosynthétiques appelés cyanobactéries ont commencé à libérer de l’oxygène dans les océans de la Terre. Pourtant, il faudra des centaines de millions d’années avant que l’oxygène ne s’accumule enfin dans l’atmosphère. Cette étude s’interroge sur les raisons de ce délai et sur la mesure dans laquelle la chimie des mers anciennes — riches en fer dissous et en silice — a aidé ou entravé ces microbes qui, au final, ont rendu notre planète respirable.

Mers riches en fer et un effet secondaire toxique
Les océans primitifs contenaient d’importantes quantités de fer dissous, en particulier dans les zones côtières où des eaux profondes remontaient vers la surface. Quand ce fer rencontrait l’oxygène produit par les cyanobactéries, il s’oxydait, formant des minéraux de fer qui deviendront plus tard les formations rubanées de fer — des roches striées qui constituent certains de nos plus anciens archives géologiques. Mais ces mêmes réactions peuvent aussi générer des « espèces réactives de l’oxygène », des formes hautement agressives de l’oxygène capables d’endommager l’ADN, les protéines et les membranes cellulaires. Des travaux antérieurs suggéraient que ce contrecoup chimique induit par le fer aurait pu empoisonner les cyanobactéries, ralentissant leur expansion et retardant l’augmentation de l’oxygène dans l’atmosphère.
La silice, un garde du corps inattendu
Les auteurs se sont concentrés sur un autre ingrédient abondant de l’eau de mer ancienne : la silice dissoute, le même matériau de base que l’on retrouve dans le verre. Les preuves géologiques indiquent que les océans primitifs contenaient des concentrations de silice bien plus élevées qu’aujourd’hui. En laboratoire, ils ont cultivé une cyanobactérie marine (Synechococcus sp. PCC 7002) sous conditions contrôlées avec des quantités variables de fer et de silice dissous. Ils ont suivi la vitesse de croissance des cellules, la quantité d’oxygène produite, la rapidité d’oxydation du fer et la formation d’espèces réactives de l’oxygène. À faibles concentrations de fer, les cellules prospéraient quelle que soit la silice. Mais lorsque le fer était très élevé — comparable aux conditions attendues dans certaines eaux côtières de l’Archéen — les cultures sans silice ajoutée déclinaient, tandis que celles à forte teneur en silice restaient actives, produisaient plus d’oxygène et atteignaient des densités cellulaires plus élevées.
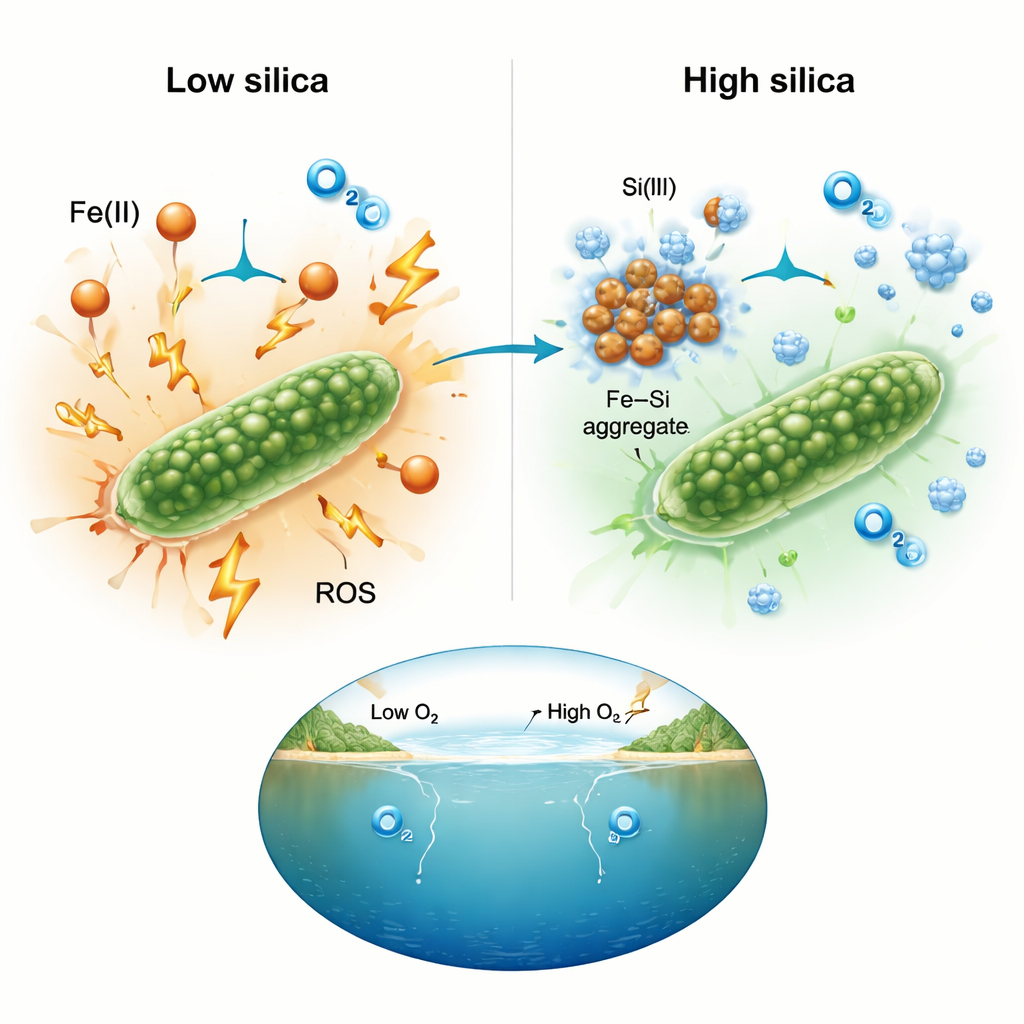
Une coopération chimique qui tempère les réactions nuisibles
Pour comprendre pourquoi la silice faisait une telle différence, l’équipe a mesuré les espèces réactives de l’oxygène directement à l’aide de colorants fluorescents. À fortes concentrations de fer, les cultures dépourvues de silice présentaient de forts signaux d’espèces réactives, cohérents avec une chimie stressante autour des cellules. Dans les milieux riches en silice, ces signaux restaient proches du niveau de fond même lorsque les concentrations de fer étaient extrêmes. Les chercheurs interprètent cela comme la liaison de la silice au fer dissous et la formation d’agrégats fer–silice. Une fois enfermés dans ces amas, le fer est moins disponible pour alimenter les réactions en chaîne qui génèrent des oxydants dommageables. L’effet net est d’adoucir l’environnement chimique, permettant aux cyanobactéries de continuer à photosynthétiser au lieu d’être paralysées par le stress oxydatif.
Rythmes jour–nuit et impacts à l’échelle océanique
Les expériences ont également été menées sous des cycles lumineux jour–nuit réalistes plutôt que sous une illumination constante. Dans ces conditions alternées, les cyanobactéries oxydèrent le fer plus rapidement et toléraient mieux les eaux riches en fer, ce qui suggère que les périodes de « repos » nocturne réduisent le stress à long terme. En utilisant les taux de production d’oxygène mesurés en laboratoire, les auteurs ont ensuite construit un modèle numérique simple d’une colonne d’eau océanique primitive. Pour des abondances plausibles de cyanobactéries et des taux réalistes de remontée d’eaux profondes, ils ont constaté que les eaux de surface pouvaient devenir riches en oxygène tandis que les couches profondes restaient chargées en fer. Dans de nombreux scénarios, les concentrations d’oxygène dans la zone éclairée atteignaient ou dépassaient les niveaux de saturation des eaux modernes, ce qui implique que des « oasis » locales d’oxygène au-dessus de profondeurs riches en fer ont pu être courantes.
Repenser pourquoi l’oxygène a mis tant de temps
Pris ensemble, les résultats suggèrent que les espèces réactives de l’oxygène formées à partir du fer et de l’oxygène n’étaient probablement pas un obstacle insurmontable pour les cyanobactéries primitives, à condition que la silice soit abondante et que les cycles naturels jour–nuit prévalent. Plutôt que d’être chroniquement empoisonnés, ces microbes ont probablement trouvé de nombreux milieux côtiers où la silice tamponnait les effets néfastes du fer, leur permettant de croître, d’oxyder d’énormes quantités de fer et de relâcher un excédent d’oxygène dans l’atmosphère. Le mystère persistant de la lente oxygénation de l’atmosphère terrestre doit donc davantage s’expliquer par des facteurs à grande échelle — tels que la rapidité avec laquelle l’oxygène était consommé par les gaz volcaniques et les roches — que par la chimie locale autour de cellules microbiennes individuelles.
Citation: Dreher, C.L., Cirpka, O.A., Schad, M. et al. Survival of cyanobacteria and mitigation of Fe(II) toxicity effects in a silica-rich Archean ocean. Nat Commun 17, 1987 (2026). https://doi.org/10.1038/s41467-026-69826-x
Mots-clés: oxygène de la Terre primitive, cyanobactéries, formations rubanées de fer, espèces réactives de l'oxygène, océans riches en silice