Clear Sky Science · fr
Exploiter un bioréacteur intestinal de souris sans germes pour l’évolution dirigée de probiotiques contre la stéatose hépatique non alcoolique
Pourquoi cette histoire intestinale compte pour votre foie
La stéatose hépatique non alcoolique (NAFLD) touche aujourd’hui plusieurs centaines de millions de personnes et est étroitement liée à l’alimentation et à la santé intestinale. Cette étude explore une idée inhabituelle : utiliser l’intestin lui‑même comme une sorte d’usine vivante pour « former » des bactéries bénéfiques afin qu’elles deviennent de meilleurs médicaments. En laissant des probiotiques évoluer chez des souris sans germes soumises à un régime riche en graisses, les chercheurs ont façonné une souche bactérienne qui gère plus efficacement les acides biliaires — des molécules détergentes qui relient notre alimentation à la façon dont le foie stocke les graisses. Ce travail suggère une nouvelle manière de concevoir des probiotiques de nouvelle génération naturellement adaptés à nos organismes plutôt que seulement modifiés en éprouvettes.
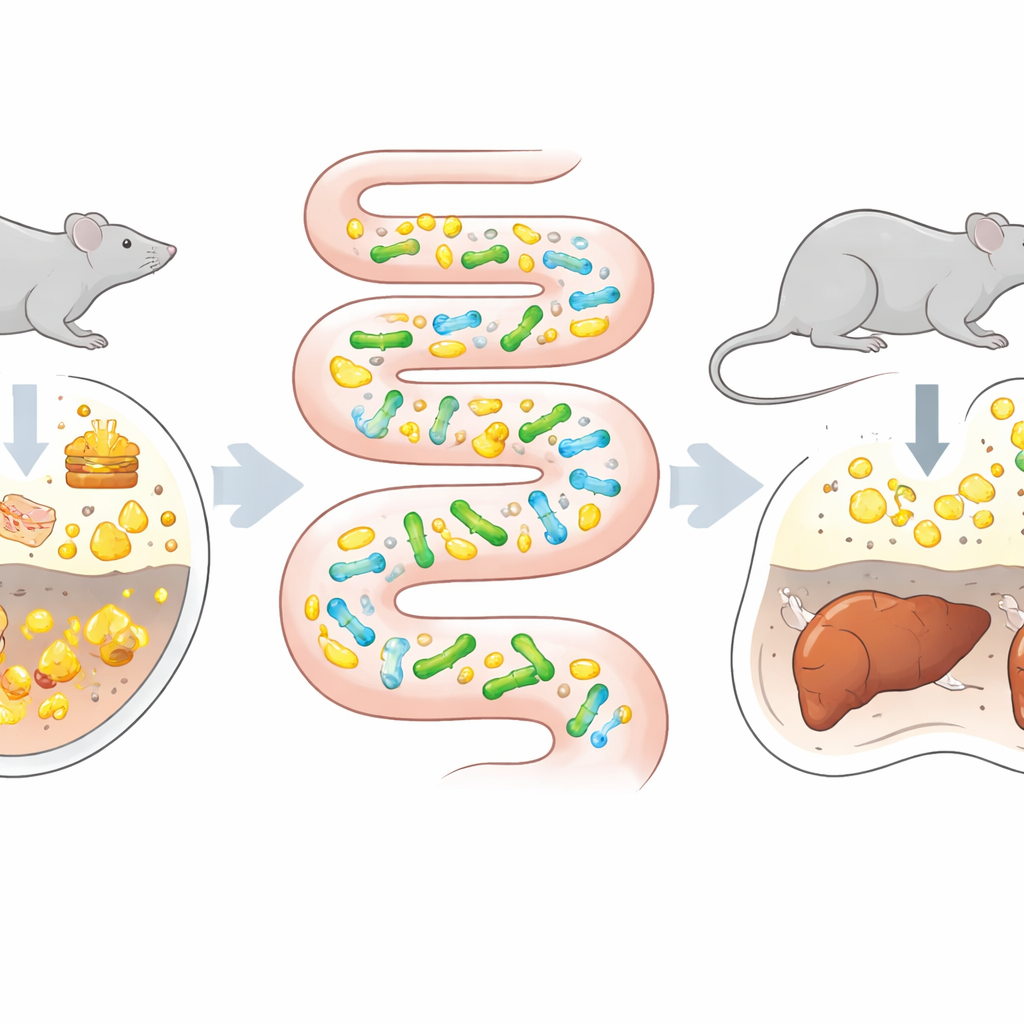
Transformer l’intestin en chambre d’évolution
L’évolution dirigée traditionnelle — faire muter des microbes et sélectionner les meilleurs — se déroule généralement dans des flacons de laboratoire. Cela fonctionne bien pour des enzymes ou des microbes industriels mais échoue souvent pour les probiotiques, qui doivent naviguer la chimie complexe, les signaux immunitaires et les forces physiques de l’intestin. Les auteurs se sont demandé : et si l’intestin lui‑même, avec toutes ses pressions naturelles, servait d’environnement sélectif ? Ils ont choisi une espèce probiotique, Bifidobacterium animalis subsp. lactis, qui possède déjà une certaine capacité à dégrader les acides biliaires. Des souris sans germes, qui ne portent aucun autre microbe, ont été colonisées par cette souche puis alimentées par paliers avec un régime de plus en plus riche en graisses et en cholestérol, connu pour augmenter les niveaux d’acides biliaires dans l’intestin. En parallèle, la même souche a été amenée à s’adapter dans un milieu de laboratoire standard contenant des acides biliaires, permettant une comparaison directe entre évolution in vitro et in vivo.
Un probiotique entraîné par l’intestin surpasse son cousin entraîné en laboratoire
Après passages répétés en flacons, les bactéries évoluées en laboratoire n’ont montré aucune amélioration significative de l’activité de traitement des acides biliaires. En contraste frappant, les isolats prélevés dans les intestins des souris nourries riche en graisses présentaient une large variation de performances ; environ un quart montrait une capacité clairement accrue à dégrader les acides biliaires. Le variant remarquable, nommé W5S9, métabolise les acides biliaires 77 % mieux que la souche parentale. Cette diversité, et la présence à la fois de gagnants et de perdants, met en évidence combien l’environnement intestinal de l’hôte exerce des pressions riches et multifacettes que de simples milieux de labo ne peuvent imiter. Cela confirme aussi que l’intestin peut agir comme un puissant « bioréacteur », générant et testant en continu des variantes génétiques dans des conditions proches de la vie réelle.
Zoom sur les mutations qui comptent
Pour comprendre ce qui avait changé dans W5S9, l’équipe a séquencé son génome et mesuré quelles gènes étaient plus ou moins actifs par rapport à la souche originelle. Parmi des centaines de petites différences d’ADN, deux ont émergé. L’une se situait juste en amont d’un gène appelé cbh, qui code pour une enzyme coupant les sels biliaires ; cette modification a agi comme un interrupteur d’activation plus fort, augmentant la production de l’enzyme sous stress biliaire. La seconde mutation a modifié la structure et l’activité d’une protéine de transport (MDR) qui expulse les acides biliaires traités hors de la cellule. Des tests en laboratoire ont montré que ces ajustements rendaient le probiotique meilleur à la fois pour couper les acides biliaires conjugués et pour exporter les produits résultants, améliorant sa survie dans des conditions riches en bile. En d’autres termes, l’évolution dans l’intestin a affiné à la fois les « ciseaux » et la « porte de sortie » de la voie des acides biliaires.
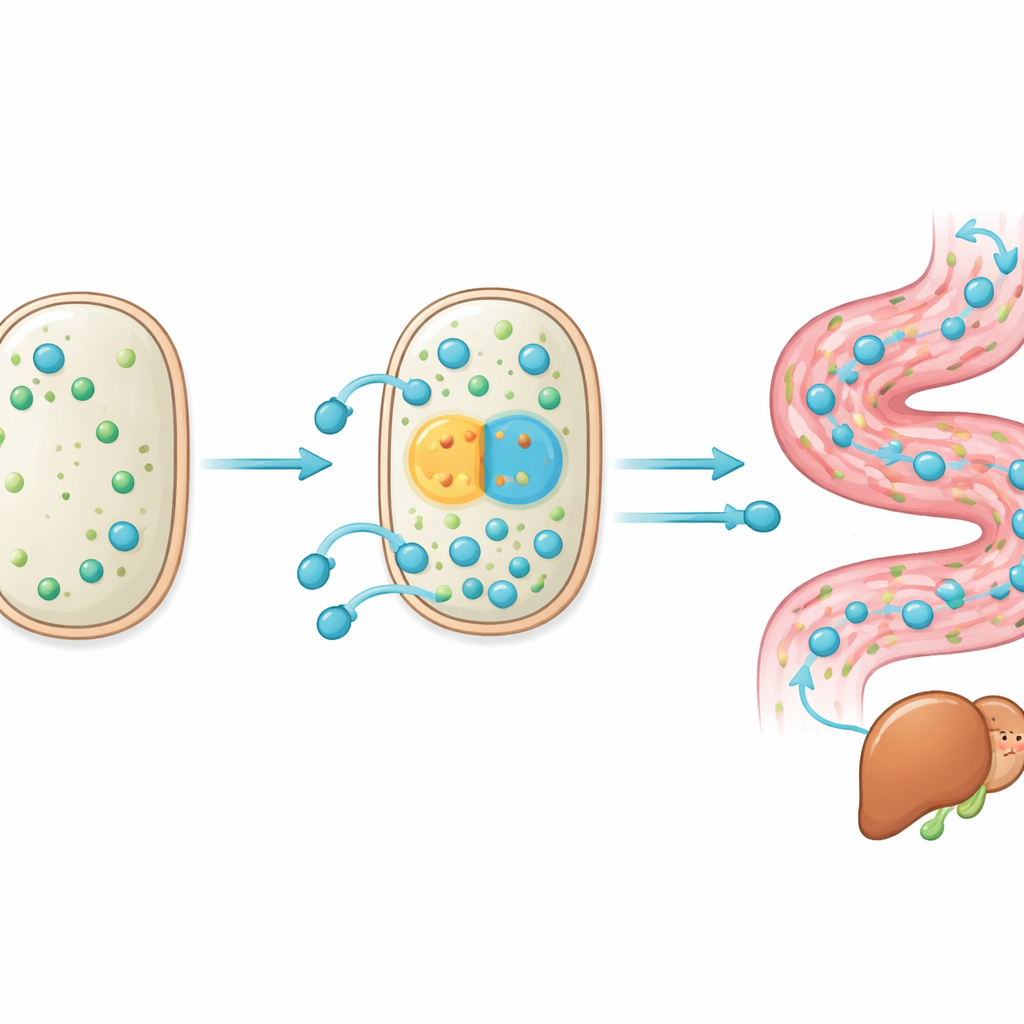
Protéger les foies graisseux dans un organisme stressé par le régime
Le test crucial était de savoir si cette souche entraînée par l’intestin pouvait réellement protéger un animal des lésions hépatiques. Les chercheurs ont utilisé un modèle murin de NAFLD, dans lequel un régime riche en graisses sur le long terme provoque une prise de poids, une accumulation de graisses dans le foie et une inflammation. Les souris ont été réparties en quatre groupes : alimentation normale, régime riche en graisses seul, régime riche en graisses plus le probiotique original, et régime riche en graisses plus la souche adaptée W5S9. Les deux groupes traités par probiotiques ont montré des améliorations par rapport au groupe riche en graisses, mais W5S9 a systématiquement fait mieux. Ces souris ont pris moins de poids, présenté de meilleurs profils de cholestérol, montré des marqueurs plus faibles de lésion et d’inflammation hépatiques, et avaient visiblement moins de gouttelettes de graisse dans les tissus hépatiques. Une analyse chimique détaillée des selles a révélé que W5S9 réduisait plus fortement les acides biliaires associés à la maladie et rééquilibrait le pool d’acides biliaires vers un état plus sain, sans remodeler de façon dramatique la communauté intestinale globale.
Ce que cela signifie pour les médicaments probiotiques futurs
Pour un public non spécialiste, le message clé est que les chercheurs n’ont pas simplement trouvé un « bon » probiotique — ils ont utilisé le corps lui‑même pour sculpter un meilleur probiotique. En laissant la sélection naturelle opérer dans des souris sans germes soumises à un environnement soigneusement conçu, riche en graisses et en bile, ils ont produit une souche qui gère plus efficacement les acides biliaires et, par conséquent, protège mieux le foie des dommages induits par le régime. Parce qu’aucun ADN étranger n’a été ajouté, ces microbes évolués restent non OGM, ce qui peut faciliter l’acceptation réglementaire et publique. L’implication plus large est que des stratégies d’évolution guidée par l’hôte similaires pourraient être adaptées à d’autres pathologies, de la maladie inflammatoire de l’intestin aux troubles métaboliques et même neurologiques, ouvrant la voie à des thérapies microbiennes vivantes personnalisées et fonctionnellement ajustées.
Citation: Han, Z., Sun, Z., Liu, X. et al. Harnessing a germ‑free mouse gut bioreactor for directed evolution of probiotics to combat non-alcoholic fatty liver disease. Nat Commun 17, 3133 (2026). https://doi.org/10.1038/s41467-026-69823-0
Mots-clés: probiotiques, microbiote intestinal, acides biliaires, maladie du foie gras, évolution dirigée