Clear Sky Science · fr
La cholécystokinine dérivée des cellules bêta favorise le développement d’adénocarcinome pancréatique associé à l’obésité
Quand le surpoids parle au pancréas
L’obésité augmente le risque de cancer du pancréas, l’un des plus mortels, mais la « conversation » biologique qui relie l’excès de masse grasse aux tumeurs restait floue. Cette étude met au jour un messager inattendu : une hormone digestive appelée cholécystokinine, ou CCK, produite à l’intérieur des cellules productrices d’insuline du pancréas. En suivant la façon dont ces cellules évoluent sous stress métabolique, les auteurs montrent comment une hormone destinée à aider l’organisme peut, au contraire, alimenter le cancer, et suggèrent de nouvelles façons d’intercepter la maladie avant qu’elle ne s’installe.
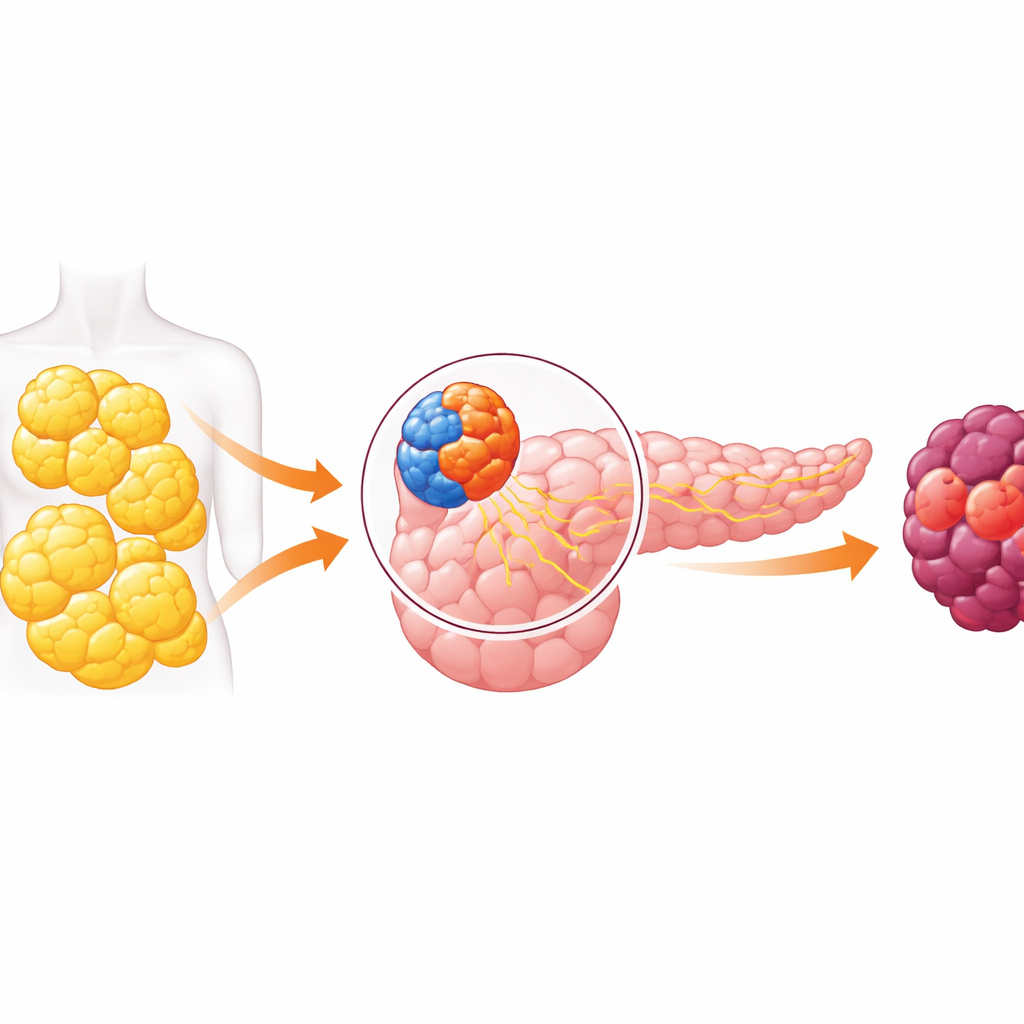
Un organe à deux visages et un dialogue dangereux
Le pancréas a deux fonctions principales. D’un côté, la partie endocrine contient de petites îles cellulaires qui libèrent des hormones comme l’insuline pour contrôler la glycémie. De l’autre, la partie exocrine produit des sucs digestifs et comprend les cellules qui donnent le plus souvent naissance au cancer du pancréas. Pendant des années, les chercheurs ont supposé que ces compartiments fonctionnaient en grande partie isolés. Des travaux récents ont renversé cette idée, montrant que des signaux provenant des cellules productrices d’hormones peuvent influencer les cellules digestives voisines. Cet article explore ce dialogue croisé et montre que, en cas d’obésité, il peut pousser la partie exocrine du pancréas vers la cancérisation.
Le stress des cellules hormonales déclenche un nouveau signal
Dans l’obésité, les cellules bêta productrices d’insuline sont soumises à une pression constante pour répondre à la demande croissante d’insuline. En utilisant le séquençage ARN unicellulaire et des outils computationnels avancés, les chercheurs ont suivi des cellules bêta individuelles chez la souris à mesure qu’elles passaient d’un état maigre à en surpoids puis à sévèrement obèses. Ils ont constaté qu’un sous-ensemble de cellules bêta immatures s’est étendu et a progressivement perdu son identité spécialisée d’insulinéosynthèse. À mesure que ces cellules étaient stressées, des marqueurs de la surcharge du pliage des protéines et des dommages cellulaires augmentaient, tandis que la production d’insuline diminuait. Parallèlement, ces cellules ont commencé à produire des niveaux élevés de CCK, une hormone habituellement associée à l’intestin qui peut stimuler la croissance et la transformation des cellules digestives.
D’une hormone utile à un carburant pour le cancer
Pour tester si cette CCK nouvellement produite n’était qu’un sous-produit du stress ou un véritable moteur de la maladie, l’équipe a conçu des souris dont les cellules bêta produisaient de la CCK en excès, même sans obésité. Ces animaux ont développé des lésions précancéreuses pancréatiques et des tumeurs invasives dans des proportions similaires à celles des souris obèses, malgré un poids et une glycémie normaux. En revanche, lorsque la CCK a été supprimée spécifiquement dans le pancréas de souris obèses, la charge tumorale a fortement diminué, même si les animaux restaient lourds et hyperinsulinémiques. Dans plusieurs modèles murins, les niveaux de CCK dans le pancréas suivaient de près la quantité de tumeur, tandis que les niveaux d’insuline avaient tendance à évoluer en sens inverse. Ces résultats désignent la CCK — et non l’insuline — comme l’hormone dominante reliant l’obésité au cancer pancréatique dans ces systèmes.
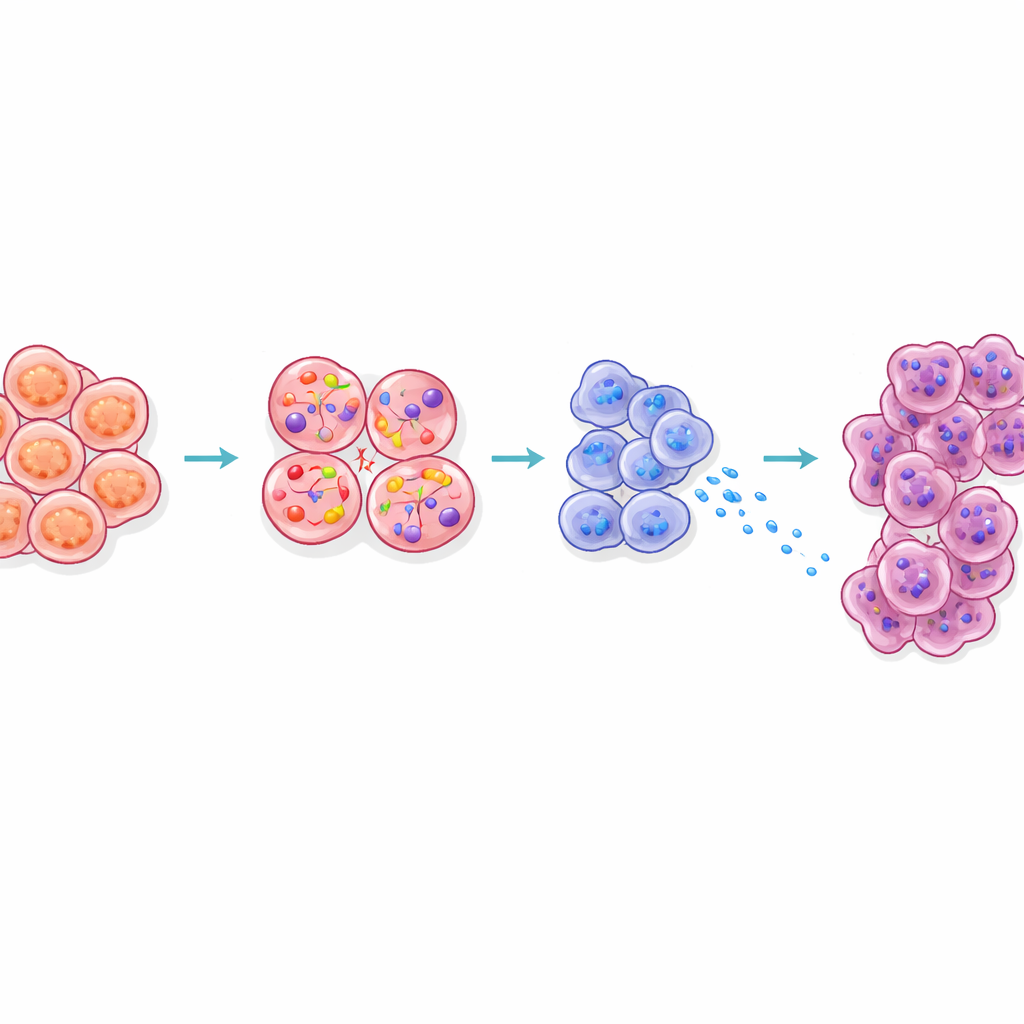
Comment le signal atteint et prépare les cellules voisines
L’étude a aussi examiné comment la CCK issue des cellules bêta remodèle le tissu environnant. Les cellules acinaires, qui sécrètent normalement des enzymes digestives, sont situées juste à côté des îlots dans le pancréas. Chez les souris obèses, les cellules acinaires proches des îlots présentaient un profil de stress, produisaient davantage d’enzymes digestives et de protéines dites Reg, et basculaient vers des états connus pour être plus facilement transformables en cancer. Le blocage de la signalisation CCK chez les souris obèses a réduit ces signaux Reg. L’imagerie tridimensionnelle a en outre révélé que les lésions précancéreuses précoces avaient tendance à apparaître anormalement près des îlots chez les animaux obèses. Ensemble, ces résultats suggèrent que la diffusion de la CCK depuis des cellules bêta stressées crée une « zone chaude » autour des îlots où les cellules digestives sont prêtes à se transformer en tumeurs.
Schémas partagés avec le diabète humain et un interrupteur clé
En comparant les données murines avec des tissus pancréatiques humains de personnes avec ou sans diabète de type 2, les auteurs ont trouvé des parallèles frappants : les cellules bêta des donneurs diabétiques correspondaient aux mêmes états stressés et moins matures observés chez les souris obèses. Ils ont ensuite utilisé une analyse régulatrice pour déterminer ce qui active la CCK dans les cellules bêta et ont identifié une voie sensible au stress centrée sur la protéine cJun. Lorsqu’ils ont bloqué la voie en amont JNK–cJun chez des souris obèses ou dans des cellules de type bêta en culture, les niveaux de CCK ont chuté, et cJun s’est montré lié à une région régulatrice du gène CCK. Cela suggère que le stress chronique active JNK–cJun, qui, à son tour, bascule les cellules bêta vers un mode de production de CCK.
Ce que cela signifie pour les personnes à risque
Pour un lecteur non spécialiste, le message central est que, sous la contrainte de l’obésité et du diabète, les cellules productrices d’insuline du pancréas ne se contentent pas de faiblir — elles s’adaptent d’une manière qui favorise involontairement la formation de cancer par les cellules voisines. Elles le font en activant la CCK, une hormone qui agit comme un signal de croissance et de stress pour les cellules digestives adjacentes, contribuant à créer un terreau propice aux tumeurs. Comme la CCK pancréatique n’est pas essentielle au contrôle de la glycémie, cibler cette source hormonale spécifique ou son interrupteur activé par le stress pourrait, en principe, réduire le risque de cancer pancréatique chez les personnes obèses ou atteintes de diabète de type 2 sans compromettre l’équilibre hormonal général. Ce travail requalifie le cancer du pancréas comme une maladie de communications mal orientées entre les deux parties de l’organe et met en lumière de nouvelles pistes pour la prévention précoce.
Citation: Garcia, C.C., Venkat, A., McQuaid, D.C. et al. Beta cell-derived cholecystokinin drives obesity-associated pancreatic adenocarcinoma development. Nat Commun 17, 3292 (2026). https://doi.org/10.1038/s41467-026-69821-2
Mots-clés: cancer du pancréas, obésité, cellules bêta, cholécystokinine, diabète de type 2