Clear Sky Science · fr
La formation d'un domaine PIN composite SMG5‑SMG6 est essentielle pour la DMM
Comment les cellules se protègent des messages défaillants
Nos cellules lisent en permanence des messages génétiques (ARNm) pour fabriquer des protéines. Mais ces messages contiennent parfois des signaux d’arrêt précoces qui donnent des protéines tronquées et potentiellement nocives. Le processus qui élimine ces messages défectueux s’appelle la décroissance des ARNm dépendante des codons d’arrêt prématurés (DMM, ou NMD en anglais). Cet article révèle comment deux protéines clés, SMG5 et SMG6, coopèrent physiquement pour cliver les messages défectueux, éclairant un mystère de longue date sur le fonctionnement du contrôle qualité cellulaire.
Découvrir le partenariat caché
Pendant des années, les chercheurs savaient que SMG6 peut cliver l’ARN directement, tandis que SMG5 était considéré comme « catalytiquement inactif », jouant surtout un rôle d’auxiliaire ou d’échafaudage. Pourtant, des expériences cellulaires montraient une énigme : SMG6 ne fonctionnait pas correctement sans SMG5, et la DMM s’effondrait si l’une ou l’autre protéine manquait. Les auteurs ont utilisé des prédictions de structure de pointe (AlphaFold), des essais biochimiques avec protéines purifiées et des tests génétiques dans des lignées cellulaires humaines pour résoudre cette contradiction. Leurs modèles prédisaient que les régions terminales de SMG5 et SMG6, appelées domaines PIN, s’emboîtent l’une contre l’autre pour former une structure conjointe. Cette unité composite — nommée « cPIN » — a été proposée comme la véritable machine de clivage dans la DMM. 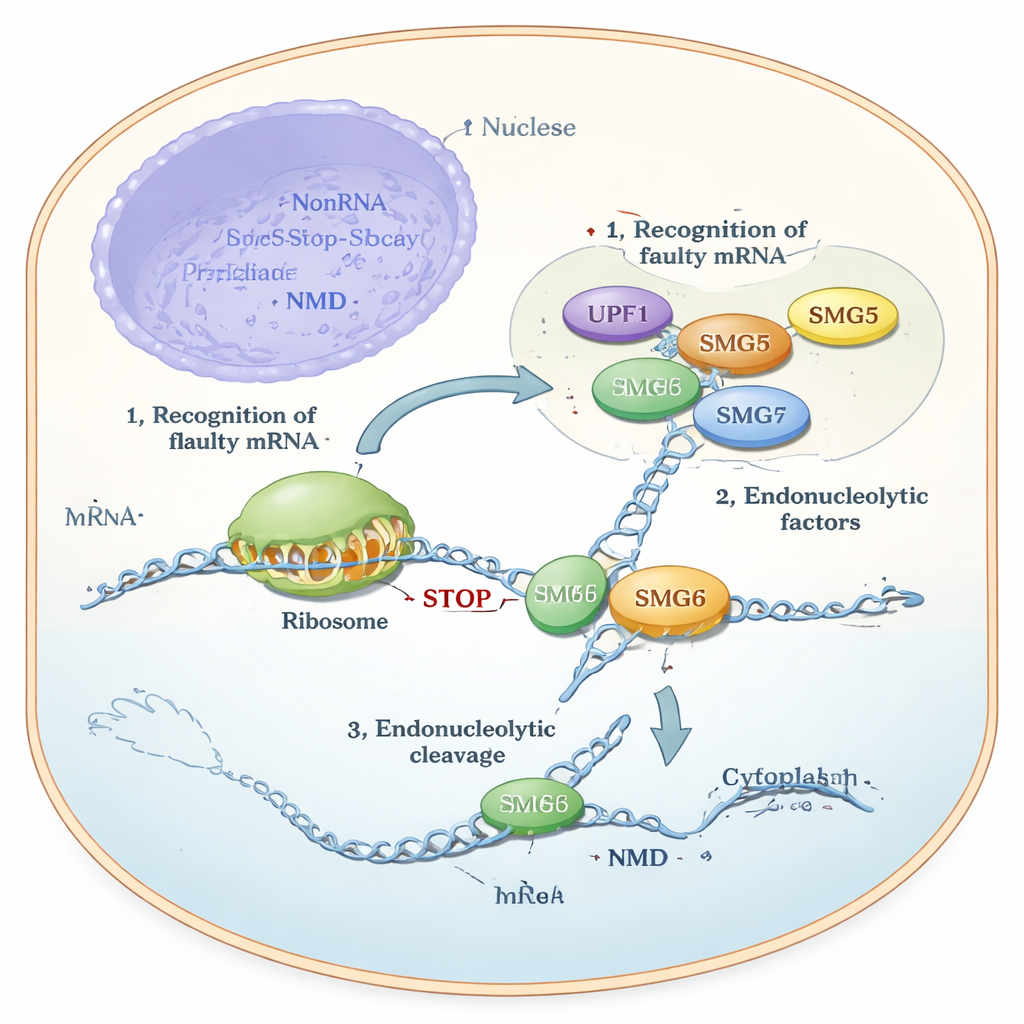
Reconstruire les ciseaux moléculaires en éprouvette
Pour tester la prédiction, l’équipe a produit des fragments humains de SMG5 et SMG6 dans des bactéries et les a purifiés. Pris individuellement, SMG6 montrait seulement une faible capacité à cliver un substrat ARN conçu, et SMG5 seul n’en montrait pratiquement aucune. Mais lorsque les deux fragments étaient mélangés, l’activité de clivage augmentait fortement, même dans des conditions rendant improbable l’intervention d’enzymes contaminantes. Le même effet apparaissait sur des molécules tests d’ARN linéaires et circulaires, indiquant que l’augmentation d’activité provenait réellement du duo SMG5–SMG6. Des expériences de réticulation chimique et de spectrométrie de masse ont en outre montré que les deux protéines se rapprochent physiquement, soutenant l’idée d’un partenariat direct, quoique transitoire.
Compléter la lame
Les modèles structuraux ont indiqué précisément comment SMG5 stimule SMG6. SMG6 apporte quatre acides aminés acides qui coordonnent des ions métalliques au cœur du site de clivage, comme c’est typique pour cette famille d’enzymes. De manière surprenante, les modèles plaçaient un acide aminé acide supplémentaire provenant de SMG5 juste à côté d’eux, étendant ainsi la poche catalytique. D’autres résidus chargés positivement de SMG5 étaient prédits pour saisir l’échine de l’ARN et aider à le positionner pour la coupure. Lorsque les chercheurs ont muté ces résidus critiques de SMG5 ou SMG6, le complexe composite perdait une grande partie de son pouvoir de clivage in vitro. Les mêmes mutations échouaient également à restaurer la DMM dans des cellules humaines modifiées où la protéine normale avait été appauvrie, reliant étroitement le modèle structural à la fonction cellulaire réelle. 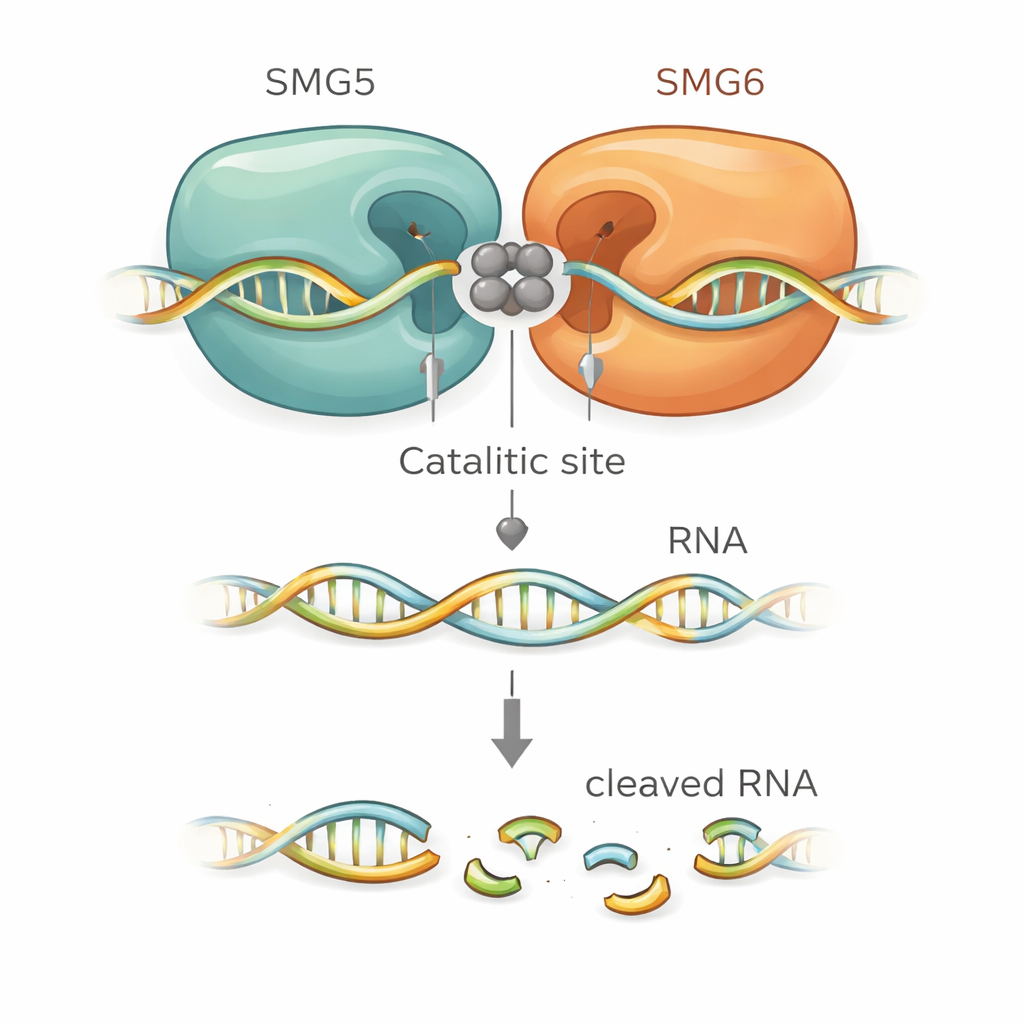
Prouver que les deux partenaires sont essentiels dans les cellules
Parce que l’élimination complète de SMG5 ou SMG6 est létale pour les cellules, l’équipe a utilisé un système de « dégron » permettant d’étiqueter chaque protéine pour qu’elle soit rapidement détruite par une petite molécule. En combinant cette dégradation rapide avec l’interférence ARN, ils ont obtenu une suppression quasi‑totale de SMG5, SMG6 ou d’un régulateur central nommé UPF1. Le séquençage global des ARNm a ensuite révélé ce qui arrive à la DMM lorsque chaque facteur est perdu. L’appauvrissement en SMG5 ou en UPF1 produisait des changements presque identiques dans les ARN cellulaires, avec une forte accumulation de transcrits défectueux sensibles à la DMM. La suppression de SMG6 donnait un effet très similaire, bien que légèrement moins marqué. Ces données montrent que SMG5 et SMG6 ne sont pas des branches parallèles optionnelles du cheminement ; au contraire, ils agissent ensemble avec UPF1 comme composants centraux d’une voie principale de dégradation.
Pourquoi cela compte pour la santé cellulaire
En termes simples, l’étude montre que SMG5 et SMG6 s’assemblent pour former une paire moléculaire unique et puissante de « ciseaux » qui coupe les messages génétiques défectueux. SMG6 fournit la majeure partie de la lame, mais SMG5 apporte un tranchant manquant et aide à maintenir l’ARN en place, transformant un coupeur faible en un instrument efficace. Cette « cPIN » composite explique pourquoi les cellules exigent absolument les deux protéines pour maintenir leurs messages ARN propres. En clarifiant comment l’étape clé de clivage de la DMM est activée uniquement lorsque des messages défectueux sont reconnus, le travail offre une image plus nette de la manière dont les cellules empêchent l’accumulation de protéines tronquées toxiques et réglent finement l’expression des gènes.
Citation: Kurscheidt, K., Theunissen, S., Pasquali, N. et al. Composite SMG5-SMG6 PIN domain formation is essential for NMD. Nat Commun 17, 1934 (2026). https://doi.org/10.1038/s41467-026-69819-w
Mots-clés: décroissance des ARNm dépendante des codons d’arrêt prématurés, contrôle de qualité des ARN, SMG5 SMG6, surveillance des ARNm, régulation de l'expression génique