Clear Sky Science · fr
Analyse d'association génomique à l'échelle du génome, efficace en calcul et en ressources, pour les grandes études d'imagerie
Plonger dans le plan génétique du cerveau
Pourquoi certains cerveaux vieillissent-ils mieux, résistent-ils aux troubles mentaux ou soutiennent-ils une mémoire et un apprentissage plus solides ? Les scanners cérébraux modernes et les tests génétiques promettent des réponses, mais le volume de données est écrasant. Cette étude présente une nouvelle méthode pour relier de petites différences d'ADN à des images cérébrales détaillées, rendant enfin pratique la recherche sur l'ensemble du génome contre des millions de points de mesure cérébraux. L'approche réduit non seulement fortement les coûts de calcul et les besoins de stockage, mais révèle aussi des motifs génétiques cachés qui lient des régions cérébrales spécifiques à des traits comme le niveau d'études, la dépression et la schizophrénie.
Des moyennes floues aux cartes cérébrales détaillées
La plupart des grandes études génétiques du cerveau simplifient les images en quelques centaines de mesures résumées, comme le volume global d'une région. Ce raccourci rend l'analyse faisable, mais il efface les détails fins. Chaque scanner contient en réalité des dizaines de milliers de petits emplacements, ou voxels, où la structure et les connexions peuvent varier. Un balayage direct « voxel par voxel » sur l'ensemble du génome serait idéal sur le plan scientifique, mais en pratique il aboutit à des milliards voire des billions de tests, nécessitant une puissance de calcul énorme et produisant des fichiers de synthèse trop volumineux pour être partagés ou réutilisés.
Une façon plus intelligente de compresser les images cérébrales
Les auteurs proposent un cadre appelé Representation learning-based Voxel-level Genetic Analysis (RVGA) pour résoudre ce goulet d'étranglement. RVGA commence par nettoyer chaque image cérébrale en séparant la structure lisse et significative du bruit aléatoire de l'appareil. Il apprend ensuite un petit ensemble de motifs sous-jacents — comme des briques de base de forme et de texture — qui peuvent être combinés pour reconstruire l'image d'origine. Le cerveau de chaque individu est résumé non pas par chaque voxel, mais par des scores sur ces motifs, réduisant la taille des données d'un à trois ordres de grandeur tout en conservant la majeure partie du signal. Ces scores de motifs sont ensuite traités comme des traits dans une étude d'association à l'échelle du génome standard, beaucoup plus rapide à exécuter.
Reconstruire l'image complète à partir de petits morceaux
De manière cruciale, RVGA ne s'arrête pas à ces traits compressés. En utilisant les motifs appris, il « projette » mathématiquement les résultats génétiques du niveau des motifs vers chaque voxel de l'image. Cette astuce permet aux chercheurs de récupérer des cartes d'association détaillées au niveau du voxel sans avoir à ajuster des milliards de modèles séparés. Tout ce qui doit être stocké et partagé se compose de trois ingrédients compacts : les résultats génétiques pour les motifs, les motifs d'image eux-mêmes, et la façon dont les scores de motifs varient entre les personnes. À partir de ce « triplet » minimal, RVGA peut reconstruire des cartes d'effets génétiques à pleine résolution, estimer combien la génétique contribue à la variation de chaque voxel, et calculer comment la génétique est partagée entre voxels et avec des traits externes.
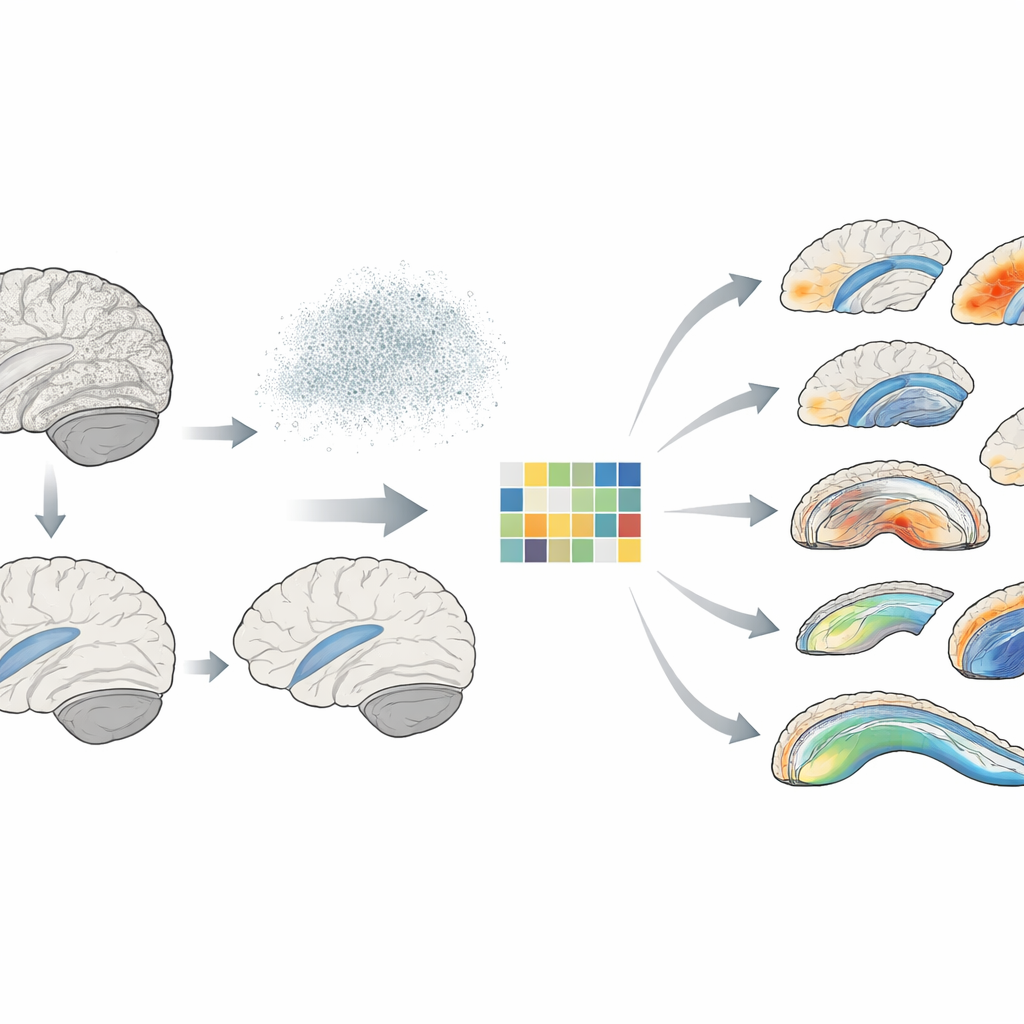
Ce que la nouvelle méthode révèle dans de vrais cerveaux
L'équipe a appliqué RVGA aux scanners cérébraux et aux données génétiques de plus de 53 000 participants de l'UK Biobank. Ils se sont concentrés sur la forme détaillée de l'hippocampe — cruciale pour la mémoire — et sur la structure fine des principales voies de matière blanche qui relient différentes régions du cerveau. Grâce à RVGA, ils ont identifié 39 régions génétiques auparavant non signalées affectant la forme de l'hippocampe et 275 nouvelles régions influençant la microstructure de la matière blanche, tout en répliquant de nombreuses découvertes connues. La méthode a réduit la taille des fichiers de synthèse génétique d'environ 229 fois, les rendant beaucoup plus faciles à partager. Elle a également révélé que l'influence génétique est loin d'être uniforme : certaines sous-régions de l'hippocampe présentaient une héritabilité bien plus élevée que d'autres, et certains segments de matière blanche portaient des signatures génétiques particulièrement fortes.
Liens avec l'éducation, l'humeur et les maladies mentales
Parce que RVGA peut être combiné avec des résultats génétiques d'autres études, les auteurs ont construit des « atlas » montrant comment les voxels cérébraux partagent des racines génétiques avec des troubles cérébraux et des traits associés. Ils ont trouvé, par exemple, que des parties de la queue de l'hippocampe et des structures voisines partagent des liens génétiques positifs avec le niveau d'études, alors qu'une autre sous-région, le présubiculum, montre un lien négatif. Dans la matière blanche, des segments spécifiques de la corona radiata antérieure partageaient des influences génétiques avec la schizophrénie, et des parties du corps calleux montraient des liens génétiques négatifs avec le trouble bipolaire. Beaucoup de ces motifs confirment des découvertes antérieures au niveau régional, mais RVGA les affine jusqu'à des sous-régions précises, suggérant des voies biologiques plus ciblées.
Pourquoi cela compte pour la santé cérébrale
En rendant possibles et partageables des analyses génétiques ultra-détaillées du cerveau, RVGA ouvre la porte à une nouvelle génération d'études d'imagerie génétique. Les chercheurs peuvent désormais voir exactement quelles petites zones de tissu cérébral sont influencées par des variants génétiques particuliers, avec quelle intensité, et de quelle manière ces zones partagent des racines génétiques avec la cognition et les troubles mentaux. Au fil du temps, de telles cartes pourraient aider à identifier des circuits biologiques à surveiller, à protéger, ou même à cibler dans des traitements personnalisés. La méthode se généralise aussi au-delà du cerveau à d'autres organes riches en imagerie, promettant un virage plus large des moyennes floues vers des aperçus génétiques à haute résolution.
Citation: Jiang, Z., Stein, J., Li, T. et al. Computation and resource efficient genome-wide association analysis for large-scale imaging studies. Nat Commun 17, 3313 (2026). https://doi.org/10.1038/s41467-026-69816-z
Mots-clés: génomique de l'imagerie, IRM cérébrale, association à l'échelle du génome, hippocampe, matière blanche