Clear Sky Science · fr
Interactions modulées métal-support pour une électroréduction efficace des nitrates à des potentiels positifs
Transformer l'eau polluée en ressource utile
La pollution par les nitrates dans les rivières, les lacs et les eaux industrielles est une préoccupation croissante pour les écosystèmes et la santé humaine, mais elle représente aussi une ressource gaspillées. Le même azote qui nuit aux cours d'eau peut être reconverti en ammoniac, pilier des engrais, des carburants et des produits chimiques. Cette étude explore une nouvelle façon d'épurer l'eau contaminée par les nitrates tout en récupérant de l'ammoniac avec une consommation d'électricité plus faible qu'auparavant, indiquant des pistes pour une agriculture plus propre, un traitement des déchets plus intelligent et de nouvelles formes de stockage d'énergie.
Pourquoi l'excès d'azote pose problème
L'agriculture moderne et l'industrie dépendent fortement de l'ammoniac, produit principalement par le procédé énergivore Haber–Bosch. Lors de son utilisation et de son élimination, une grande partie de cet ammoniac se retrouve sous forme de nitrate dans les eaux usées, perturbant le cycle naturel de l'azote et contribuant à des problèmes environnementaux tels que les proliférations d'algues et la contamination des eaux potables. Les méthodes existantes pour éliminer les nitrates peuvent être coûteuses et se contenter de déplacer ou diluer le problème. La conversion électrochimique des nitrates en ammoniac offre un moyen d'assainir l'eau tout en recyclant l'azote, mais la plupart des systèmes actuels exigent une forte énergie parce qu'ils doivent fonctionner à des tensions fortement négatives.
Concevoir une surface catalytique plus intelligente
Pour relever ce défi, les chercheurs ont conçu un nouveau catalyseur composé de petits agrégats de ruthénium ancrés sur des feuillets minces d'hydroxyde de cobalt. Ils ont utilisé une méthode simple de « corrosion auto-induite » : une mousse métallique se dissout lentement en présence d'un sel de ruthénium et d'oxygène, formant une couche fraîche d'hydroxyde pendant que des agrégats de ruthénium se déposent directement dessus. Ce procédé peut être appliqué à différents métaux, mais l'équipe s'est concentrée sur des supports à base de cobalt, de nickel et de fer pour voir comment chacun influence les performances. La microscopie et la spectroscopie ont confirmé que les agrégats de ruthénium sont ultrafins et répartis de manière homogène sur les feuillets d'hydroxyde, et que des transferts d'électrons ont lieu entre le métal et son support, ajustant subtilement la façon dont la surface interagit avec le nitrate et l'eau.

Équilibrer adhérence et flux pour une meilleure conversion
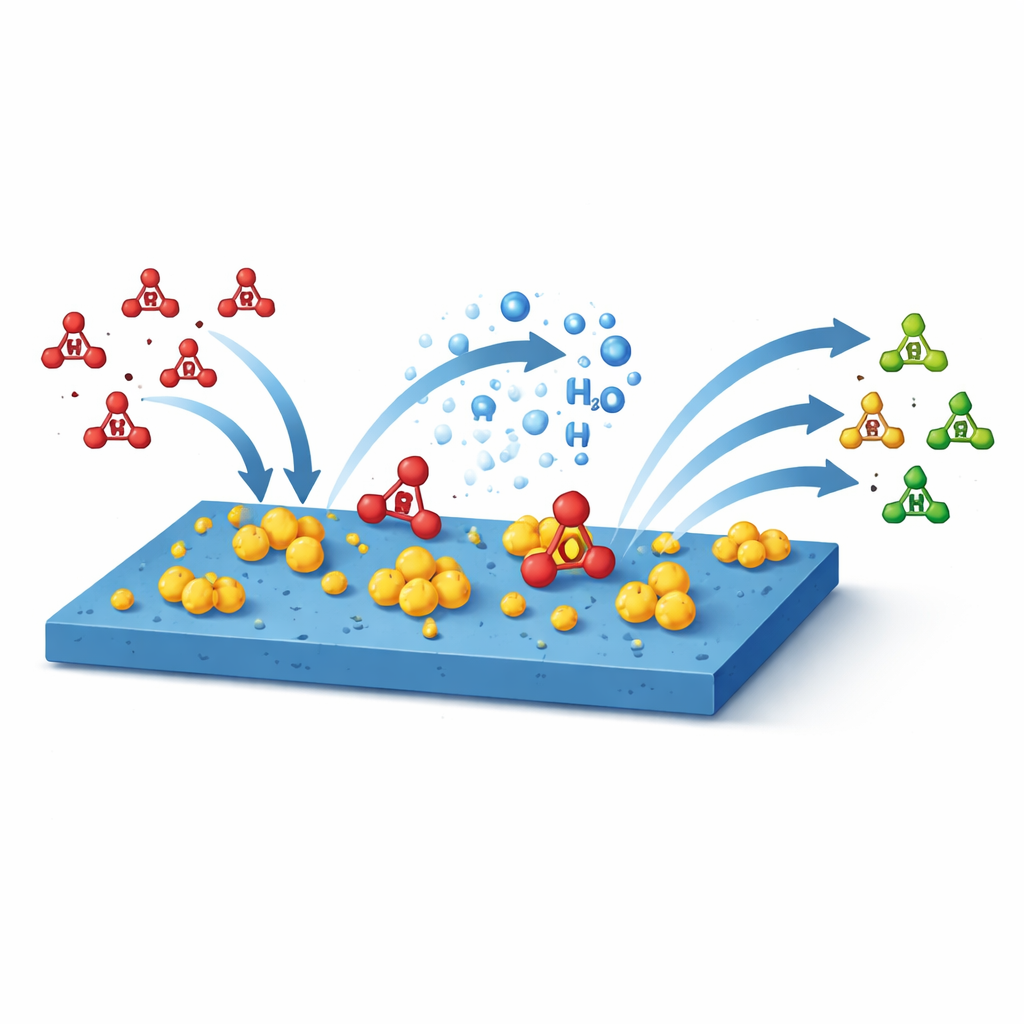
Pour que la réaction fonctionne efficacement, deux choses doivent se produire en harmonie : le nitrate doit adhérer à la surface du catalyseur suffisamment fortement pour réagir, et l'eau à l'interface doit se dissocier pour fournir des atomes d'hydrogène « actifs » qui transforment progressivement le nitrate en ammoniac. Si le nitrate se lie trop fortement, la surface s'encombre ; s'il se lie trop faiblement, il s'échappe sans être utilisé. De même, une dissociation lente de l'eau prive la réaction en hydrogène. Les tests ont montré que le catalyseur à base de cobalt atteint ce juste équilibre. Comparé aux versions supportées par le nickel et le fer, il amorce la réaction à une tension plus proche de l'idéal, atteint une sélectivité pour l'ammoniac proche de 100 % et atteint une efficacité énergétique d'environ 50 % à un potentiel de fonctionnement positif — une demande d'énergie remarquablement faible pour cette chimie. Il conserve aussi une forte activité pendant plus de 1 200 heures à des niveaux de courant pertinents industriellement, tout en réduisant la concentration de nitrate dans des eaux usées simulées en dessous des limites de potabilité.
Observer les étapes cachées
Pour comprendre pourquoi le cobalt fonctionne le mieux, l'équipe a surveillé la réaction en temps réel à l'aide de sondes optiques et électrochimiques, et a soutenu les observations par des modélisations informatiques. Ils ont constaté que le support en hydroxyde de cobalt reconfigure la couche mince d'eau à la surface, affaiblissant son réseau de liaisons hydrogène de sorte que les molécules d'eau se dissocient plus facilement en fragments réactifs. En parallèle, l'interaction électronique entre l'hydroxyde de cobalt et le ruthénium ajuste la force de liaison du nitrate et de ses intermédiaires. Les calculs montrent que sur cette surface, l'étape la plus difficile — la conversion d'un fragment de type nitrosyle en une espèce plus riche en hydrogène — nécessite beaucoup moins d'énergie que sur les versions supportées par le nickel ou le fer. En pratique, le support au cobalt fournit le juste équilibre : le nitrate est maintenu fermement sans être piégé, et l'eau fournit rapidement de l'hydrogène, permettant à la séquence d'étapes du nitrate à l'ammoniac de se dérouler sans accroc.
Du nettoyage des déchets au stockage d'énergie et à l'upcycling des plastiques
À partir de ce catalyseur efficace, les auteurs ont assemblé une batterie rechargeable qui associe du zinc métallique à la réduction des nitrates sur une cathode cobalt–ruthénium. Pendant la décharge, le nitrate est converti en ammoniac pendant que le zinc s'oxyde, fournissant de l'énergie électrique. Lors de la charge, ils remplacent la réaction habituelle de formation d'oxygène par l'oxydation plus douce de l'éthylène glycol, un bloc de construction pouvant être récupéré à partir de plastiques usagés. Cette astuce réduit l'énergie nécessaire pour recharger la batterie et valorise des molécules issues du plastique en produits de plus grande valeur, tandis que l'ammoniac produit peut être transformé en sels d'ammonium. Le dispositif hybride fonctionne de manière stable sur de nombreux cycles, illustrant comment le contrôle de la pollution, la récupération de ressources et le stockage d'énergie peuvent être intégrés dans un même système.
Un nouveau levier pour une chimie plus propre
En termes accessibles, ce travail montre que le réglage fin des interactions entre un catalyseur métallique et son matériau de support peut améliorer considérablement l'efficacité de la conversion des nitrates nocifs en eau en un ammoniac utile. En choisissant un support qui ne retient ni trop fermement ni trop faiblement le nitrate, et qui facilite la rupture de l'eau pour alimenter la réaction, les chercheurs atteignent de hautes efficacités à des tensions plus douces et maintiennent les performances sur de longues périodes. Le même principe de conception — ajuster soigneusement les interactions métal-support — pourrait guider le développement de futurs catalyseurs pour de nombreux autres procédés chimiques durables.
Citation: Tang, Y., Wan, Y., Yan, W. et al. Modulated metal-support interactions for efficient nitrate electroreduction at positive potentials. Nat Commun 17, 3006 (2026). https://doi.org/10.1038/s41467-026-69802-5
Mots-clés: pollution par les nitrates, production d'ammoniac, électrocatalyse, traitement des eaux usées, stockage d'énergie