Clear Sky Science · fr
Analogues non hydrolysables de l’acétyllysine pour étudier l’acétylation des protéines in vitro et en cellules
Pourquoi de petites étiquettes chimiques sur les protéines comptent
À l’intérieur de chaque cellule, les protéines sont constamment modulées par de petites étiquettes chimiques qui agissent comme des interrupteurs marche/arrêt ou des variateurs d’intensité pour leur activité. L’une des plus importantes de ces étiquettes est l’acétylation, qui peut modifier le comportement d’une protéine sans changer son code génétique sous‑jacent. Comprendre précisément ce que fait l’acétylation en un site donné d’une protéine spécifique a été étonnamment difficile, car les cellules peuvent retirer ces étiquettes aussi rapidement qu’elles les ajoutent. Cette étude présente un « remplaçant » chimique ingénieux de l’acétylation qui ne peut pas être retiré, offrant aux scientifiques un moyen de figer ces interrupteurs et d’observer ce qui se passe.
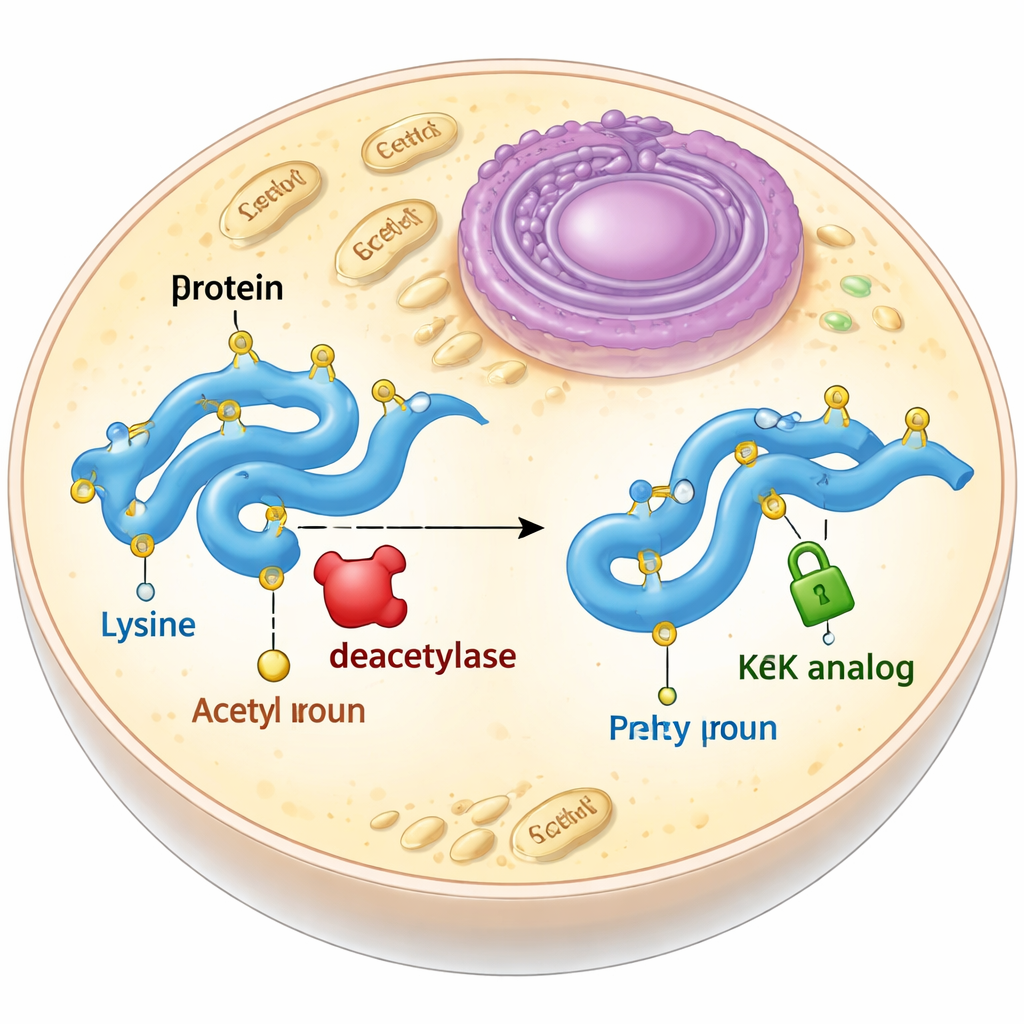
Un substitut stable pour une étiquette fugace
L’acétylation se produit généralement sur un élément constitutif des protéines appelé lysine. Lorsqu’une lysine est acétylée, elle perd sa charge positive et sa chaîne latérale s’allonge légèrement. Les biologistes essaient souvent d’imiter cela en mutant la lysine en un autre acide aminé, la glutamine, qui est neutre mais plus courte, ou en incorporant de la véritable acétyllysine via une extension du code génétique. Les deux approches ont des limites : la glutamine ne reproduit pas entièrement les changements de forme induits par l’acétylation, et la véritable acétyllysine est rapidement retirée par des enzymes appelées désacétylases à l’intérieur des cellules. Les auteurs ont entrepris de concevoir et tester des ressemblants d’acétyllysine qui conservent la bonne taille et la bonne forme mais ne peuvent pas être éliminés.
Tester de nouveaux mimétiques chimiques sur une protéine modèle
L’équipe s’est d’abord concentrée sur l’ubiquitine, une petite protéine bien étudiée qui elle‑même reçoit de nombreuses étiquettes. Grâce à un génie génétique avancé, ils ont placé différentes variantes de lysine en un site de l’ubiquitine : l’acétyllysine naturelle, deux analogues non‑amovibles nommés TFAcK et cétolysine (KeK), et des substituts courants tels que la glutamine, l’alanine et l’arginine. Ils ont ensuite examiné comment ces modifications affectaient la forme et la fonction de l’ubiquitine. Des mesures RMN à haute résolution ont montré que l’acétyllysine, le TFAcK et le KeK produisaient des changements structurels presque identiques, en particulier autour d’une hélice centrale, tandis que la glutamine et d’autres mutations simples ne le faisaient pas. Des tests fonctionnels avec une enzyme appelée HDM2 ont révélé que l’ubiquitine portant l’acétyllysine, le TFAcK ou le KeK se comportait de manière similaire entre elles et différemment de la version glutamine, soulignant que la longueur et le volume de la chaîne latérale — pas seulement sa charge — sont cruciaux.
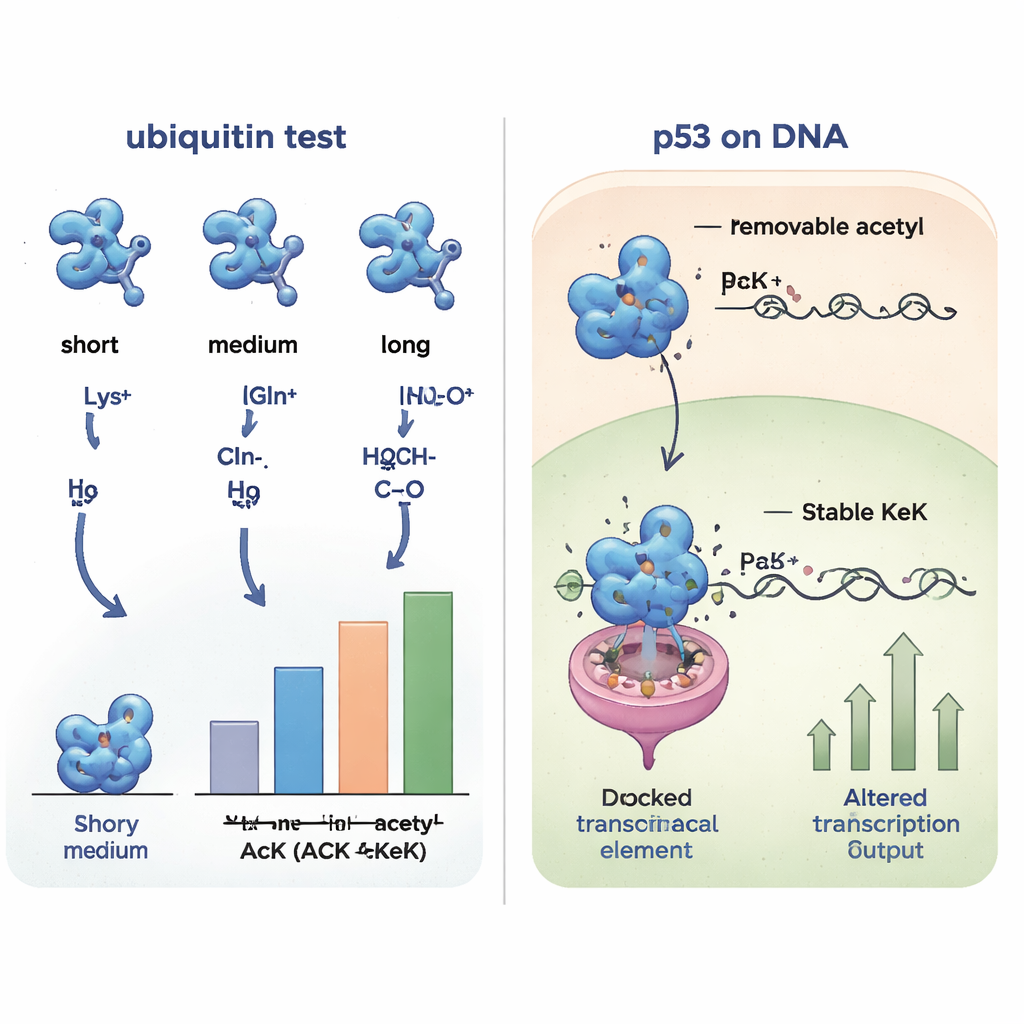
Explorer les partenariats protéiques dans la cellule
Parce que de petits changements structuraux peuvent modifier les partenaires d’interaction d’une protéine, les chercheurs ont comparé ensuite comment les différentes versions d’ubiquitine se liaient à d’autres protéines provenant d’extraits cellulaires humains. En capturant les partenaires d’interaction et en les identifiant par spectrométrie de masse, ils ont constaté que l’ubiquitine contenant l’acétyllysine, le TFAcK ou le KeK partageait des profils d’interaction très similaires, tandis que les formes contenant de la glutamine ou de l’alanine formaient un groupe distinct et différent. Les variantes chargées positivement (lysine ou arginine) formaient encore un autre groupe. Cette comparaison systématique a montré que les analogues non‑amovibles TFAcK et surtout KeK imitent à la fois la structure et le comportement d’interaction de la véritable acétylation bien mieux que la substitution traditionnelle par la glutamine.
Verrouiller l’acétylation du suppresseur de tumeur p53
Pour vérifier si ces outils fonctionnent à l’intérieur de cellules vivantes, les auteurs se sont intéressés à p53, un suppresseur de tumeur clé souvent appelé « gardien du génome ». Des lysines spécifiques dans la région de liaison à l’ADN de p53 peuvent être acétylées, modifiant les gènes qu’il active, tels que ceux qui arrêtent le cycle cellulaire ou déclenchent la mort cellulaire. L’équipe a conçu des cellules humaines pour que p53 incorpore de l’acétyllysine, du TFAcK ou du KeK à deux positions lysine importantes (120 et 164) uniquement lorsque l’acide aminé non standard correspondant était fourni. Les trois pouvaient être incorporés dans p53, mais des mesures détaillées ont montré que, dans les cellules, les groupes acétyl et TFAcK étaient en grande partie retirés par des désacétylases, tandis que le KeK restait intact. Lorsqu’ils ont testé la capacité de p53 à activer un gène rapporteur et le gène naturel p21, les variantes portant KeK à ces sites étaient beaucoup moins actives, ce qui correspond à ce que l’on attend quand l’acétylation à ces positions est verrouillée, tandis que l’acétyllysine et le TFAcK se comportaient davantage comme le p53 normal parce qu’ils avaient été désacéylés.
Ce que cela signifie pour l’étude des décisions cellulaires
Globalement, l’étude montre que le KeK est un substitut fidèle et non‑amovible de l’acétyllysine : il reproduit étroitement les changements structurels, les préférences d’interaction et les conséquences fonctionnelles de l’acétylation, tout en ne pouvant pas être effacé par les enzymes cellulaires. Pour les non‑spécialistes, cela signifie que les chercheurs disposent désormais d’un moyen de « figer » un interrupteur chimique normalement réversible à un site unique d’une protéine, puis d’observer comment cela affecte des processus tels que la régulation génique et les décisions de devenir d’une cellule. Cela devrait grandement faciliter la distinction des rôles spécifiques de l’acétylation par rapport à d’autres modifications qui se chevauchent, et pourrait à terme éclairer la façon dont une acétylation des protéines mal régulée contribue à des maladies comme le cancer.
Citation: Kienle, S.M., Sigg, M., Schneider, T. et al. Non-hydrolyzable acetyllysine analogs to study protein acetylation in vitro and in cells. Nat Commun 17, 1985 (2026). https://doi.org/10.1038/s41467-026-69782-6
Mots-clés: acétylation des protéines, modification post‑tradutionnelle, ubiquitine, p53, extension du code génétique