Clear Sky Science · fr
Remodelage transcriptomique dynamique des cellules progénitrices neurales humaines greffées dévoile des mécanismes de préservation de la vision dans un modèle de rat de la rétinite pigmentaire
Pourquoi il est important de protéger une vision qui s’éteint
La rétinite pigmentaire regroupe des maladies héréditaires qui privent progressivement les personnes de leur vision, souvent en commençant par la cécité nocturne et en évoluant vers une cécité légale. Parce que des centaines de mutations génétiques distinctes peuvent provoquer cette maladie, traiter chacune d’elles par une thérapie génique ciblée est difficile. Cette étude explore une approche plus universelle : transplanter des cellules progénitrices neurales humaines — des cellules nerveuses immatures cultivées en laboratoire — dans l’œil pour protéger les cellules photoréceptrices restantes. Comprendre précisément comment ces cellules greffées se comportent et contribuent à préserver la vision pourrait orienter les traitements futurs, non seulement pour la rétinite pigmentaire, mais aussi pour d’autres maladies causes de cécité.
Favoriser les cellules existantes plutôt que les remplacer
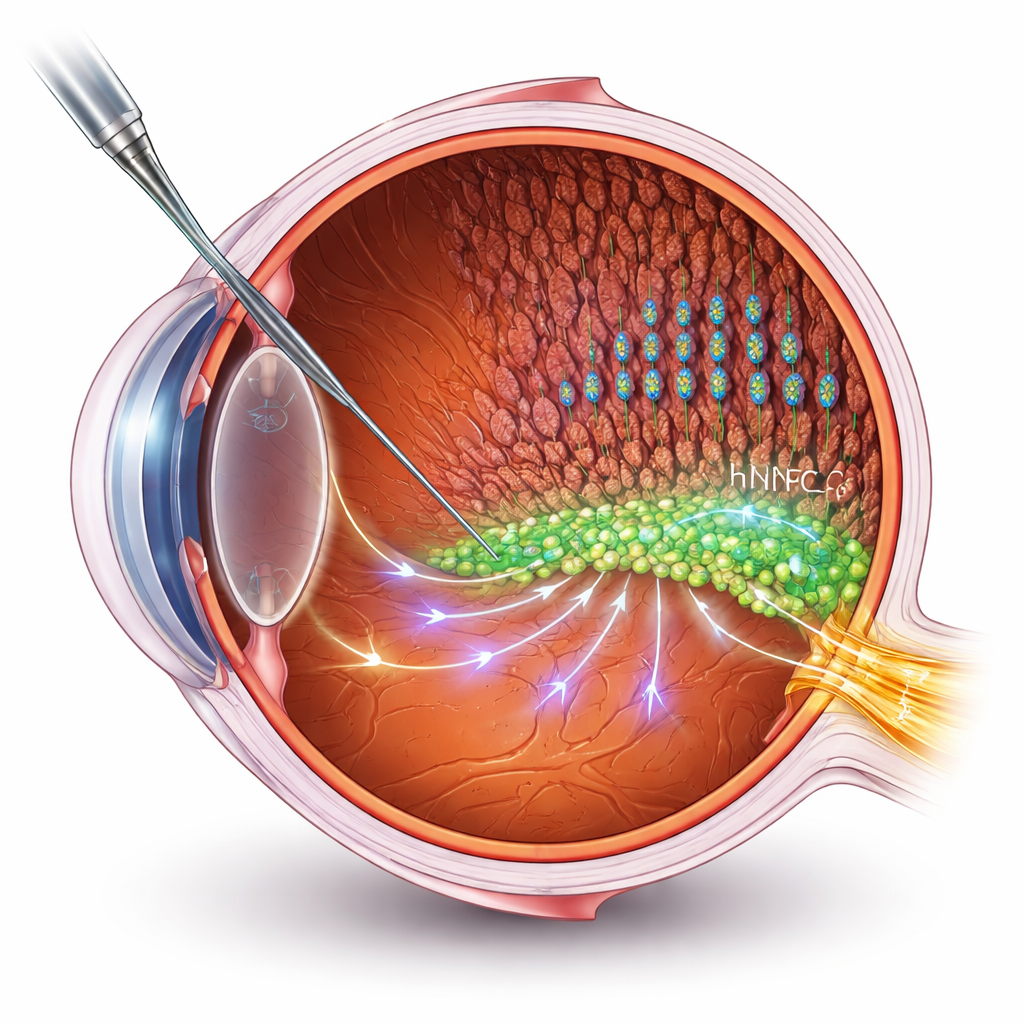
Be nombreuses thérapies à base de cellules souches visent à remplacer des cellules mortes ou endommagées. Mais dans les stades avancés des maladies rétiniennes, recréer de nouvelles connexions vers le cerveau représente un obstacle technique majeur. Ici, les auteurs choisissent une voie différente : utiliser des cellules progénitrices neurales humaines (hNPCs) comme « aides » soutenant les propres cellules rétiniennes du patient. Ils ont transplanté des hNPCs dans l’espace sous-rétinien d’un modèle de rat bien établi de rétinite pigmentaire, puis évalué la vision par enregistrements électriques et tests comportementaux. Les rats traités ont conservé une meilleure fonction visuelle et des couches de photorécepteurs — bâtonnets et cônes — plus intactes que les animaux non traités, bien que la dégénérescence ait continué à progresser lentement.
Comment les cellules greffées évoluent dans un œil malade
Pour examiner ce qui se passe au niveau moléculaire, l’équipe a utilisé le séquençage ARN unicellulaire, une technique qui profile les gènes actifs dans des milliers de cellules individuelles. Ils ont suivi les hNPCs greffées à deux moments distincts, correspondant grossièrement à des phases précoces et plus tardives après la transplantation. Plutôt que de se transformer en nouveaux photorécepteurs, la plupart des cellules transplantées ont mûri en cellules de soutien de type astrocytaire, une plus petite fraction exprimant des marqueurs d’oligodendrocytes ou de neurones immatures. Avec le temps, ces cellules se sont stabilisées, adoptant des caractéristiques suggérant qu’elles sont adaptées à survivre dans un environnement dégénératif stressant et à interagir étroitement avec les cellules rétiniennes voisines.
Signaux protecteurs, métabolisme et nettoyage
Les hNPCs ont produit un mélange riche en protéines protectrices connues sous le nom de facteurs trophiques. Parmi elles figurent MANF et MYDGF, liées à la survie cellulaire, à la réduction du stress oxydatif et à l’atténuation de l’inflammation, ainsi que d’autres facteurs comme la midkine et la pléiotrophine qui soutiennent la croissance et la migration des cellules neurales. Ces molécules semblaient agir à la fois sur la greffe elle-même et sur la rétine environnante. Chez les rats traités, les bâtonnets et les cônes présentaient des profils d’expression génique plus proches des témoins sains, avec un meilleur soutien des voies de signalisation visuelle et de l’entretien cellulaire. Les cellules greffées ont également stimulé des voies impliquées dans l’élimination des débris cellulaires et l’ajustement du métabolisme, suggérant qu’elles aident les photorécepteurs à faire face aux besoins énergétiques et aux sous-produits toxiques qui s’accumulent pendant la maladie.
Apaiser les cellules de soutien et remodeler le voisinage rétinien
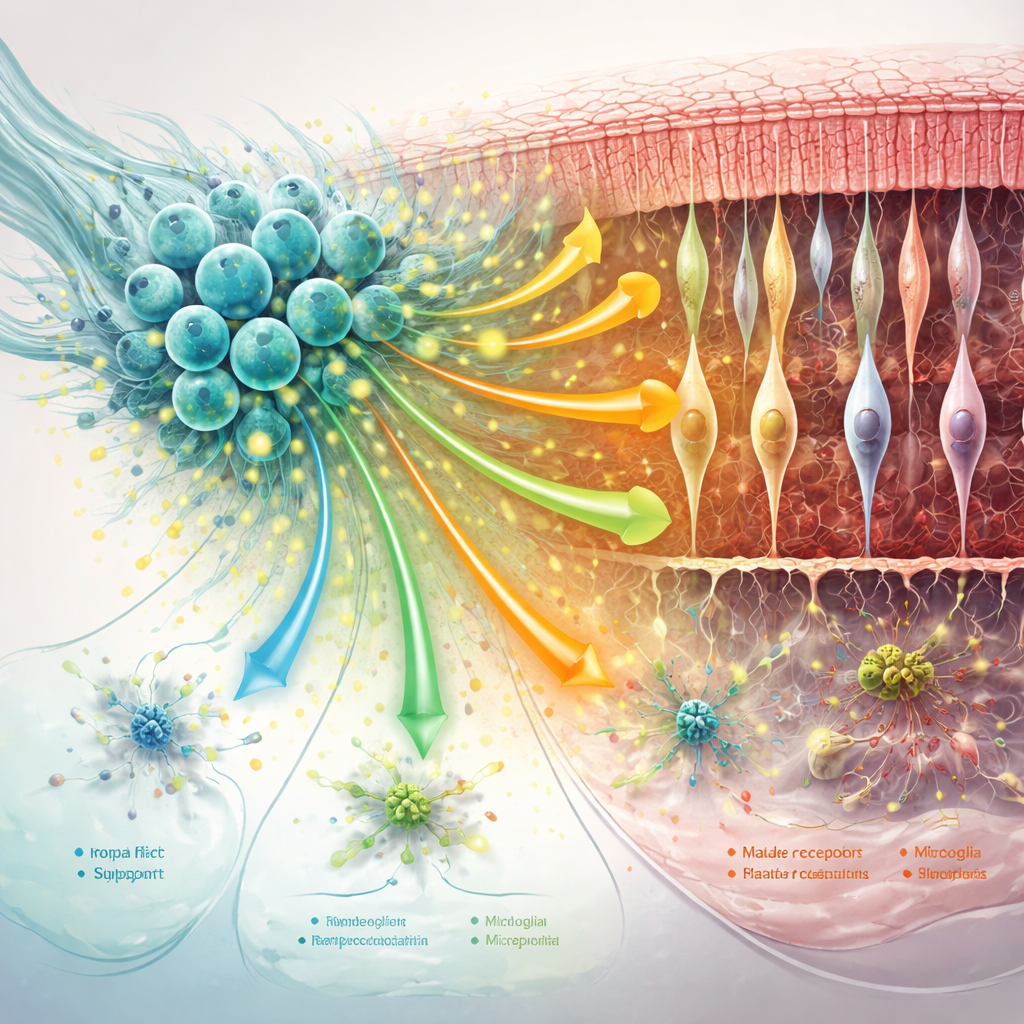
Le réseau de soutien rétinien — glies de Müller, microglie et matrice protéique environnante — joue un rôle important pour aggraver ou ralentir la dégénérescence. L’étude a montré que le traitement par hNPCs a atténué les marqueurs clés des changements « réactifs » nocifs dans les cellules de Müller et a fait basculer la microglie vers des états moins inflammatoires, surtout aux premiers stades. Parallèlement, les signaux de communication favorisant la stabilisation des synapses, l’adhésion cellulaire et le maintien de l’architecture autour des photorécepteurs se sont renforcés. À mesure que la maladie progressait, certains de ces bénéfices se sont estompés : la communication intercellulaire globale s’est affaiblie, certaines voies protectrices — y compris la signalisation liée à MANF — ont diminué, et les cellules de soutien ont adopté des profils plus axés sur le stress et l’activité immunitaire.
Ce que cela signifie pour les thérapies oculaires futures
Pour un non-spécialiste, le message principal est que les cellules progénitrices neurales humaines greffées peuvent agir comme des « premiers répondants » locaux dans une rétine en dégénérescence. Elles ne reconstruisent pas la rétine de zéro, mais elles libèrent des molécules protectrices, ajustent le métabolisme, calment l’inflammation dommageable et contribuent à maintenir la structure locale, ce qui ralentit la perte de vision. Cependant, cet effet protecteur diminue avec le temps à mesure que l’environnement devient plus hostile et que le dialogue entre greffe et cellules hôtes s’affaiblit. Les auteurs suggèrent qu’augmenter des facteurs clés tels que MANF et améliorer la santé de la rétine hôte — éventuellement par ingénierie génétique de la greffe ou par traitements combinés — pourrait être essentiel pour transformer ce répit temporaire en une préservation durable de la vue.
Citation: Shahin, S., Bell, S., Lu, B. et al. Dynamic transcriptomic remodeling in grafted human neural progenitor cells uncovers mechanisms for vision preservation in a rat model of retinitis pigmentosa. Nat Commun 17, 2164 (2026). https://doi.org/10.1038/s41467-026-69776-4
Mots-clés: rétinite pigmentaire, thérapie par cellules souches, dégénérescence rétinienne, neuroprotection, séquençage ARN unicellulaire