Clear Sky Science · fr
Limites du clonage en série chez les mammifères
Pourquoi copier des mammifères n’est pas aussi simple qu’on le croit
Pendant des décennies, l’idée de reproduire des animaux à l’identique — jusqu’à leur ADN — a fasciné le public, de la brebis Dolly aux rêves de ressusciter des espèces disparues. Mais les mammifères peuvent-ils réellement se maintenir uniquement par clonage, génération après génération, comme le font certaines plantes et animaux simples ? Cette étude a suivi une lignée de souris produite entièrement par clonage sur près de 20 ans pour répondre à cette question. Les résultats expliquent pourquoi, malgré nos progrès techniques, la nature dépend toujours largement de la reproduction sexuée pour préserver la santé des mammifères à long terme.
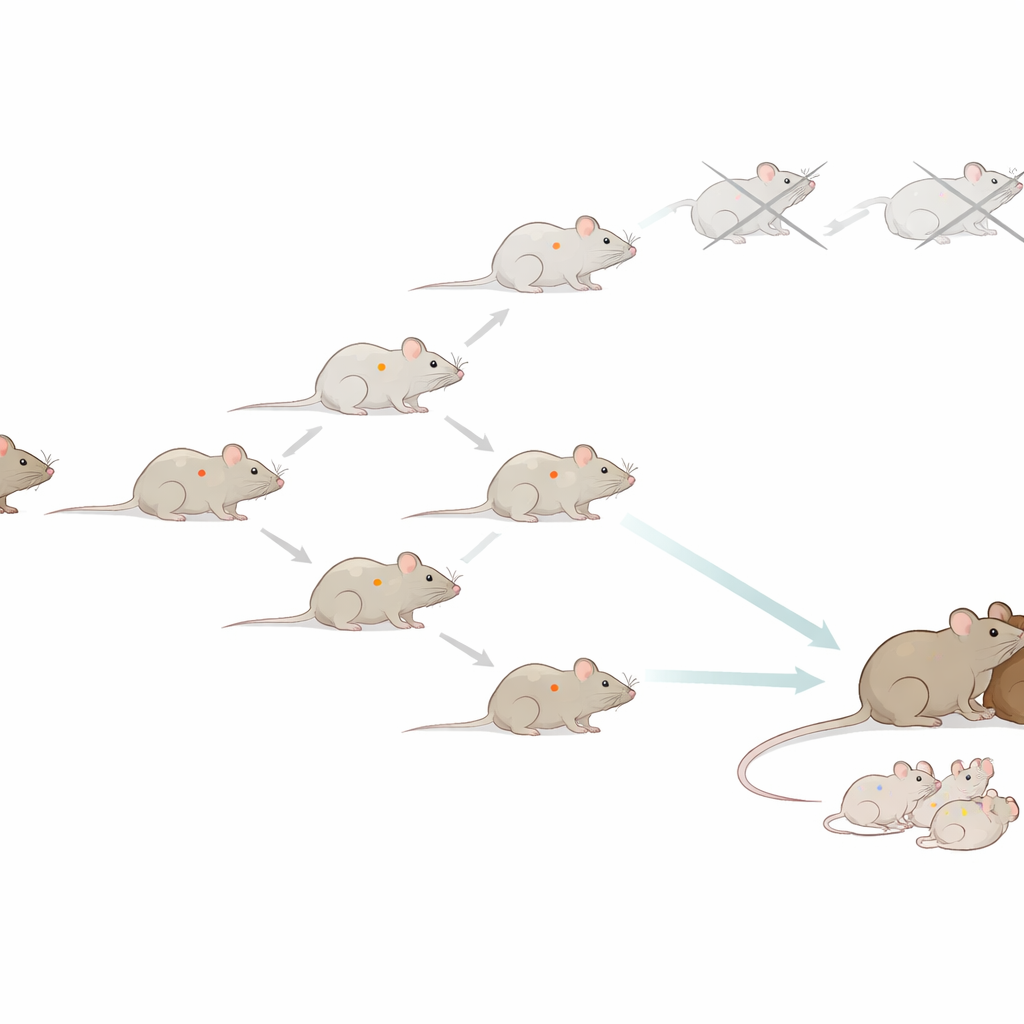
Suivre une lignée de souris pendant vingt ans
Les chercheurs ont commencé avec une seule souris femelle et ont utilisé ses cellules somatiques pour créer une souris clonée. Une fois ce premier clone arrivé à maturité, ils ont prélevé des cellules sur celui-ci pour fabriquer le clone suivant, et ont répété ce processus encore et encore. Au total, ils ont tenté plus de 30 000 procédures de transfert nucléaire et produit plus de 1 200 animaux clonés, atteignant 58 générations à partir du donneur initial. Beaucoup de ces souris ressemblaient à des animaux ordinaires et se comportaient comme tels, avec des durées de vie normales d’environ deux ans et des poids corporels similaires. Au début, le taux de réussite du clonage s’est même amélioré d’une génération à l’autre, laissant penser que le clonage en série des mammifères pourrait être viable sur le long terme.
Des corps sains, mais des dégâts cachés
En apparence, les souris clonées semblaient en bonne santé. Leurs organes internes et en particulier leurs placentas présentaient les bizarreries habituelles observées dans les expériences de clonage, comme une taille supérieure à celle des souris conçues naturellement, mais ces anomalies ne s’aggravaient pas d’une génération à l’autre. L’équipe a aussi évalué le développement des embryons en laboratoire et examiné les motifs des marques chimiques sur les protéines d’emballage de l’ADN — des éléments qui dysfonctionnent souvent dans le clonage. Les embryons précoces issus des clones de générations tardives ressemblaient beaucoup à ceux de la première génération clonée. Cela suggérait que les problèmes connus de « reprogrammation » liés au clonage ne s’accumulaient pas progressivement dans le temps.
Les mutations s’insinuent à chaque copie
La véritable histoire est apparue lorsque les scientifiques ont séquencé les génomes de souris issues de différentes générations de clonage. À chaque cycle de copie, de nouvelles altérations de l’ADN sont apparues : en moyenne environ 70 mutations ponctuelles et une à deux altérations structurelles par génération, incluant de grandes réarrangements et des pertes de chromosomes. Beaucoup de ces changements ressemblaient aux mutations naturelles observées lors de la reproduction ordinaire, mais la différence clé est que, dans le clonage, il n’y a pas de brassage des chromosomes par l’accouplement pour aider à éliminer les variantes nuisibles. Au fil du temps, notamment après environ la 25e génération, des mutations délétères — telles que la perte d’un chromosome X entier ou des cassures et échanges entre chromosomes — ont commencé à s’accumuler. La proportion de mutations susceptibles de perturber des gènes importants a presque doublé dans les générations ultérieures.
Les ovules révèlent le point de rupture
Pour voir comment ces dégâts cachés affectaient la reproduction, l’équipe s’est concentrée sur les ovules de femelles clonées de générations tardives. Lorsqu’on a déclenché le développement de ces ovules sans spermatozoïde, presque aucun n’a donné d’embryon précoce viable, indiquant que beaucoup portaient des combinaisons létales de mutations. La fécondation avec des spermatozoïdes de mâles normaux a amélioré le développement dans une certaine mesure, mais le succès chuta fortement dans les générations avancées. Des expériences qui ont échangé les noyaux et le cytoplasme entre ovules de souris normales et de clones tardifs ont montré que tant le matériel génétique que le cytoplasme de l’ovule étaient compromis. Finalement, à la 58e génération, tous les descendants clonés sont morts peu après la naissance et la lignée clonale n’a pas pu se poursuivre.
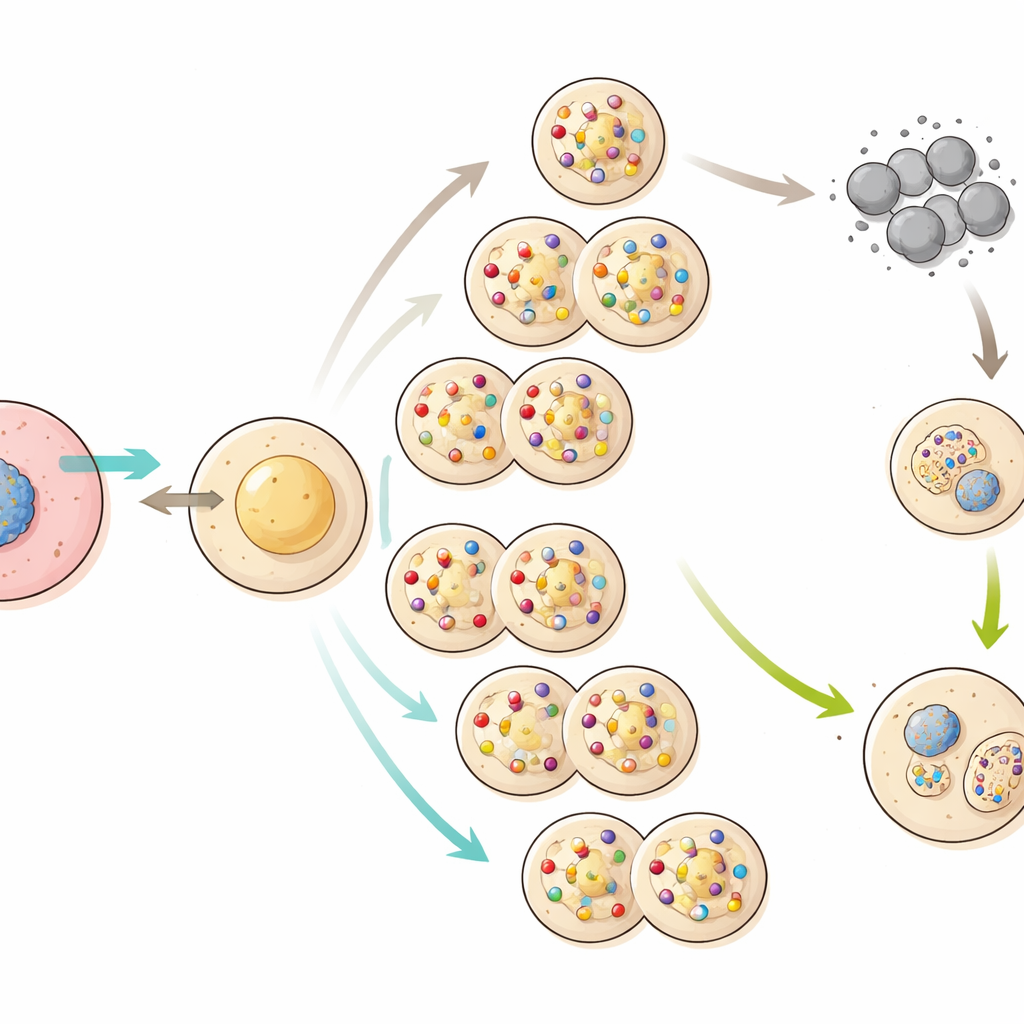
La reproduction sexuée comme système de réparation
Lorsque les scientifiques ont laissé les souris clonées de générations tardives s’accoupler naturellement avec des mâles normaux, un schéma différent est apparu. Bien que ces mères clonées aient eu des portées réduites, certains de leurs descendants — et en particulier leurs petits-enfants — étaient bien plus sains. Les placentas de la génération suivante ont diminué pour revenir vers des tailles normales et le développement s’est globalement amélioré. Cela suggère que le mélange et le tri des chromosomes lors de la formation des ovules et des spermatozoïdes, suivis par la fécondation, peuvent dissocier les combinaisons de mutations délétères et éliminer beaucoup des pires altérations. Autrement dit, le sexe a agi comme un système de nettoyage intégré dont le clonage pur est dépourvu.
Quelles implications pour l’avenir du clonage
En suivant soigneusement une seule lignée clonée de souris sur 57 générations réussies, ce travail montre que les mammifères ne peuvent pas compter uniquement sur le clonage pour maintenir une lignée indéfiniment. Une santé apparente et des durées de vie normales peuvent masquer un déclin génétique lent, les mutations s’accumulant silencieusement jusqu’à l’échec de la reproduction. Si le clonage reste un outil puissant — pour sauver des espèces menacées, multiplier des animaux d’élevage précieux ou préserver des ressources génétiques — il est peu probable qu’il remplace la reproduction sexuée comme stratégie à long terme pour la survie des mammifères. L’étude fournit un solide soutien expérimental à l’idée que, chez les animaux complexes, la sexualité n’est pas seulement une façon de produire des descendants : elle est un entretien essentiel du génome.
Citation: Wakayama, S., Ito, D., Inoue, R. et al. Limitations of serial cloning in mammals. Nat Commun 17, 2495 (2026). https://doi.org/10.1038/s41467-026-69765-7
Mots-clés: clonage animal, mutations génétiques, reproduction des souris, reproduction asexuée, évolution du sexe