Clear Sky Science · fr
TCL1A médie les défauts de méthylation de l’ADN dans la môle hydatiforme récidivante avec variantes pathogéniques de NLRP7
Pourquoi c’est important pour la santé des femmes
Certaines grossesses dérapent très tôt et se transforment en une masse de tissu placentaire anormal au lieu d’un fœtus en développement. Cette affection, appelée môle hydatiforme, peut récidiver chez certaines femmes et évoluer parfois vers un cancer. Cette étude explore l’une des principales causes génétiques de ces grossesses rares mais graves et révèle comment une seule protection défaillante dans l’ovocyte peut perturber les « étiquettes » chimiques qui orientent un développement sain.
Un problème de grossesse qui prend racine dans l’ovocyte
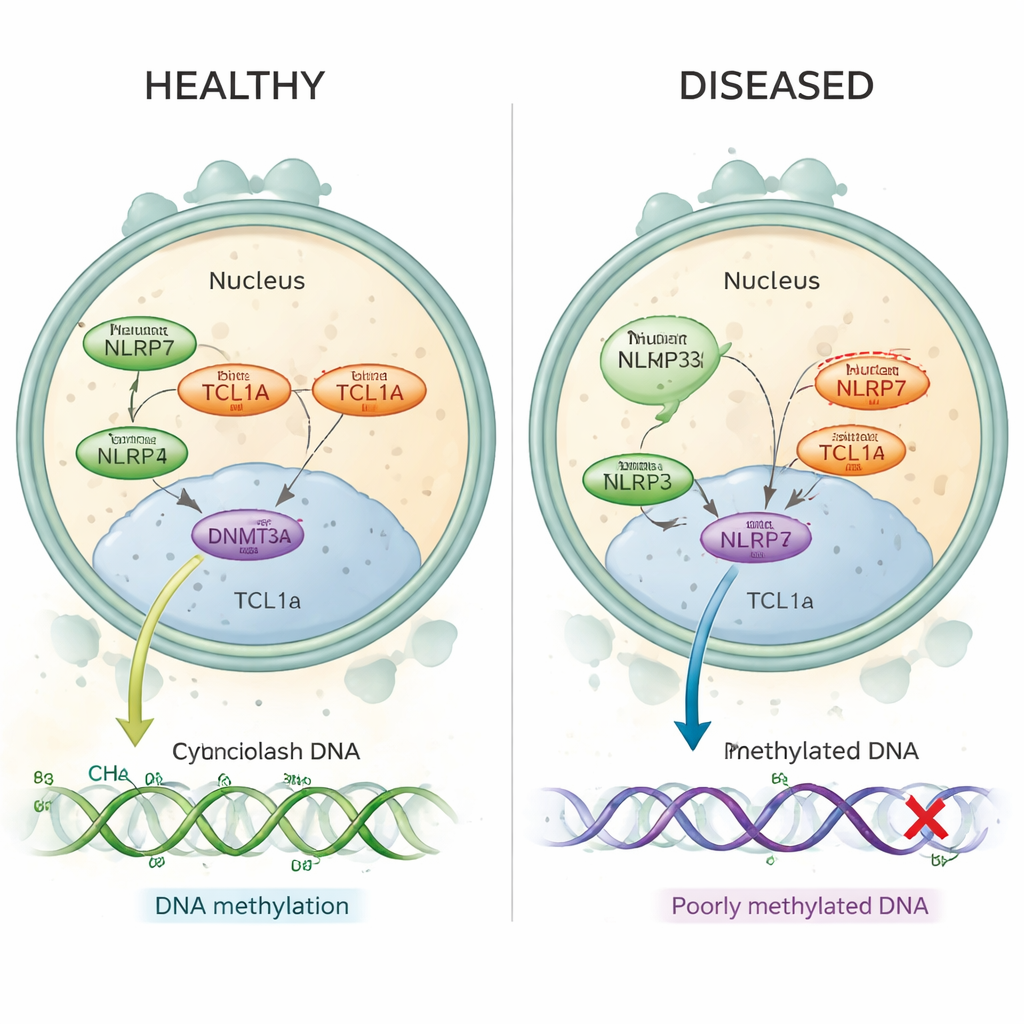
La môle hydatiforme récidivante est un trouble dans lequel des femmes subissent des grossesses molaires répétées, souvent sans aucune grossesse normale entre‑temps. De nombreux cas sont aujourd’hui attribués à des altérations délétères d’un gène appelé NLRP7, qui est actif dans l’ovocyte avant et juste après la fécondation. Chez ces femmes, des régions clés de l’ADN qui devraient porter des « empreintes » maternelles sont dépourvues des marques de méthylation normales — de petits tags chimiques qui aident à activer ou réprimer les gènes au bon moment. Jusqu’à présent, les chercheurs ne comprenaient pas comment une protéine située dans le cytoplasme de l’ovocyte, comme NLRP7, pouvait contrôler la méthylation qui se produit sur l’ADN compacté dans le noyau.
À la recherche d’un partenaire manquant
Pour résoudre ce mystère, les chercheurs ont examiné des ovocytes humains et des embryons très précoces jetés par des cliniques de fertilité. Ils ont isolé NLRP7 et ses partenaires connus dans ces cellules et identifié d’autres protéines qui s’y associent. Une a été particulièrement marquante : TCL1A, déjà connue dans les cancers du sang comme une protéine capable de se déplacer vers le noyau et d’interférer avec des enzymes de méthylation de l’ADN appelées DNMT3A et DNMT3B. TCL1A est anormalement abondante dans les ovocytes humains, ce qui suggère qu’elle y joue un rôle important. Des tests d’interaction détaillés ont montré que TCL1A se lie fortement et spécifiquement à NLRP7, mais pas à des protéines étroitement apparentées, et que ce complexe s’intègre dans une structure spécifique de l’ovocyte appelée complexe maternel sous‑cortical.
Voir l’étreinte moléculaire
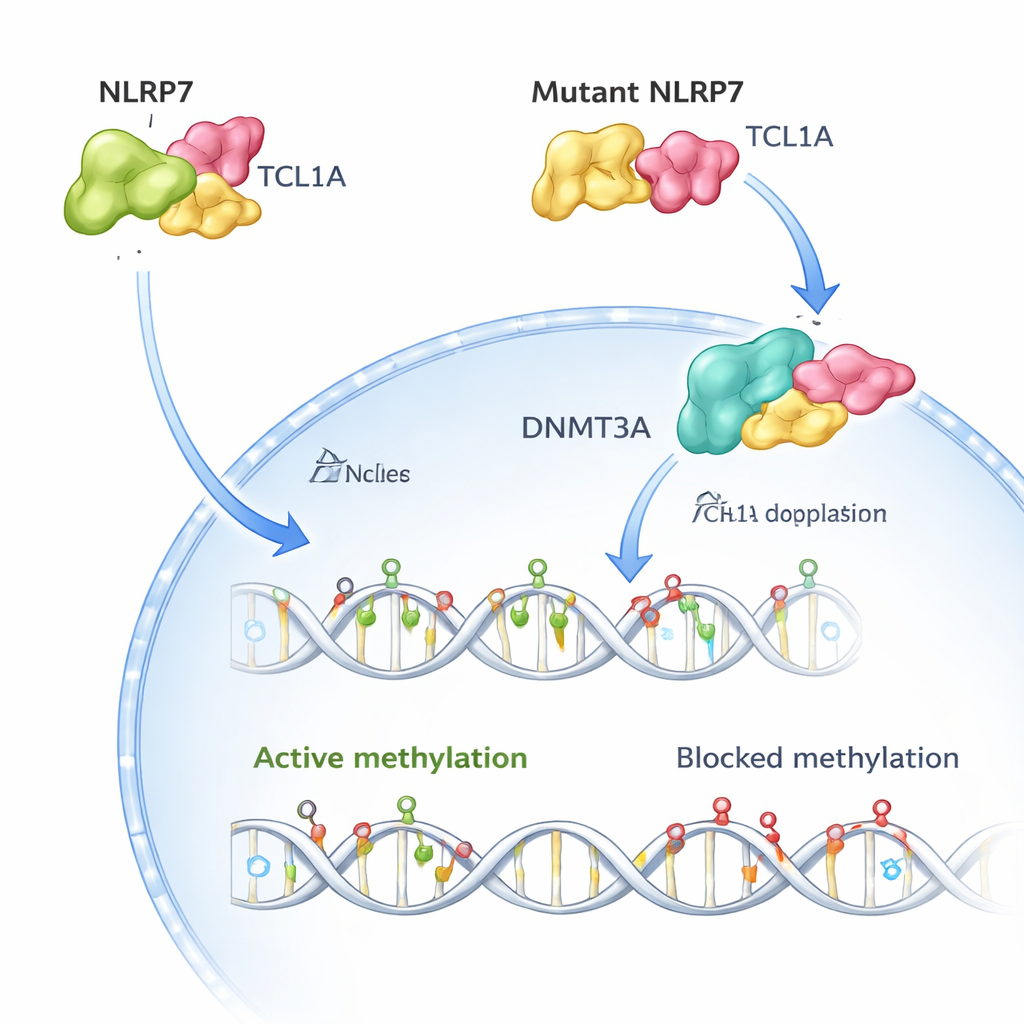
L’équipe a ensuite utilisé la cryo‑microscopie électronique pour visualiser la structure tridimensionnelle du complexe NLRP7–TCL1A. Ils ont constaté que deux molécules de NLRP7 se jumellent et que chacune saisit un dimère de TCL1A le long d’une surface courbe formée de motifs répétés. Cette organisation explique pourquoi de nombreuses altérations causant la maladie dans NLRP7 se regroupent le long de cette surface : modifier des points de contact clés affaiblit ou détruit l’étreinte avec TCL1A. Lorsque les chercheurs ont reproduit plus de 50 variantes connues de patients dans des cellules, la plupart des versions associées aux grossesses molaires récidivantes déstabilisaient NLRP7 ou réduisaient fortement sa capacité à lier TCL1A.
Comment des protéines mal placées perturbent les marques ADN
Dans les ovocytes humains sains, NLRP7 et TCL1A se trouvent principalement dans le cytoplasme, avec seulement une faible quantité de TCL1A atteignant le noyau. Les auteurs montrent que NLRP7 agit comme un garde‑barrière : lorsqu’il peut retenir TCL1A, celle‑ci reste hors du noyau. Quand NLRP7 est muté et ne peut plus bien se lier, TCL1A s’infiltre dans le noyau. Là, elle s’attache à DNMT3A, l’enzyme principale qui pose de nouvelles marques de méthylation dans les ovocytes, et atténue son activité. Dans des modèles de cellules souches qui gagnent normalement en méthylation en mûrissant, la surexpression de TCL1A provoque une perte spectaculaire de méthylation sur l’ensemble du génome, tandis que l’expression conjointe de NLRP7 corrige partiellement ce défaut. Ensemble, ces résultats soutiennent un schéma simple : NLRP7 normal maintient un « frein » de la méthylation (TCL1A) enfermé dans le cytoplasme afin que DNMT3A puisse correctement marquer l’ADN ; NLRP7 défaillant laisse ce frein pénétrer dans le noyau et bloquer le processus.
Du mécanisme au diagnostic
Au‑delà de l’explication des causes des grossesses molaires récidivantes, l’étude suggère une méthode pratique pour juger si une nouvelle variation de NLRP7 identifiée chez une patiente est réellement dommageable. Les auteurs comparent trois approches — des tests en laboratoire de liaison NLRP7–TCL1A, des prédictions informatiques et des outils génétiques standards — et montrent que la perte de liaison à TCL1A s’aligne étroitement avec les variantes pathogènes. Ils identifient aussi une variante délétère jusque‑là méconnue, L766R, dans des familles atteintes de môle récidivante, confirmant qu’elle affaiblit la protéine et dirige TCL1A vers le noyau.
Ce que cela signifie en termes simples
Ce travail révèle une réaction en chaîne moléculaire à l’origine d’un trouble de grossesse rare mais dévastateur. En substance, les ovocytes des femmes concernées portent une protéine « garde du corps » défectueuse, NLRP7, qui ne parvient pas à empêcher son partenaire TCL1A de pénétrer dans le noyau. Une fois à l’intérieur, TCL1A interfère avec l’enzyme qui écrit des tags chimiques vitaux sur l’ADN. Sans ces marques, le placenta précoce se développe anormalement et un embryon ne peut pas se former. En retraçant cette voie étape par étape, l’étude clarifie pourquoi certaines variations génétiques maternelles peuvent saboter à répétition des grossesses et ouvre la voie à un conseil génétique et un diagnostic plus précis pour les femmes atteintes de môle hydatiforme récidivante.
Citation: Gao, Z., Liu, Q., Li, L. et al. TCL1A mediates DNA methylation defects in recurrent hydatidiform mole with NLRP7 pathogenic variants. Nat Commun 17, 2160 (2026). https://doi.org/10.1038/s41467-026-69744-y
Mots-clés: méthylation de l’ADN, môle hydatiforme récidivante, NLRP7, TCL1A, empreinte génomique