Clear Sky Science · fr
GCN5 stimule la progression de la MASLD via la voie de signalisation LXRα/SREBP1c médiant la lipogenèse de novo
Pourquoi cette histoire de foie compte
La stéatose hépatique associée à un dysfonctionnement métabolique (MASLD), anciennement appelée maladie du foie gras non alcoolique, touche désormais environ une personne sur quatre dans le monde. Elle évolue souvent de façon silencieuse, mais peut conduire à la fibrose, au cancer du foie et à des troubles métaboliques graves. Cette étude révèle un « bouton de volume » moléculaire qui favorise l’accumulation nocive de graisses dans le foie et montre comment le réduire pourrait à la fois protéger le foie et rendre potentiellement plus sûres certaines stratégies médicamenteuses utilisées contre les maladies cardiaques.
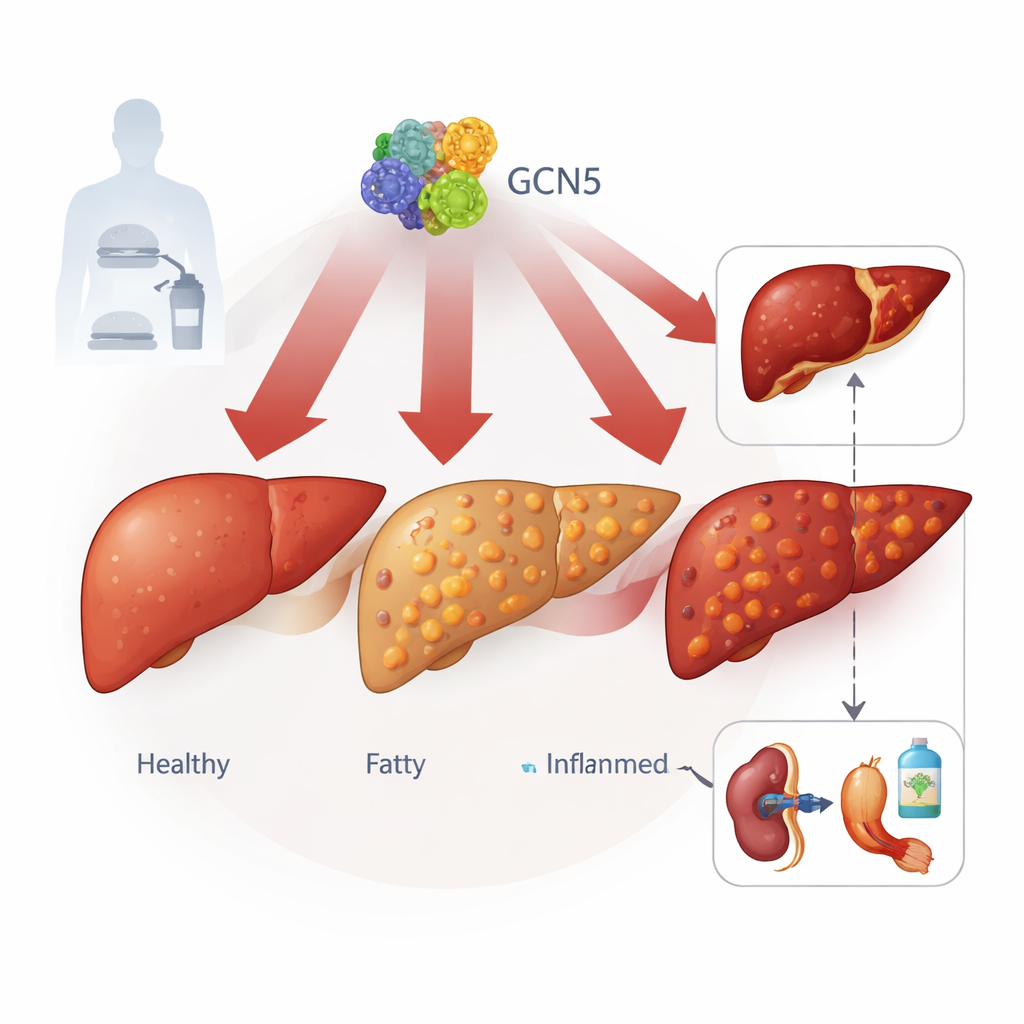
Un interrupteur caché à l’intérieur des cellules hépatiques
Les auteurs se concentrent sur une protéine nommée GCN5, surtout connue comme régulateur du compactage de l’ADN. En étudiant des tissus hépatiques provenant de plus de 100 personnes, allant de sujets sains à des cas sévères de MASLD, et plusieurs modèles murins de foie gras induit par l’alimentation, ils ont constaté que les niveaux de GCN5 dans les cellules du foie augmentent régulièrement à mesure que la maladie s’aggrave. Une protéine étroitement apparentée, PCAF, n’a pas montré ce schéma, ce qui suggère que GCN5 joue un rôle particulier. Un fort GCN5 corrélait avec plus de graisse hépatique, des lipides sanguins plus élevés et des signes accrus de lésion hépatique, reliant cet interrupteur moléculaire à la sévérité clinique de la maladie.
Augmenter ou diminuer GCN5 chez les animaux
Pour tester la causalité, l’équipe a augmenté ou supprimé génétiquement GCN5 spécifiquement dans les cellules hépatiques de souris. Quand GCN5 était surexprimé, les souris nourries avec un régime riche en graisses développaient des foies plus lourds et plus gras, des lipides sanguins plus élevés et davantage de lésions hépatiques, bien qu’elles ne mangeassent pas plus et ne gagnassent pas de poids corporel supplémentaire. Des hépatocytes cultivés en laboratoire ont montré un comportement similaire : un excès de GCN5 entraînait des gouttelettes lipidiques plus grandes et plus nombreuses. En revanche, des souris dépourvues de GCN5 uniquement dans leurs cellules hépatiques étaient fortement protégées. Dans plusieurs modèles alimentaires mimant la MASLD humaine et sa forme inflammatoire plus sévère, ces animaux accumulaient moins de gras hépatique, présentaient des lipides sanguins et des enzymes hépatiques plus bas, et développaient moins d’inflammation et de fibrose.
Comment GCN5 pousse le foie à fabriquer des graisses
En explorant le métabolisme, les chercheurs ont mesuré de nombreux acides gras et leurs précurseurs dans le foie. La perte de GCN5 réduisait principalement les lipides que le foie synthétise à partir de zéro, un processus appelé lipogenèse de novo, tout en laissant relativement inchangés les acides gras polyinsaturés d’origine alimentaire. Des expériences d’expression génique et de marquage isotopique ont montré que GCN5 se situe en amont d’un régulateur maître de la synthèse lipidique nommé SREBP1c. Lorsque GCN5 était actif, les gènes impliqués dans la synthèse et la modification des acides gras étaient activés et le taux de fabrication de lipides internes du foie augmentait. Supprimer ou inhiber GCN5 abaissait ce programme, réduisant le flux de carbone issu du sucre vers les nouveaux lipides hépatiques.
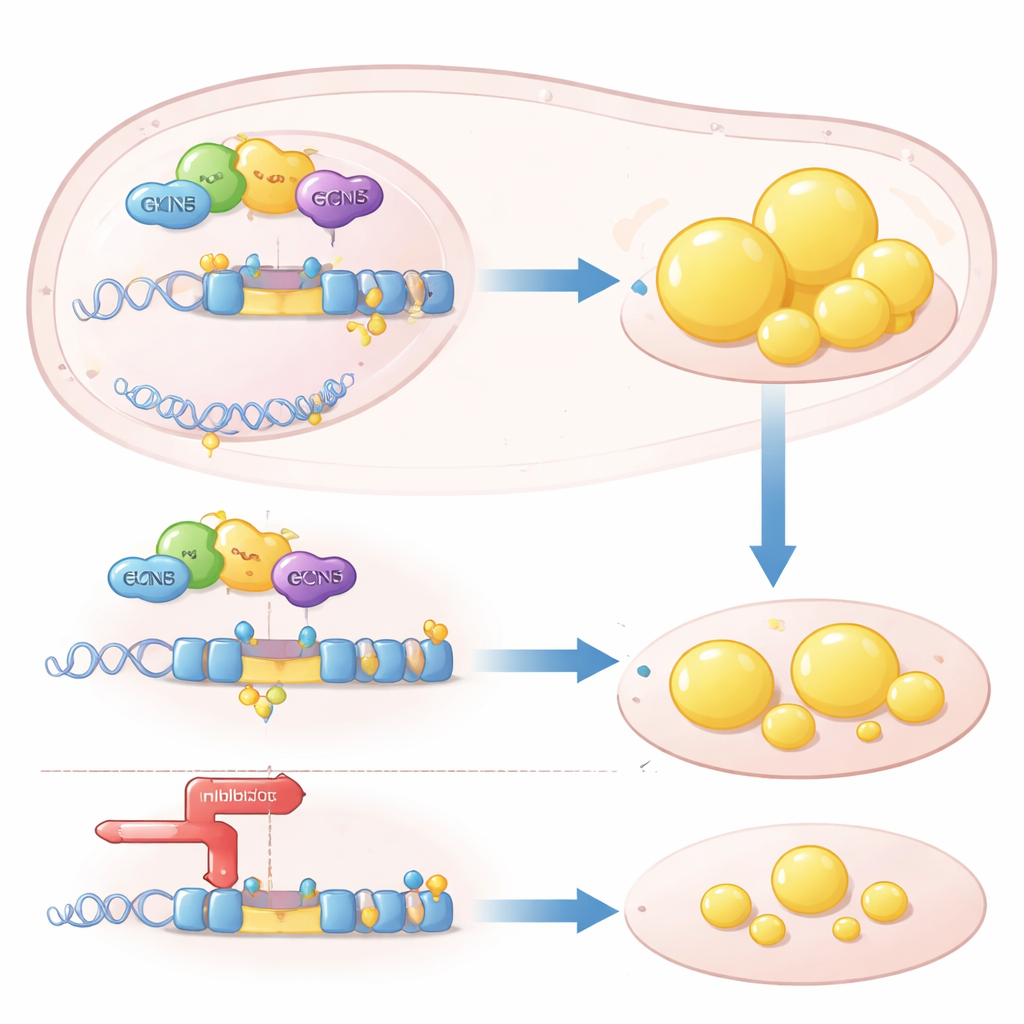
Un levier épigénétique sur un gène clé des lipides
Sur le plan mécanistique, GCN5 agit comme un levier « épigénétique » : il modifie chimiquement les protéines histones liées à l’ADN pour rendre certains gènes plus faciles à transcrire. Les auteurs ont montré que GCN5 est recruté dans la région régulatrice du gène SREBP1c en coopération avec un récepteur nucléaire nommé LXRα, qui détecte des molécules liées au cholestérol. Une fois présent, GCN5 ajoute des marques d’acétylation sur l’histone H3, assouplissant la chromatine locale et renforçant la transcription de SREBP1c. Cet effet était très sélectif : GCN5 renforçait la capacité de LXRα à activer SREBP1c mais pas une autre cible de LXR, ABCA1, qui aide à éliminer le cholestérol des tissus. En l’absence de GCN5, LXRα ne pouvait plus engager efficacement le promoteur de SREBP1c, et le programme de synthèse lipidique en aval s’enrayer.
Un candidat médicament et une combinaison prometteuse
L’équipe a ensuite testé CPTH2, un petit inhibiteur moléculaire de GCN5 qui se concentre dans le foie. Dans des modèles murins soumis à des régimes riches en lipides, CPTH2 a réduit la taille du foie, la teneur en graisses et les marqueurs de lésion sans toxicité apparente ni modification de la prise alimentaire. Dans des cellules hépatiques humaines et murines cultivées, CPTH2 diminuait les gouttelettes lipidiques et les triglycérides seulement lorsque GCN5 était présent, confirmant la spécificité de son action. Fait important, chez les cellules et les souris traitées par des composés activateurs de LXR (conçus pour améliorer l’élimination du cholestérol et lutter contre l’athérosclérose), CPTH2 bloquait sélectivement l’augmentation indésirable de la production de lipides pilotée par SREBP1c tout en préservant les gènes favorisant le transport inverse du cholestérol. Combiné à un agoniste de LXR chez des souris nourries avec un régime riche en graisses, CPTH2 a en outre abaissé les lipides sanguins nocifs et le cholestérol hépatique et a empêché l’accumulation supplémentaire de graisse dans le foie.
Ce que cela signifie pour les patients
Cette étude place GCN5 comme un moteur central de l’accumulation de graisses hépatiques dans la MASLD en reliant les signaux alimentaires et hormonaux au commutateur de production lipidique SREBP1c. Parce que GCN5 semble dispensable pour le volet bénéfique d’épuration du cholestérol de la signalisation LXR, des médicaments qui inhibent GCN5 — tels que CPTH2 ou des dérivés plus avancés — pourraient maîtriser la stéatose et l’inflammation hépatiques tout en laissant agir les thérapies protectrices pour le cœur. Pour les personnes à risque à la fois de maladie du foie gras et de maladies cardiovasculaires, cibler cet interrupteur épigénétique pourrait un jour offrir un moyen de protéger le foie sans sacrifier les bienfaits d’une meilleure gestion du cholestérol.
Citation: Xiao, HT., Song, P., Jin, J. et al. GCN5 drives MASLD progression through LXRα/SREBP1c signaling pathway–mediated de novo lipogenesis. Nat Commun 17, 2821 (2026). https://doi.org/10.1038/s41467-026-69736-y
Mots-clés: maladie du foie gras, épigénétique, métabolisme des lipides, métabolisme hépatique, récepteurs nucléaires