Clear Sky Science · fr
Contrôle non‑chélation dans les allylations des cétones α‑oxy grâce aux allylatranes du groupe 14
Façonner les molécules avec une précision accrue
De nombreux médicaments et produits naturels ne sont actifs que lorsque leurs atomes sont arrangés dans une forme tridimensionnelle précise. Les chimistes consacrent donc d’importants efforts à apprendre comment « pousser » de nouvelles pièces sur une molécule d’un côté ou de l’autre. Cet article décrit une nouvelle façon d’introduire des groupes allyle — courtes chaînes de trois carbones — sur une classe courante de molécules, ouvrant l’accès à des structures images‑miroir qui étaient jusqu’ici très difficiles à obtenir.
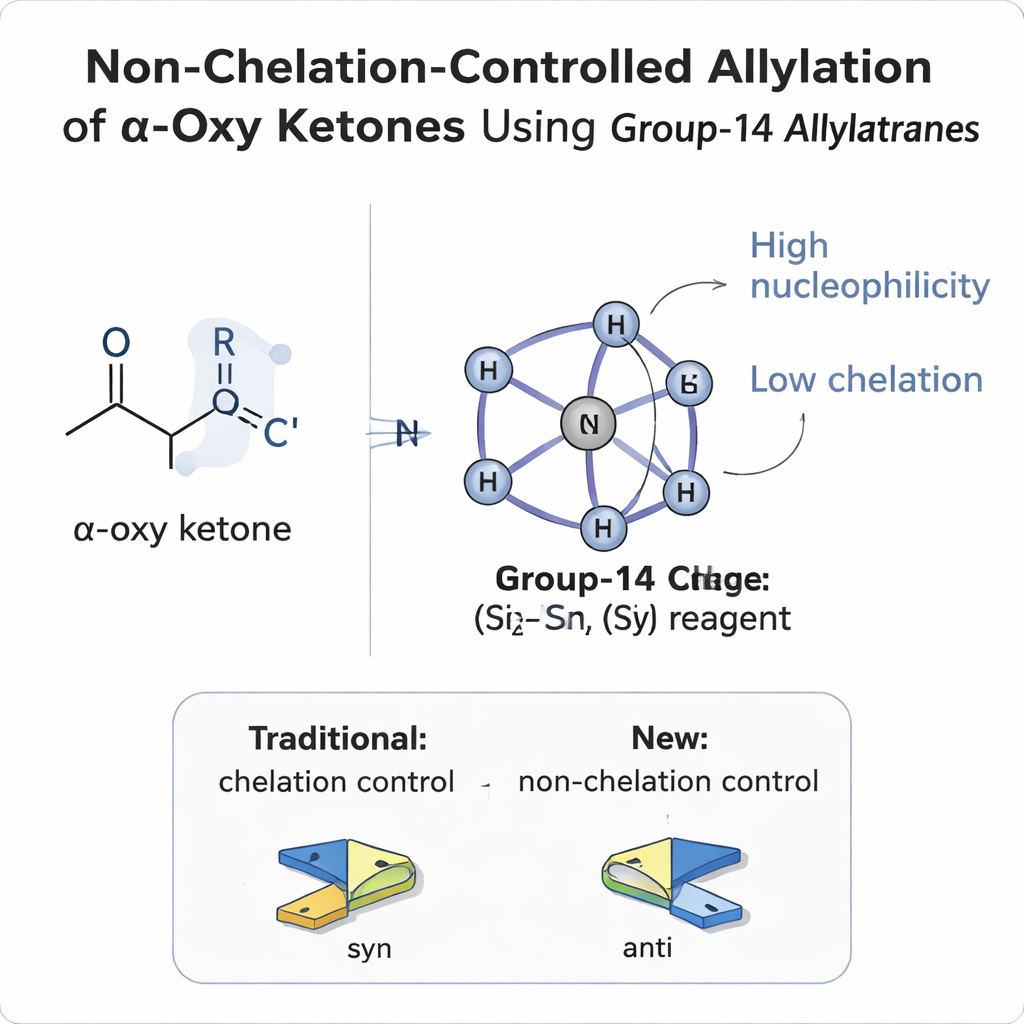
Pourquoi il est si difficile de contrôler les faces d’une molécule
Quand un nouveau groupe se fixe sur une liaison carbone‑oxygène plane (une carbonyle), il peut attaquer de l’une ou l’autre face, un peu comme une balle frappant une pièce de monnaie par le dessus ou par le dessous. Si un substituant voisin est déjà présent au carbone adjacent (la position α), le résultat est deux produits tridimensionnels possibles, appelés diastéréomères. Pendant des décennies, les chimistes ont utilisé des modèles simples — Felkin–Anh, Felkin–Anh polaire, Cram et modèles de chélation — pour prédire quel côté un réactif privilégiera. Dans les composés carbonylés α‑oxy, où le substituant voisin contient de l’oxygène (tel qu’un éther ou un ester), l’oxygène agit généralement comme une pince qui s’accroche aux réactifs métalliques. Cette « chélation » verrouille la molécule dans une conformation et conduit presque toujours à des produits dits syn, où les groupes alcool nouvellement formés se retrouvent du même côté de la chaîne carbonée.
Le problème ancien des voisins oxygénés
Si la voie par chélation est très utile, elle est aussi limitante : elle biaise fortement les réactions vers les produits syn et rend très difficile l’obtention de l’arrangement opposé, anti, où les deux groupes alcool pointent de côtés opposés. Pour les aldéhydes α‑oxy — molécules dont le carbone carbonyle porte au moins un hydrogène — quelques astuces astucieuses utilisant des réactifs silicones spéciaux et des acides de Lewis soigneusement choisis ont permis d’obtenir des produits anti. Mais pour les cétones α‑oxy, moins réactives et plus fréquentes dans les cibles complexes, le défi est plus important. Les nucléophiles plus forts tendent à être plus acides de Lewis, ce qui favorise précisément la chélation que le chimiste cherche à éviter. Ainsi, trouver l’équilibre entre « suffisamment réactif » et « pas trop collant » vis‑à‑vis de l’oxygène a été un problème central non résolu.
Un réactif en forme de cage qui rompt la règle
Les auteurs présentent une nouvelle famille de réactifs appelés allylatranes, centrés sur des éléments du groupe 14 — silicium, germanium et étain — maintenus dans une structure rigide en forme de cage. Dans ces molécules, un atome d’azote interne s’étend à travers la cage pour se lier à l’atome central, créant un centre métallique fortement coordonné, presque encapsulé. Cette conception produit deux effets cruciaux. D’abord, elle augmente la nucléophilie du fragment allyl lié, le rendant prompt à former une nouvelle liaison carbone‑carbone. Ensuite, elle modère l’acidité de Lewis de l’atome central, qui est beaucoup moins enclin à se lier fortement aux atomes d’oxygène du substrat. Des calculs quantiques et des données de résonance magnétique nucléaire confirment que la charge est localisée sur le fragment allyl tandis que la communication électronique avec le centre silicium est réduite, ce qui explique comment le réactif peut être à la fois puissant et réticent à la chélation.
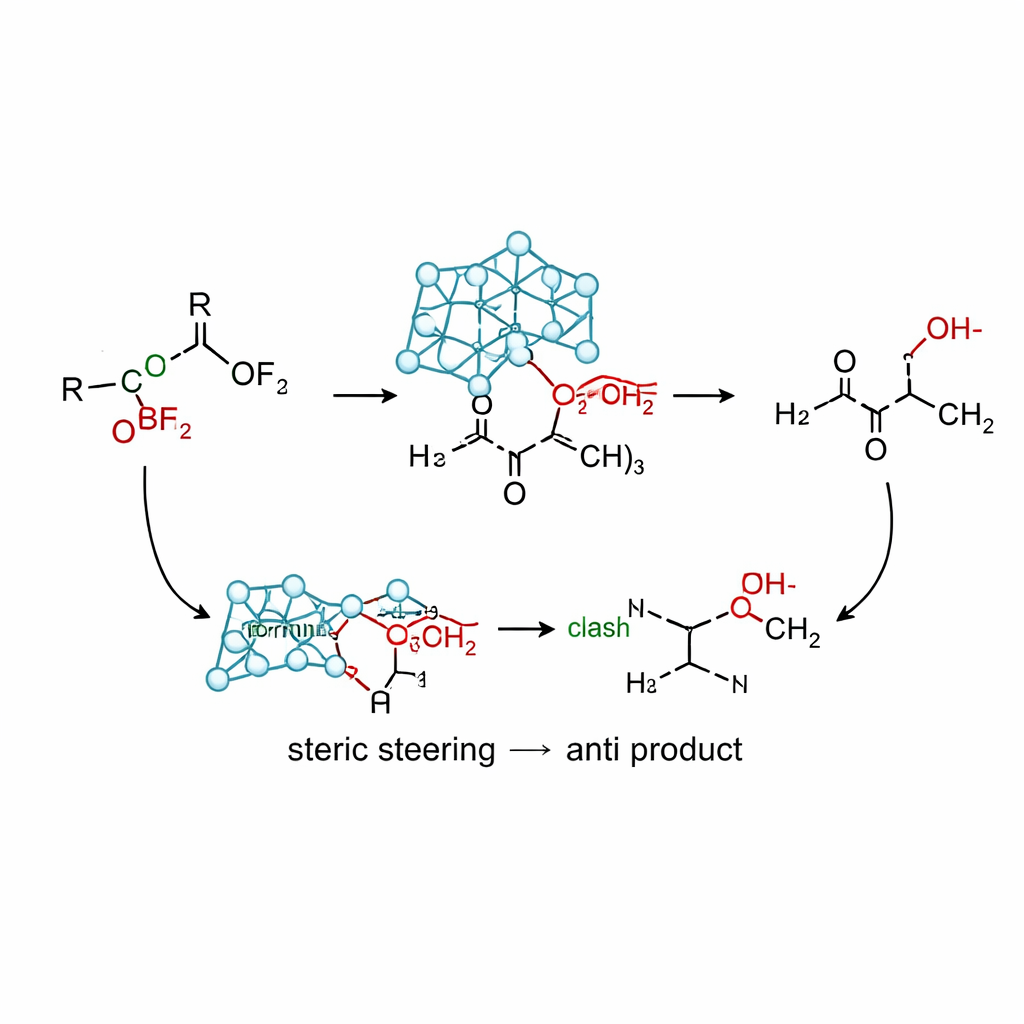
Comment la nouvelle réaction fonctionne en pratique
En utilisant la version silicium de ce réactif, l’allylsilatrane, associée à un acide de Lewis doux (trifluorure de bore), l’équipe a mis au point des conditions donnant de bons rendements d’alcools homoallyliques anti à partir d’une large gamme de cétones α‑oxy. Des expérimentations de référence montrent que de nombreuses sources d’allyl traditionnelles — à base d’étain, d’indium, de magnésium, de lithium et de simples silanes — favorisent soit le produit syn, donnent des mélanges ou se décomposent. En revanche, l’allylsilatrane délivre systématiquement des rapports anti/syn supérieurs à 95:5 pour des substrats portant des groupes méthoxy, isopropoxy, phénoxy, acétoxy, silyloxy et aminoxy, ainsi que divers cycles aromatiques et cétones cycliques. Les calculs suggèrent une voie non‑chélation dans laquelle le volume de la charpente atrane oriente l’approche du fragment allyl dans une conformation rappelant le modèle de Cram : le substituant oxygéné se trouve opposé à la carbonyle tandis que la répulsion stérique entre la cage et des cycles phényle voisins favorise la trajectoire conduisant au produit anti.
Conséquences pour la synthèse de médicaments et de produits naturels
La méthode fonctionne aussi pour des systèmes cycliques plus rigides, où l’encombrement de l’allylsilatrane encourage l’attaque depuis des positions moins encombrées, et pour des dérivés spécialisés qui transfèrent des groupes allyl substitués avec une sélectivité anti tout aussi élevée. Comme les anti‑1,2‑diols porteurs d’un fragment homoallylique sont des motifs fréquents dans des molécules bioactives, y compris des candidats modulant des enzymes, cette transformation offre aux chimistes un moyen fiable d’accéder à des variantes structurales qui nécessitaient auparavant des itinéraires en plusieurs étapes ou étaient simplement impraticables. Fait important, les mêmes substrats peuvent être orientés pour donner soit des produits syn soit anti en passant d’un système chélatant à base d’étain au nouveau système non‑chélatant à base de silatrane, offrant un contrôle précis sur la forme moléculaire.
Ce que cela signifie en termes simples
Essentiellement, les chercheurs ont construit un outil intelligent de livraison d’allyl qui frappe le carbone cible depuis le côté « défavorisé » sans être piégé par les atomes d’oxygène voisins. En ingénierienant soigneusement une cage autour du silicium, ils ont découplé puissance et « collance » : le réactif est assez fort pour former une nouvelle liaison mais pas suffisamment collant pour s’agripper aux atomes environnants et compromettre la géométrie souhaitée. Pour les non‑spécialistes, cela signifie que les chimistes disposent désormais d’un bien meilleur levier pour sculpter les structures moléculaires tridimensionnelles qui sous‑tendent de nombreux médicaments et produits naturels, élargissant l’espace de conception pour de futures molécules thérapeutiques et synthétiques complexes.
Citation: Tsutsui, Y., Shiga, K., Konishi, A. et al. Non-chelation control in allylations of α-oxy ketones using group-14 allylatranes. Nat Commun 17, 2019 (2026). https://doi.org/10.1038/s41467-026-69732-2
Mots-clés: allylation stéréosélective, cétones alpha‑oxy, allylsilatrane, contrôle non‑chélation, alcools homoallyliques