Clear Sky Science · fr
La région N-Myc MB0–MBI interagit de manière spécifique et dynamique avec le N-lobe de la kinase Aurora A
Pourquoi cela compte pour le traitement du cancer
De nombreux cancers infantiles agressifs dépendent d’une protéine appelée N-Myc pour maintenir la prolifération des cellules tumorales. N-Myc lui‑même est difficile à cibler avec des médicaments car il se comporte davantage comme un filament souple que comme une serrure rigide à laquelle une clé pourrait s’adapter. Cette étude révèle, avec un niveau de détail sans précédent, comment N-Myc s’accole à une autre protéine, l’enzyme Aurora kinase A (AurA), pour en renforcer l’activité et aider les cellules cancéreuses à survivre. En cartographiant ce partenariat, les chercheurs mettent au jour une voie réaliste pour le rompre à l’aide de petites molécules.
Un fauteur de troubles flexible trouve un partenaire solide
N-Myc appartient à la famille MYC, des commutateurs maîtres qui contrôlent la croissance cellulaire, le métabolisme et la division. Lorsqu’ils sont surexprimés, ces commutateurs deviennent de puissants moteurs du cancer, en particulier dans les tumeurs du système nerveux comme le neuroblastome à haut risque chez l’enfant. Contrairement à de nombreuses enzymes ou récepteurs, N-Myc ne se replie pas en une forme 3D fixe par lui‑même ; c’est une protéine « intrinsèquement désordonnée » qui remue et se reconfigure en permanence. Cette flexibilité la rend adaptative mais aussi notoirement difficile à viser avec des médicaments. AurA, en revanche, est une enzyme bien structurée qui participe à l’organisation de la division cellulaire. Des travaux antérieurs ont montré qu’AurA aide à stabiliser N-Myc dans les cellules tumorales et que les deux protéines interagissent physiquement, mais la nature exacte et l’importance des points de contact restaient floues.
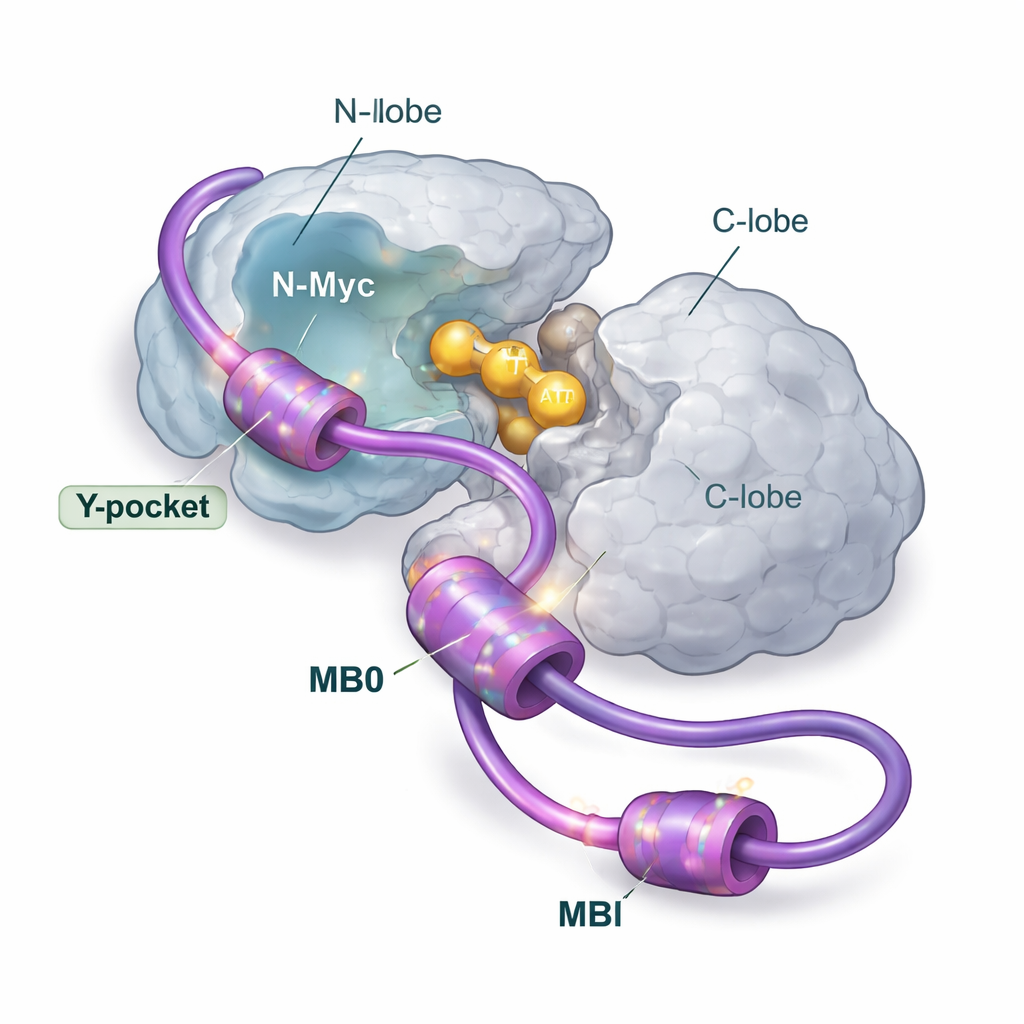
Plusieurs points d’accroche, une plateforme principale
À l’aide d’un large éventail de méthodes structurales et biophysiques, incluant la résonance magnétique nucléaire, la diffusion des rayons X en solution, la spectrométrie de masse, la calorimétrie et la modélisation informatique, les auteurs dissèquent la façon dont N-Myc et AurA se rencontrent en solution. Ils se sont concentrés sur l’extrémité N‑terminale de N-Myc, qui contient deux régions conservées appelées MB0 et MBI. Ces courts segments sont riches en résidus aromatiques (comme la phénylalanine, la tyrosine et le tryptophane) qui ont tendance à s’insérer dans des poches hydrophobes des protéines partenaires. L’équipe montre que N-Myc se lie principalement à AurA sous forme d’un couple 1:1, MB0 et MBI agissant comme zones de contact principales. Un autre fragment de N-Myc qui avait retenu l’attention dans des structures cristallographiques antérieures s’avère ne jouer qu’un rôle mineur lorsque la région complète MB0–MBI est présente.
Une poignée dynamique qui active l’enzyme
Plutôt que de se figer dans une unique conformation verrouillée, N-Myc reste majoritairement désordonné une fois lié à AurA. Les données sont compatibles avec un complexe « flou » : plusieurs segments de N-Myc se relaient pour contacter différentes zones du N-lobe d’AurA, en particulier un sillon connu sous le nom de Y-pocket et une boucle voisine qui relie les signaux au site actif. Malgré cette souplesse, l’effet est net — la liaison de MB0 et MBI stabilise le N-lobe d’AurA et augmente son activité kinase, c’est‑à‑dire sa capacité à transférer plus efficacement des groupes phosphate à ses cibles. Lorsque les chercheurs ont remplacé systématiquement des résidus aromatiques clés de MB0 et MBI par de l’alanine, le complexe N-Myc–AurA s’est affaibli, l’enzyme a été moins stabilisée et son activité a diminué. Cela montre que des « ancres » aromatiques spécifiques dans la chaîne par ailleurs souple de N-Myc sont essentielles pour stimuler AurA.
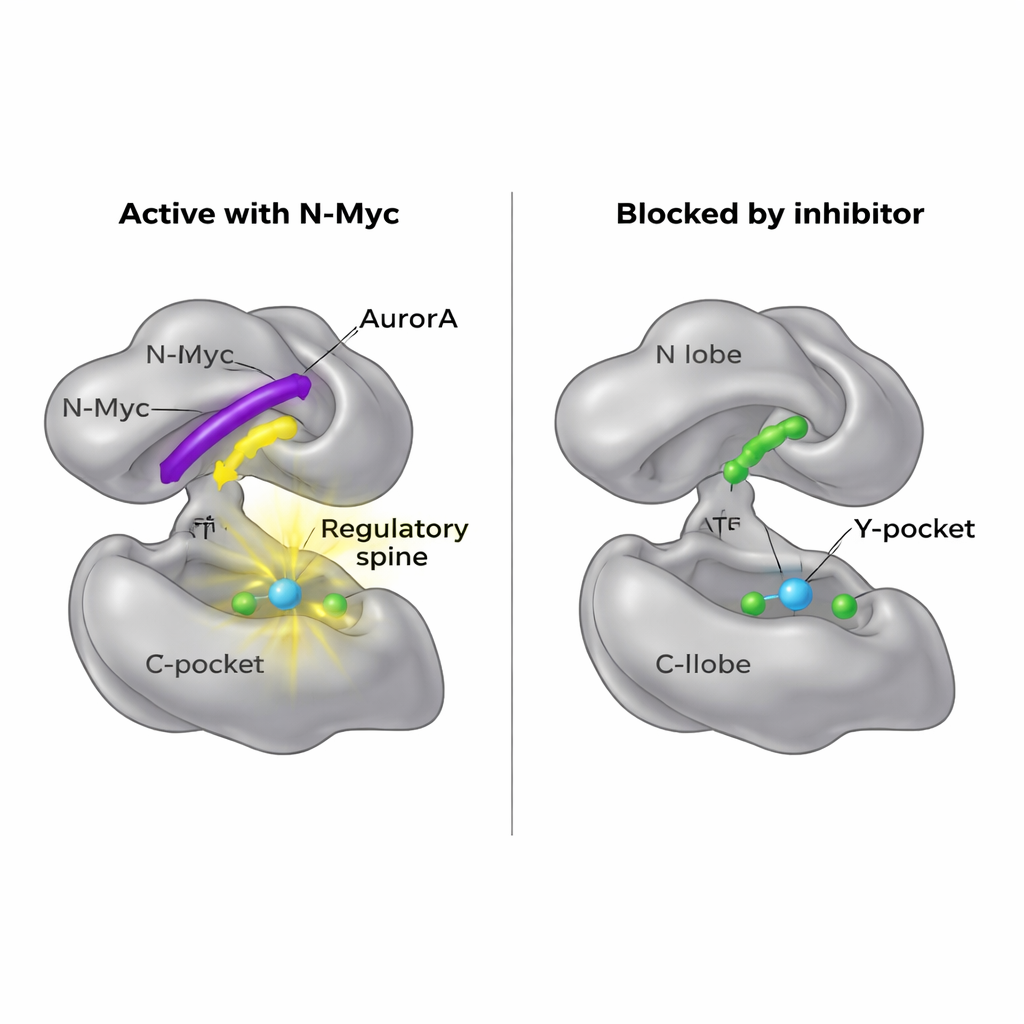
Ouvrir une nouvelle porte d’accès médicamenteuse
Parce que N-Myc est difficile à cibler directement, les chercheurs se sont demandé s’il serait possible de bloquer son site d’ancrage sur AurA. Leurs cartes structurelles ont révélé que MB0 et MBI occupent la même région générale du N-lobe que celle utilisée par une autre protéine partenaire, TPX2, pour activer AurA. Une petite molécule appelée AurkinA est déjà connue pour se loger dans le Y-pocket et déloger TPX2. Dans des expériences de liaison, AurkinA a efficacement concurrencé N-Myc pour le N-lobe d’AurA, empêchant l’attachement des fragments N-Myc1–69 et N-Myc1–100. Ce résultat montre que la surface du N-lobe, et en particulier le Y-pocket, constitue un point chaud « druggable » qui contrôle non seulement des régulateurs classiques comme TPX2, mais aussi des oncoprotéines désordonnées telles que N-Myc.
Ce que cela signifie pour les thérapies futures
Ce travail requalifie le partenariat N-Myc–AurA en une étreinte dynamique à multiples contacts centrée sur le N-lobe d’AurA, plutôt que comme un simple site de liaison rigide. Pour les non‑spécialistes, le message clé est que même une protéine cancéreuse informe comme N-Myc peut être affrontée indirectement en ciblant un patch d’ancrage solide sur son enzyme partenaire. En montrant que des composés existants se liant au N-lobe peuvent repousser N-Myc hors d’AurA, l’étude ouvre une voie claire vers des médicaments qui perturbent sélectivement cette interaction. De tels agents pourraient affaiblir un soutien critique pour N-Myc dans les tumeurs pédiatriques à haut risque et, avec un développement supplémentaire, offrir une nouvelle option thérapeutique pour des cancers longtemps jugés “indruggables”.
Citation: Hultman, J., Morad, V., Tanner, E. et al. The N-Myc MB0-MBI region interacts specifically and dynamically with the N-lobe of Aurora kinase A. Nat Commun 17, 2016 (2026). https://doi.org/10.1038/s41467-026-69725-1
Mots-clés: N-Myc, Aurora kinase A, protéines intrinsèquement désordonnées, neuroblastome, inhibiteurs d’interactions protéine–protéine