Clear Sky Science · fr
Promotion simultanée de la conversion photocatalytique du CH4 et de la production de H2O2 via la confinement de l’eau dans des nanopores
Transformer un gaz à effet de serre en liquides utiles
Le méthane, principal composant du gaz naturel, est à la fois une ressource précieuse et un puissant gaz à effet de serre. Le convertir en douceur en produits chimiques et carburants liquides pourrait aider à réduire les émissions tout en fournissant des produits du quotidien comme des solvants et des désinfectants. Cette étude montre une manière d’utiliser la lumière, l’eau et des nanoparticules soigneusement conçues pour valoriser le méthane en liquides oxygénés utiles tout en produisant simultanément du peroxyde d’hydrogène, un désinfectant courant et un oxydant « vert ».
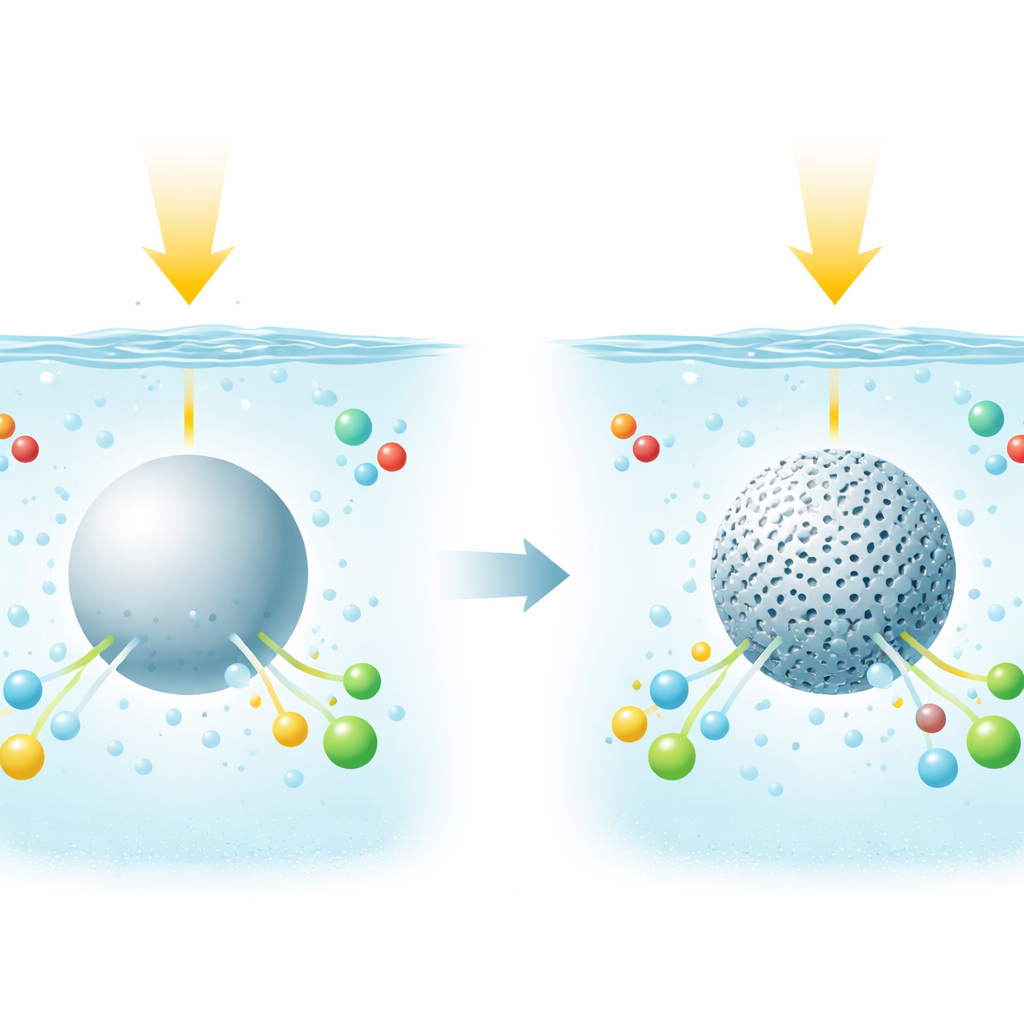
Pourquoi la structure de l’eau compte
De nombreuses réactions énergétiques propres ont lieu dans l’eau, où électrons et protons doivent se déplacer ensemble selon des étapes finement orchestrées. Dans l’eau liquide ordinaire, les molécules sont maintenues par un réseau de liaisons hydrogène en perpétuel renouvellement, qui gouverne discrètement la facilité de déplacement des charges et des atomes. Les auteurs se sont demandé : et si l’on pouvait comprimer légèrement l’eau dans de tous petits espaces pour modifier ce réseau ? Cela faciliterait‑il pour les catalyseurs excités par la lumière de diriger le méthane vers les produits désirés plutôt que de l’oxyder complètement en dioxyde de carbone ?
Une petite cage autour d’un noyau actif
Pour tester cette idée, l’équipe a fabriqué des particules coeur‑enveloppe. Au centre se trouve un photocatalyseur bien connu, du dioxyde de titane décoré de minuscules particules métalliques comme l’or ou le platine. Autour de ce noyau, ils ont fait croître une fine coque de silice transparente percée de pores à l’échelle nanométrique remplis d’eau. En ajustant le diamètre des pores jusqu’à environ 1,7 nanomètre — soit seulement quelques molécules d’eau de large — ils ont créé une couche d’eau confinée épousant la surface du catalyseur. Il est important de noter que l’absorption de la lumière et les propriétés de base du catalyseur restaient presque inchangées ; ce qui changeait, c’était la façon dont l’eau se disposait et se déplaçait dans ces canaux étroits.
Du méthane et de l’oxygène vers des liquides et du peroxyde
Lorsque ces particules ont été éclairées dans l’eau sous atmosphère de méthane et d’oxygène, la conception avec eau confinée a considérablement amélioré les performances. Par rapport au même catalyseur sans la coque poreuse, la conversion du méthane a été multipliée par environ trois et la production de peroxyde d’hydrogène a été multipliée par environ vingt‑deux. Le procédé a produit des produits liquides oxygénés tels que le méthanol et des molécules apparentées avec une sélectivité élevée, ce qui signifie beaucoup moins de sur‑oxydation gaspilleuse en dioxyde de carbone. L’effet était robuste : il se manifestait sous différentes sources lumineuses, persistait sur de nombreux cycles de réaction et pouvait être reproduit en utilisant d’autres métaux et même d’autres noyaux semi‑conducteurs, montrant que la stratégie est largement applicable et non un tour isolé.
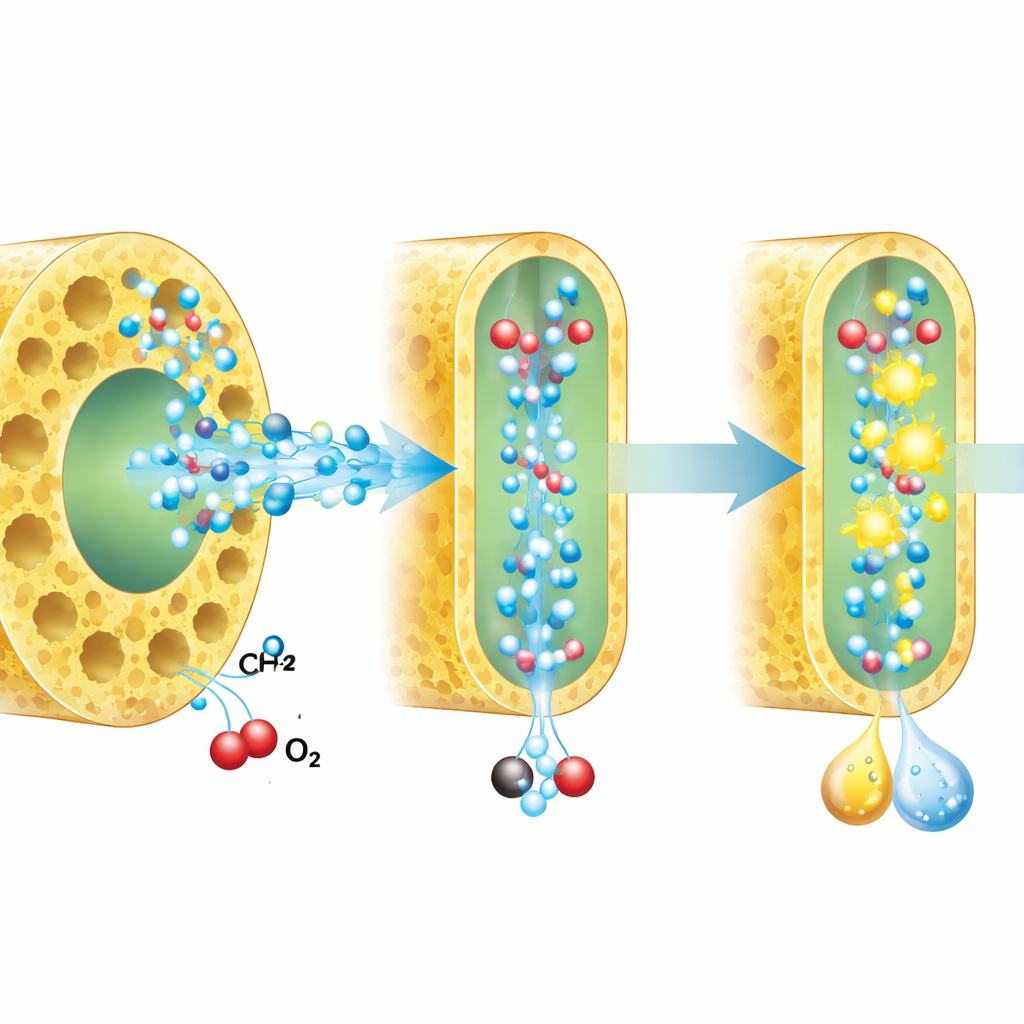
Comment l’eau comprimée modifie la voie réactionnelle
Pour comprendre pourquoi le confinement aide, les chercheurs ont combiné mesures spectroscopiques, expériences de piégeage des radicaux, marquage isotopique et simulations informatiques. Ils ont constaté que l’eau confinée forme un réseau de liaisons hydrogène plus faible et plus linéaire que l’eau en vrac. Dans cet environnement modifié, des espèces réactives clés — des radicaux oxygénés à vie courte qui attaquent le méthane — sont générées plus efficacement et vivent plus longtemps à proximité de la surface du catalyseur. Parallèlement, la voie de réduction de l’oxygène est orientée vers la formation directe de peroxyde d’hydrogène plutôt que vers d’autres intermédiaires moins utiles. Des études isotopiques, où l’hydrogène a été remplacé par du deutérium ou où des atomes d’oxygène ont été relabellisés, ont confirmé que le mouvement des protons devient plus central dans les étapes lentes et déterminantes de l’oxydation de l’eau et de la réduction de l’oxygène une fois l’eau confinée.
Un nouveau levier pour une chimie plus propre
En termes concrets, la coque de silice agit comme une éponge soigneusement conçue qui force l’eau à s’écouler dans des couloirs étroits autour du catalyseur actif, modifiant subtilement la façon dont elle se tient et la facilité de déplacement des protons et des électrons. Ce micro‑environnement réarrangé facilite pour les charges excitées par la lumière de transformer le méthane en liquides de valeur et de convertir l’oxygène en peroxyde d’hydrogène, au lieu de simplement brûler le combustible. Ce travail suggère que régler la « sensation » de l’eau près des surfaces solides — sans changer le matériau actif lui‑même — pourrait devenir un outil de conception puissant pour des procédés chimiques plus propres, depuis la conversion des gaz à effet de serre jusqu’à la production d’oxydants et de carburants verts.
Citation: Lv, F., Wei, S., Wu, X. et al. Simultaneous promotion of photocatalytic CH4 conversion and H2O2 production via nanopore water confinement. Nat Commun 17, 2119 (2026). https://doi.org/10.1038/s41467-026-69719-z
Mots-clés: oxydation photocatalytique du méthane, catalyseurs coeur‑enveloppe nanoporeux, eau confinée, production de peroxyde d’hydrogène, transfert électron‑proton couplé