Clear Sky Science · fr
Spatial perturb-seq : génomique fonctionnelle unicellulaire au sein de l’architecture tissulaire intacte
Voir les gènes à l’œuvre dans des circuits cérébraux vivants
De nombreuses maladies cérébrales, de la maladie d’Alzheimer à la maladie de Parkinson, sont liées à des gènes de risque, mais nous savons encore peu de choses sur la façon dont ces gènes affectent des cellules individuelles dans le cerveau vivant. Cette étude présente une méthode puissante pour observer ce qui se passe lorsque des gènes précis sont désactivés dans des cellules uniques, tandis que ces cellules restent dans leur environnement naturel au sein du tissu cérébral. L’approche, appelée Spatial Perturb-Seq, aide à relier le risque génétique à des perturbations du comportement cellulaire et de la communication intercellulaire dans le cerveau intact.
Une nouvelle façon de tester de nombreux gènes à la fois
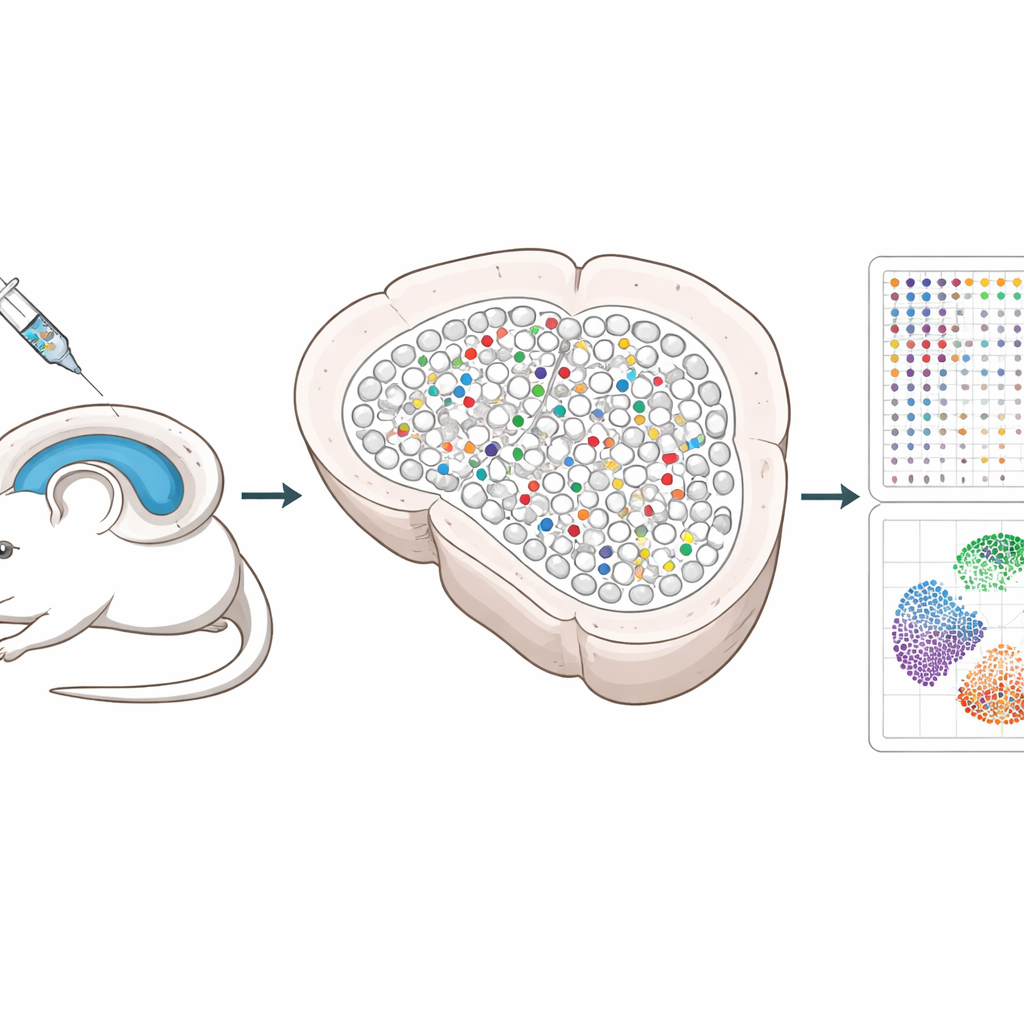
Les chercheurs ont développé un système qui utilise des outils d’édition génique CRISPR délivrés par des virus inoffensifs dans l’hippocampe, une région cérébrale importante pour la mémoire. Chaque virus transporte trois guides qui inactivent un gène choisi, ainsi qu’un « code-barres » ADN unique et un marqueur fluorescent pour permettre de retrouver ensuite les cellules modifiées. En mélangeant ces virus et en les injectant à faible dose, seule une petite fraction dispersée de cellules est modifiée, tandis que la plupart des voisines restent intactes. Ce schéma parcimonieux permet aux scientifiques de distinguer les changements survenant à l’intérieur des cellules modifiées de ceux apparaissant dans les cellules voisines saines.
Préserver la carte du cerveau
Les méthodes unicellulaires traditionnelles exigent de dissocier les tissus, ce qui détruit la position précise des cellules et peut même faire disparaître des neurones fragiles. Spatial Perturb-Seq lit au contraire l’activité génique directement sur des tranches cérébrales fines, de sorte que la localisation de chaque cellule est préservée. En utilisant une technologie appelée Stereo-seq, l’équipe a capturé les profils d’expression génique complets de plus de 200 000 cellules, tout en lisant les codes-barres CRISPR et en enregistrant les coordonnées de chaque cellule dans le tissu. Ils ont ensuite employé des algorithmes d’imagerie avancés pour délimiter chaque cellule et des outils computationnels pour identifier les types cellulaires et les voisinages locaux, en se concentrant en particulier sur les neurones hippocampiques et leurs contacts proches.
Comment les cellules modifiées influencent leurs voisines
Avec la carte tissulaire en main, les scientifiques ont comparé les neurones modifiés aux neurones non modifiés et, séparément, aux voisins non modifiés entourant chaque cellule modifiée. Cela leur a permis de distinguer les effets « autonomes à la cellule » (à l’intérieur de la cellule modifiée) des effets « non autonomes à la cellule » (dans le microenvironnement alentour). L’inactivation de 18 gènes différents, dont beaucoup sont liés au risque de maladies neurodégénératives, a produit des motifs distincts de modifications d’expression génique à l’intérieur des neurones modifiés. Certaines modifications, comme celles ciblant le gène Cfap410, ont aussi déclenché des changements puissants d’activité génique dans les cellules voisines, reflétant une altération des signaux locaux et du soutien cellulaire.
Indices sur les voies impliquées dans les maladies neurodégénératives
Plusieurs gènes ont fourni des éclairages particulièrement intéressants. La désactivation de Lrrk2, un gène majeur de risque pour la maladie de Parkinson, a provoqué d’importantes altérations dans les neurones modifiés, notamment une baisse des niveaux de Bc1, un ARN important pour l’ajustement de la production protéique aux synapses. En parallèle, les cellules voisines ont montré une expression altérée de gènes impliqués dans la structure des synapses, le trafic protéique et la gestion du calcium, suggérant que les problèmes liés à Lrrk2 se propagent au sein des circuits locaux. L’inactivation d’un autre gène, Srf, a perturbé un réseau de gènes associés à la croissance neuronale et à la plasticité, et affaibli des voies de signalisation ligand–récepteur spécifiques entre neurones, indiquant une communication cellulaire rompue. En évaluant systématiquement ces paires de signalisation, l’équipe a pu identifier quelles voies de communication étaient le plus affectées pour chaque gène.
Outils flexibles pour cartographier les effets génétiques
Pour montrer que Spatial Perturb-Seq n’est pas limité à une seule plateforme, les chercheurs l’ont aussi adapté à un système d’imagerie nommé Xenium. Là, des panneaux de sondes préconçues et des sondes de code-barres personnalisées lisent des gènes sélectionnés et des codes-barres directement dans le tissu. Bien que cette approche ciblée couvre moins de gènes que le Stereo-seq du transcriptome complet, les motifs de changements d’expression pour des modifications clés telles que Lrrk2 et Srf concordaient bien entre les deux méthodes et avec un grand atlas cérébral externe. Ces contrôles croisés renforcent la robustesse des effets observés sur les gènes et les voisinages.
Ce que cela signifie pour la recherche sur la santé cérébrale
De façon concrète, Spatial Perturb-Seq permet aux scientifiques d’éteindre de nombreux gènes différents dans des cellules cérébrales individuelles, puis d’observer comment ces cellules et leurs voisins immédiats réagissent, tout en préservant le schéma de connexions du tissu. Cela rend possible la cartographie de la manière dont les facteurs de risque génétique perturbent non seulement des cellules isolées, mais aussi les « conversations » entre elles, essentielles au bon fonctionnement du cerveau. À mesure que le séquençage deviendra moins coûteux et que des expériences de plus grande ampleur seront menées, cette approche pourrait aider à révéler quels gènes et quels circuits locaux sont les plus importants aux stades précoces de troubles comme Alzheimer, Parkinson et la SLA, guidant des stratégies thérapeutiques plus ciblées.
Citation: Shen, K., Seow, W.Y., Keng, C.T. et al. Spatial perturb-seq: single-cell functional genomics within intact tissue architecture. Nat Commun 17, 3018 (2026). https://doi.org/10.1038/s41467-026-69677-6
Mots-clés: génomique spatiale, criblages CRISPR, séquençage unicellulaire, neurogénération, communication cellule-cellule