Clear Sky Science · fr
FLEXTAG : un petit système d'étiquetage protéique auto-renouvelable pour l'imagerie super-résolution multicolore anti-décoloration
Voir l'invisible à l'intérieur des cellules
Une grande partie de la biologie moderne repose sur l'imagerie des molécules qui maintiennent nos cellules en vie. Mais même nos meilleurs microscopes optiques butent sur un problème simple : les marqueurs lumineux utilisés pour mettre en évidence les protéines s'estompent rapidement, et il est difficile d'étiqueter de nombreuses cibles simultanément sans perturber le fonctionnement cellulaire. Cet article présente FLEXTAG, une nouvelle famille de petits tags renouvelables qui gardent leur fluorescence beaucoup plus longtemps, prennent en charge plusieurs couleurs et fonctionnent avec les microscopes les plus puissants que les scientifiques utilisent pour observer l'architecture interne des cellules.
Pourquoi il est si difficile d'obtenir des images cellulaires plus nettes
Les microscopes à fluorescence conventionnels peuvent révéler des structures d'environ un quart de micromètre, ce qui reste bien plus grand que la plupart des protéines individuelles. Les méthodes de super-résolution extraient davantage de détails, atteignant quelques nanomètres, mais seulement si les marqueurs fluorescents se comportent parfaitement. Les marqueurs de protéines populaires aujourd'hui sont soit des anticorps volumineux, soit des protéines fluorescentes peu lumineuses, soit des étiquettes chimiques dont les colorants s'épuisent rapidement sous la lumière intense requise pour ces techniques. La fixation chimique des cellules pour l'imagerie détaillée peut aussi lier les protéines entre elles de manière à empêcher les colorants d'atteindre leurs cibles, et des molécules de colorant libres peuvent se lier de façon non spécifique, brouillant l'image par un fond lumineux.
Un nouveau type de tag protéique rechargeable
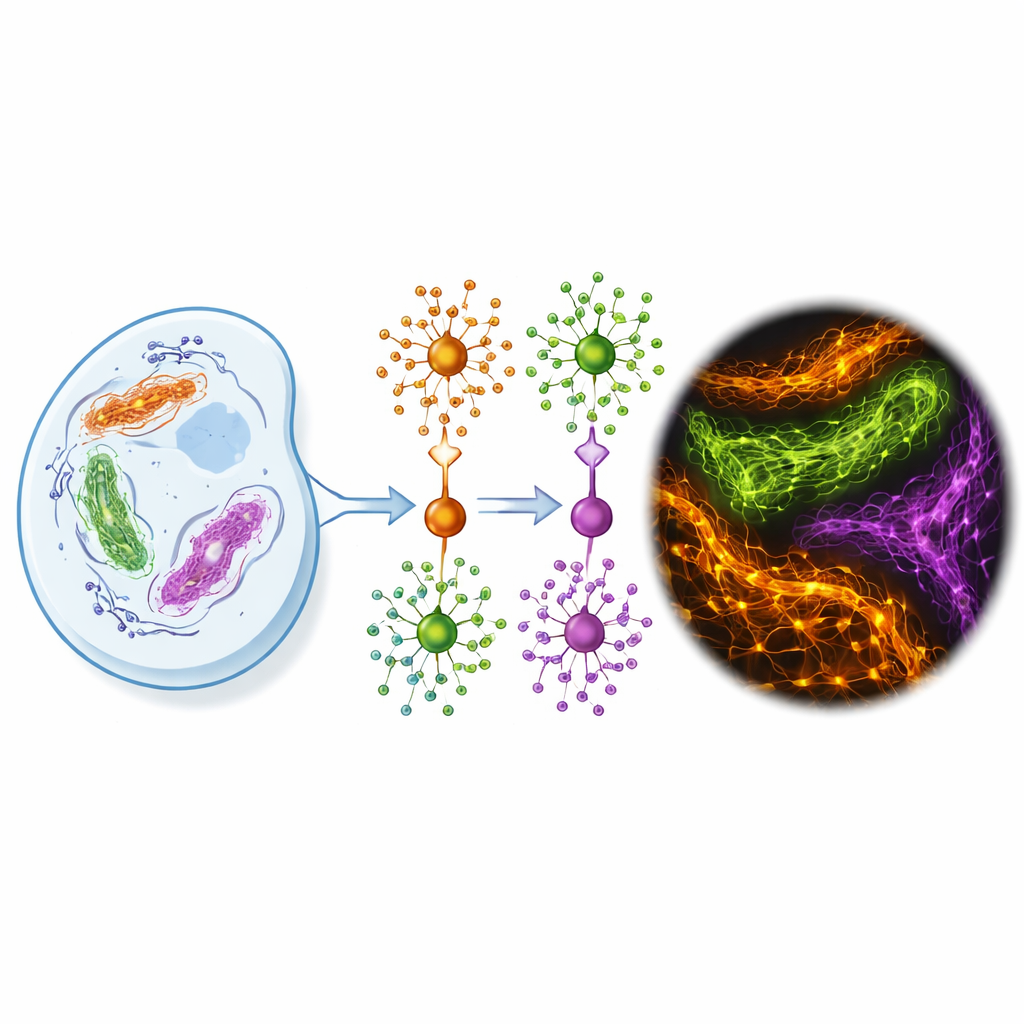
Les auteurs ont conçu FLEXTAG (abréviation de Fluorescent Labeling for Exchangeable, X-resilient Tagging in Advanced Generic Nanoscopy) pour aborder ces limitations de front. FLEXTAG n'est pas un tag unique mais un trio coordonné — FLEXTAG1, FLEXTAG2 et FLEXTAG3 — chacun étant une petite protéine ingénierée (12–18 kilodaltons, soit à peu près la moitié de la taille de tags classiques comme la GFP et bien plus petit que HaloTag). Chaque FLEXTAG se lie à un ligand petit-moléculaire assorti qui porte un colorant organique brillant. Crucialement, cette liaison est réversible : les molécules colorant–ligand se lient et se détachent continuellement. Lorsqu'un fluorophore est endommagé par la lumière, un nouvel exemplaire en solution lui succède, si bien que le signal se « renouvelle » plutôt que de s'affaiblir de façon continue.
Construire trois tags compacts et fiables
Pour créer FLEXTAG1–3, l'équipe a réutilisé trois échafaudages protéiques bien connus de la biologie cellulaire et de la conception de médicaments, puis a utilisé la modélisation structurale et des essais d'imagerie pour remodeler leur comportement. FLEXTAG1 est dérivé d'une bromodomaine reconnaissant une petite molécule modifiée ; les auteurs ont introduit des mutations pour rompre sa tendance à s'apparier et former des agrégats, tout en préservant une liaison forte à son ligand. FLEXTAG2 provient de la dihydrofolate réductase bactérienne. En ajoutant une liaison disulfure stratégique et en ajustant des linkers flexibles, ils ont stabilisé la protéine et augmenté de manière spectaculaire la fraction de tags portant un colorant à un instant donné, tout en conservant une liaison réversible. FLEXTAG3 est basé sur une protéine humaine FKBP utilisée en biologie chimique ; ici, l'équipe a équilibré force et vitesse de liaison pour que les colorants se détachent suffisamment rapidement pour être remplacés, tout en restant assez fortement liés pour fournir des images lumineuses et éviter une agrégation excessive.
Protéger les tags lors de la fixation et réduire le voile de fond
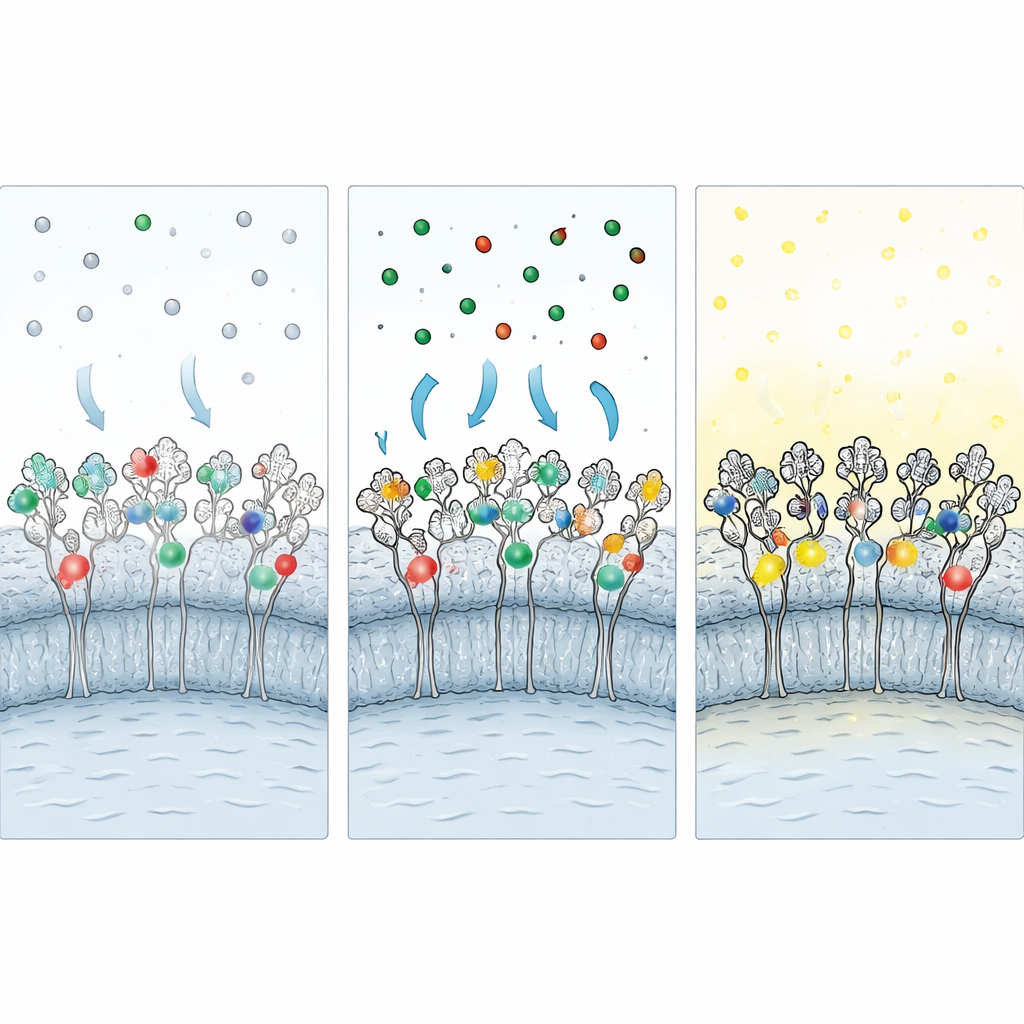
Parce que de nombreuses expériences importantes nécessitent l'imagerie de cellules fixées, les chercheurs ont développé une stratégie de « fixation protectrice ». Avant d'ajouter les fixatifs aldéhydes, ils saturent les cellules vivantes avec des versions non marquées de chaque ligand, bouchant le site de liaison du tag. Pendant la fixation, ces ligands protecteurs protègent les acides aminés vulnérables contre le réticulage chimique. Après fixation, les ligands protecteurs sont éliminés par lavage et remplacés par des ligands fluorescents, rétablissant l'accès au tag. Des étapes supplémentaires — réduction chimique pour neutraliser les groupes réactifs résiduels et un cocktail de blocage contenant de l'albumine, un détergent et un sel chaotropique — réduisent davantage la liaison non spécifique des colorants libres. Ensemble, ces mesures préservent environ 60–70 % du marquage observé dans les cellules vivantes tout en améliorant nettement le rapport signal/bruit.
Films plus nets et plus durables sur de nombreuses méthodes
Avec le cadre FLEXTAG en place, les auteurs l'ont mis à l'épreuve sur les principales familles de microscopie super-résolution. Dans les méthodes à illumination structurée telles que SIM et STED, les FLEXTAG ont permis l'imagerie multicolore des mitochondries, des microtubules, du réticulum endoplasmique et de l'actine avec beaucoup moins de décoloration que les étiquettes covalentes standard ; sur des dizaines de cycles d'imagerie, le signal des étiquettes conventionnelles diminuait de moitié ou plus, tandis que les signaux FLEXTAG restaient presque constants. Dans les méthodes « single-molecule » comme PAINT et STORM, l'échange rapide on–off des ligands FLEXTAG a produit des flux riches et stables de localisations pouvant être convertis en cartes tridimensionnelles et multicolores des structures subcellulaires, même dans des cellules vivantes sur plusieurs minutes. FLEXTAG2 a montré des cinétiques particulièrement favorables pour PAINT, tandis que FLEXTAG3 a excellé dans les films STORM de longue durée. Parce que les tags sont orthogonaux les uns aux autres et compatibles avec une large palette de colorants, les scientifiques peuvent marquer plusieurs protéines simultanément puis choisir le mode d'imagerie le mieux adapté à leur question sans modifier les constructions sous-jacentes.
Ce que cela change pour l'observation des cellules
FLEXTAG offre une sorte de connecteur universel et rechargeable entre les protéines et les colorants brillants. Sa petite taille réduit le risque que le tag ne déplace une protéine ou n'altère son fonctionnement, et ses colorants auto-renouvelables aident à contourner le problème ancien du photoblanchiment dans les microscopes puissants. En associant ces tags à une fixation protectrice et à une chimie de suppression du fond, les chercheurs peuvent obtenir des vues plus propres, plus durables et plus colorées de l'organisation et du mouvement des protéines à l'intérieur des cellules. Concrètement, cela signifie de meilleures cartes de l'architecture cellulaire, un suivi plus fiable des interactions moléculaires dans le temps et une boîte à outils polyvalente susceptible de bénéficier tant à la biologie cellulaire fondamentale qu'aux études translationnelles qui s'appuient sur l'observation des modifications liées aux maladies à l'échelle nanométrique.
Citation: Zhang, H., Yao, Y., Wang, X. et al. FLEXTAG: a small and self-renewable protein labeling system for anti-fading multi-color super-resolution imaging. Nat Commun 17, 2156 (2026). https://doi.org/10.1038/s41467-026-69658-9
Mots-clés: microscopie super-résolution, marquage par protéines fluorescentes, imagerie de cellules vivantes, résistance au photoblanchiment, architecture cellulaire