Clear Sky Science · fr
Surcyclage efficace du méthanol en éthylène glycol et glycolaldéhyde via une synthèse divergente d’accouplements C−C
Transformer un carburant simple en blocs de construction utiles
Le méthanol, un alcool simple qui peut être produit à partir du dioxyde de carbone, du gaz naturel, du charbon ou de la biomasse, est déjà un carburant et un produit chimique majeur. Cette étude montre comment des faisceaux lumineux et des nanomatériaux conçus avec précision peuvent transformer le méthanol en molécules plus complexes et de plus grande valeur — tout en libérant simultanément de l’hydrogène gazeux comme vecteur d’énergie propre. Le travail révèle une nouvelle manière d’orienter un matériau de départ unique vers deux produits utiles différents simplement en changeant l’arrangement des atomes métalliques sur la surface d’un petit catalyseur. 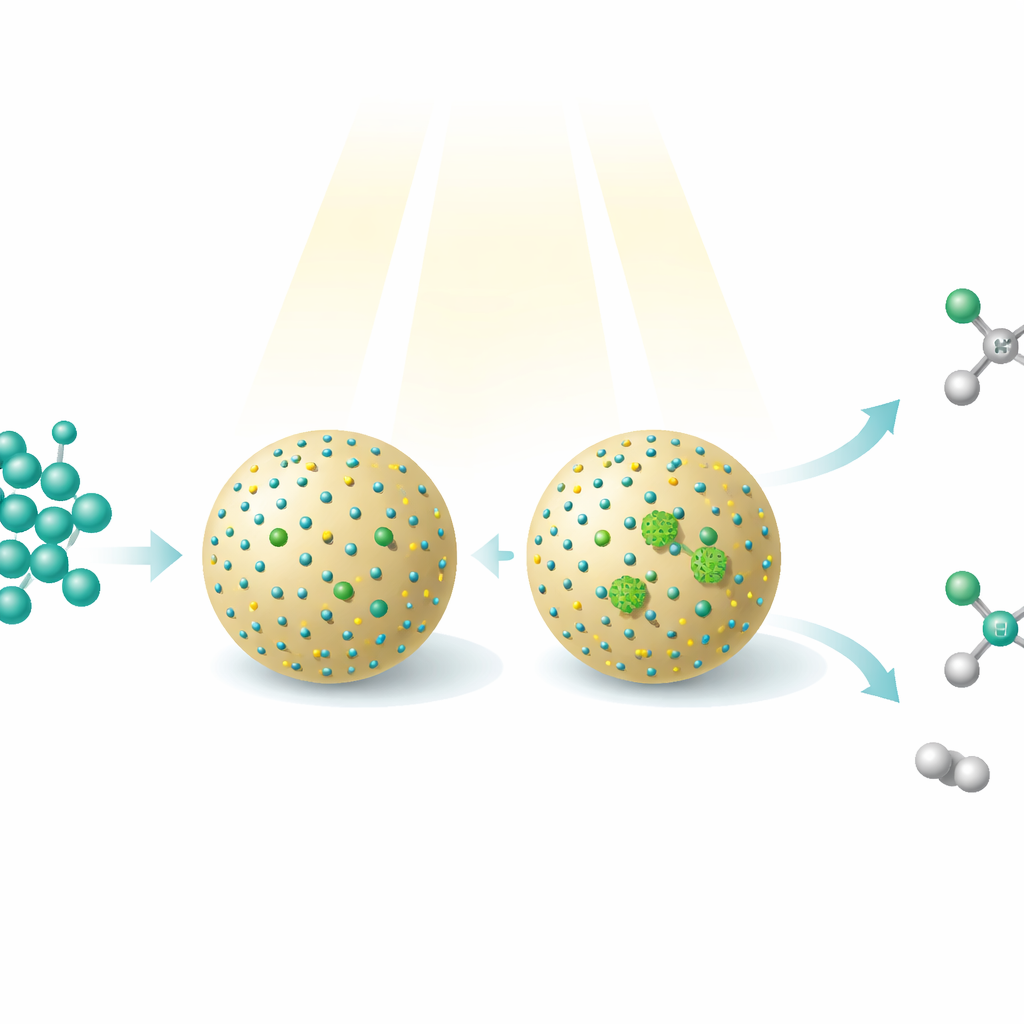
Pourquoi il est important d’améliorer le méthanol
Alors que le monde cherche des alternatives au pétrole, le méthanol est apparu comme un liquide attractif capable de stocker énergie et carbone. Cependant, la plupart des procédés industriels qui transforment le méthanol en molécules plus lourdes sont des outils grossiers : ils nécessitent des températures élevées, dépendent de filières fossiles et génèrent souvent de nombreux sous-produits indésirables. Les chimistes souhaitent coupler des molécules de méthanol avec une grande précision afin de produire sélectivement les composés désirés. Réaliser cela dans des conditions douces en utilisant la lumière plutôt que la chaleur faciliterait l’intégration de la production chimique avec les énergies renouvelables.
Des nanosphères activées par la lumière qui font le travail
Les chercheurs ont construit un photocatalyseur — littéralement un catalyseur activé par la lumière — en déposant de minuscules points quantiques de sulfure de cadmium sur des particules sphériques de silice. Ces points quantiques absorbent la lumière et génèrent des électrons et des trous énergétiques capables d’arracher des atomes d’hydrogène au méthanol, formant des fragments très réactifs. Des atomes de nickel ont ensuite été déposés sur les points quantiques de deux façons distinctes. Dans un matériau, le nickel existait principalement sous forme d’atomes isolés ; dans l’autre, le nickel formait de très petits agrégats de plusieurs atomes. Bien que la composition globale change à peine, cette différence subtile dans l’arrangement du nickel a profondément modifié les réactions qui se produisent à la surface.
Deux conceptions de nickel, deux produits propres
Lorsque le catalyseur avec des atomes de nickel isolés a été exposé à la lumière dans du méthanol, il a favorisé l’association de deux fragments identiques issus du méthanol, conduisant principalement à l’éthylène glycol — un diol à deux carbones largement utilisé dans les antigels et les plastiques. Cette voie a atteint environ 90 % de sélectivité, ce qui signifie que presque tout le méthanol converti est devenu ce seul produit, tandis que l’hydrogène gazeux était produit en quantités correspondantes à partir des atomes d’hydrogène retirés. En revanche, le catalyseur avec des agrégats de nickel a canalisé les mêmes fragments de méthanol le long d’un autre chemin. Ici, une portion du méthanol a été davantage oxydée en un intermédiaire de type formaldéhyde de courte durée, qui s’est ensuite combiné avec un autre fragment pour former du glycolaldéhyde, un autre composé à deux carbones utilisé dans la chimie fine et potentiellement dans des procédés d’origine biologique. Cette voie a délivré du glycolaldéhyde avec 96 % de sélectivité, là encore en parallèle avec de l’hydrogène. Le support en silice a aidé les points quantiques à capter la lumière plus efficacement et a rendu les particules plus robustes au fil de nombreux cycles d’utilisation. 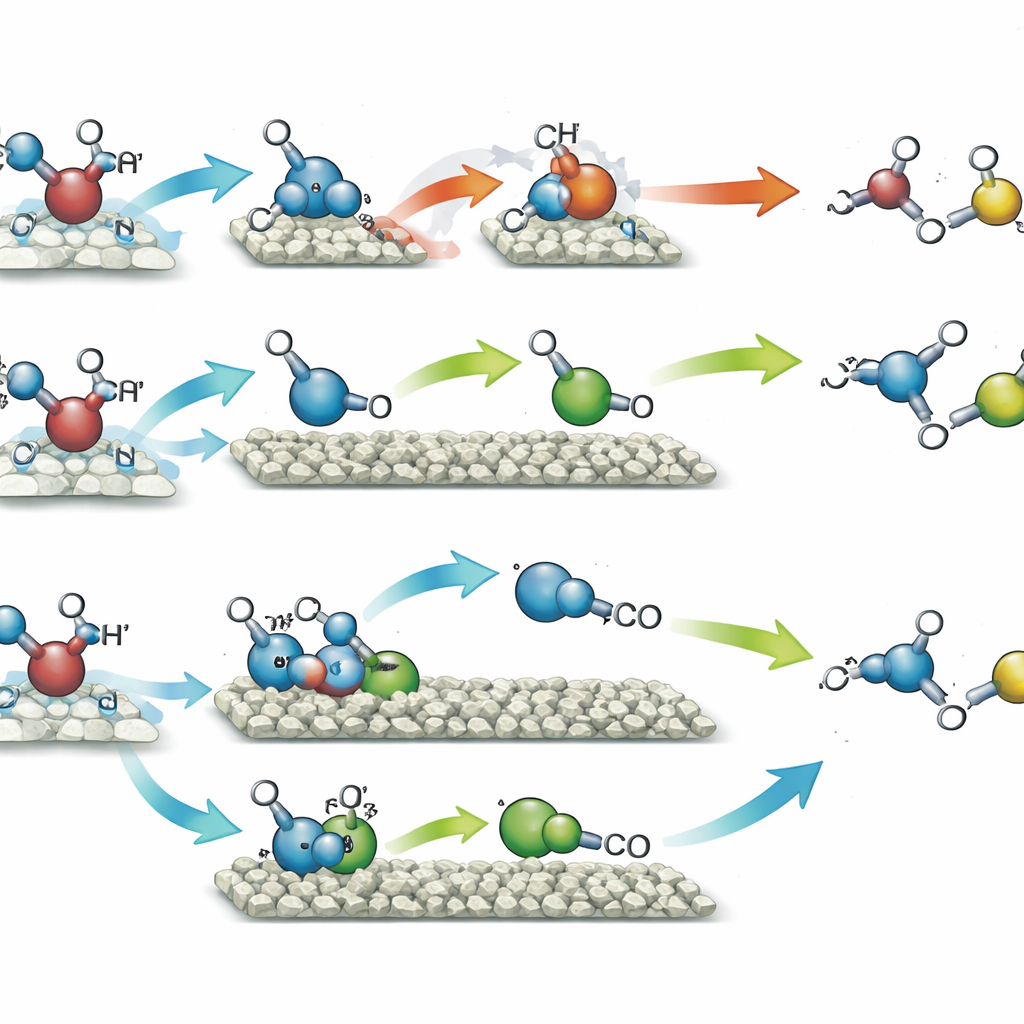
Plongée sous le capot de la réaction
Pour comprendre pourquoi les deux arrangements du nickel se comportaient si différemment, l’équipe a combiné une série de mesures avancées avec des simulations informatiques. Des expériences de résonance paramagnétique électronique ont montré que les deux catalyseurs généraient des radicaux issus du méthanol sous lumière, mais le catalyseur à agrégats favorisait aussi la rupture de la liaison oxygène–hydrogène, entraînant des fragments réactionnels plus divers et l’intermédiaire formaldéhyde. Des tests en temps résolu ont confirmé que cet intermédiaire apparaissait puis diminuait en concentration à mesure qu’il était consommé pour former le glycolaldéhyde. Des calculs quantiques ont cartographié les coûts énergétiques de chaque petite étape. Sur des atomes de nickel isolés, l’accouplement direct de deux radicaux identiques pour former l’éthylène glycol était la voie la plus facile. Sur des agrégats de nickel, ce même couplage liait trop fortement le produit, rendant son relargage difficile, tandis que la voie qui formait d’abord l’intermédiaire asymétrique puis le glycolaldéhyde devenait énergétiquement préférée.
Un nouveau levier pour une chimie plus propre
En termes concrets, ce travail montre que le « où » chaque atome de nickel se trouve sur une surface à l’échelle nanométrique peut décider du « quoi » que devient le méthanol lorsqu’il est illuminé. En basculant entre atomes isolés et petits agrégats de nickel, les chercheurs peuvent faire passer le produit principal de l’éthylène glycol au glycolaldéhyde, tous deux fabriqués de manière efficace et propre en même temps que de l’hydrogène combustible. Cette stratégie d’architecture des catalyseurs atome par atome offre une voie prometteuse pour valoriser des matières premières simples et renouvelables comme le méthanol en une gamme de produits chimiques utiles sans dépendre du pétrole, de conditions sévères ou de réactions secondaires génératrices de déchets.
Citation: Qi, MY., Tan, CL., Tang, ZR. et al. Efficient methanol upcycling to ethylene glycol and glycolaldehyde via divergent C−C coupling synthesis. Nat Commun 17, 2835 (2026). https://doi.org/10.1038/s41467-026-69656-x
Mots-clés: surcyclage du méthanol, photocatalyse, atomes uniques de nickel, éthylène glycol, glycolaldéhyde