Clear Sky Science · fr
Les signatures d'inclusion d'exons permettent d'estimer avec précision l'activité des facteurs d'épissage
Lire les marques d'édition cachées de la cellule
Chaque cellule de notre corps édite constamment ses messages ARN avant de les transformer en protéines. Cette modification, appelée épissage, contribue à décider si une cellule reste saine ou devient cancéreuse. L'étude à l'origine de cet article montre qu'en examinant attentivement quelles portions d'ARN sont conservées ou sautées — appelées signatures d'inclusion d'exons — les chercheurs peuvent déduire avec précision l'activité des « éditeurs » moléculaires qui contrôlent l'épissage, même dans des maladies complexes comme le cancer.
Comment les cellules coupent et recollent leurs messages
Les gènes ne sont pas lus en un seul bloc continu. Les cellules retirent des segments non codants et assemblent des fragments codants, appelés exons, pour construire le message ARN final. Des protéines spécialisées, les facteurs d'épissage, guident ce processus de découpe et de collage en décidant quels exons sont inclus. Leur comportement est régulé à de nombreux niveaux : la quantité de leur propre ARN et protéine produite, leurs modifications chimiques, leur localisation dans la cellule et leurs interactions avec d'autres protéines. Parce que tant de leviers peuvent modifier l'activité des facteurs d'épissage, mesurer un seul type de données — par exemple l'expression génique — ne suffit souvent pas à révéler ce qu'ils font réellement.
Transformer les motifs d'exons en mesures d'activité
S'inspirant de travaux antérieurs sur les facteurs de transcription, les auteurs proposent une stratégie différente : au lieu d'essayer de mesurer directement les facteurs d'épissage, lire leur activité à partir de leurs effets. Lorsqu'un facteur d'épissage change, l'inclusion de ses exons cibles évolue selon des motifs reconnaissables. L'équipe a compilé des centaines d'expériences où des facteurs d'épissage individuels étaient réduits, éliminés ou surexprimés, et a utilisé ces données pour construire des « réseaux empiriques » reliant chaque facteur aux exons qu'il affecte de manière évidente. Ils ont ensuite adapté un cadre computationnel appelé VIPER pour lire une nouvelle signature d'inclusion d'exons et attribuer un score d'activité à chaque facteur, indiquant à quel point il doit être actif pour expliquer le motif observé.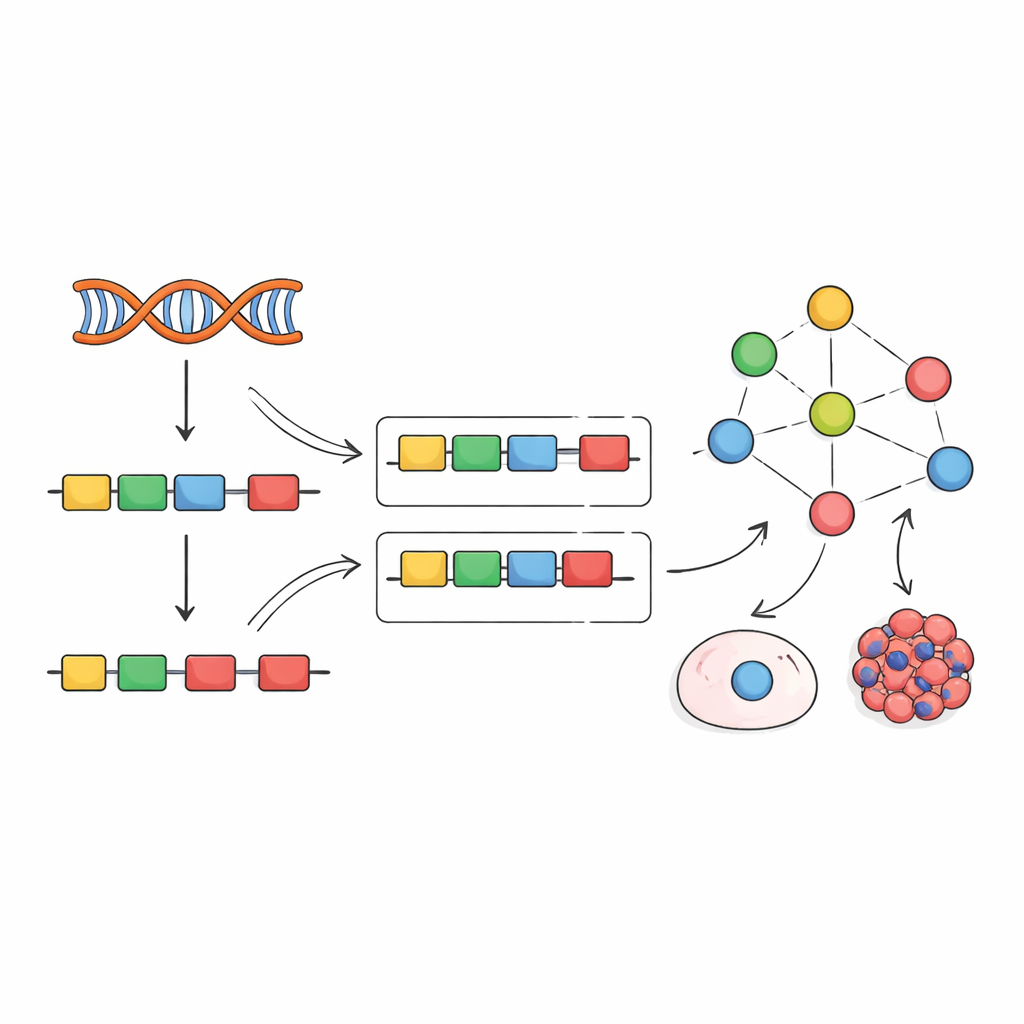
Tester la méthode sur des perturbations réelles
Pour vérifier l'efficacité de cette approche, les chercheurs ont comparé plusieurs façons de construire les réseaux et de calculer les scores d'activité. Les réseaux empiriques dérivés directement d'expériences de perturbation, combinés à l'analyse d'enrichissement de VIPER, surpassent nettement les alternatives basées uniquement sur l'inférence statistique. La méthode a identifié correctement le facteur d'épissage perturbé expérimentalement dans la plupart des tests, même entre différents types cellulaires et études. Elle a aussi saisi des mécanismes régulateurs plus subtils. Par exemple, un médicament anticancéreux appelé Indisulam provoque la dégradation de la protéine du facteur d'épissage RBM39 tandis que ses niveaux d'ARN augmentent, apparemment en tentative de compensation. Une analyse d'expression traditionnelle suggérerait à tort que RBM39 est plus actif, mais le score d'activité fondé sur les exons révèle correctement une forte perte de fonction, en accord avec l'action connue du médicament.
Dégager des programmes d'épissage cachés dans le cancer
Munis de cet outil, les auteurs se sont tournés vers The Cancer Genome Atlas, analysant des données au niveau des exons pour plusieurs types de tumeurs et tissus sains correspondants. Ils ont découvert deux grands programmes d'épissage récurrents. Un programme regroupe des facteurs d'épissage plus actifs dans les tumeurs et est associé à une survie moins bonne des patients — un programme de type oncogénique. L'autre réunit des facteurs systématiquement moins actifs dans les tumeurs et liés à de meilleurs résultats, ressemblant à des suppresseurs de tumeur. Ces programmes touchent des gènes impliqués dans des caractéristiques fondamentales du cancer, comme la division cellulaire rapide et la capacité des tumeurs à se dissimuler du système immunitaire. Par exemple, certains exons régulés par le programme de type suppresseur de tumeur semblent influencer la réponse des patients aux thérapies par inhibition des points de contrôle immunitaires, ce qui pointe vers de nouveaux marqueurs ou points d'intervention.
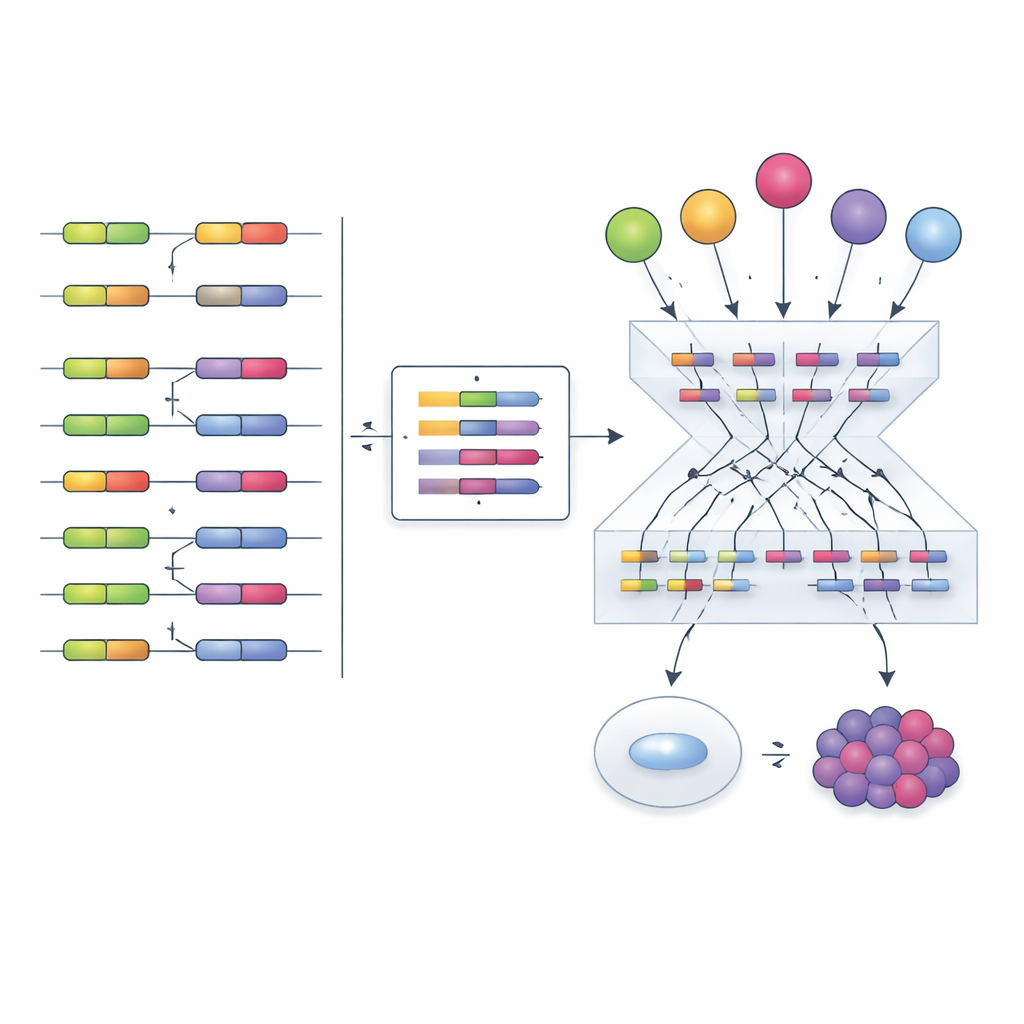
Suivre les changements d'épissage sur la route du cancer
Suivre les changements d'épissage sur la route du cancer
L'équipe a également examiné un modèle étape par étape de cellules humaines progressant de l'état normal à l'immortalisation, à la formation de tumeur, puis à la métastase. Ils ont constaté que le programme de type oncogénique devient plus actif à mesure que les cellules acquièrent des mutations favorisant le cancer, tandis que le programme de type suppresseur de tumeur s'estompe. En intégrant plusieurs couches de données — niveaux d'ARN, abondance protéique, modifications chimiques et changements d'épissage au sein des facteurs d'épissage eux-mêmes — ils ont identifié un ensemble ciblé d'événements moléculaires candidats susceptibles de piloter ces basculements de programme, offrant une liste priorisée pour des tests expérimentaux futurs.
Pourquoi cela compte pour les patients et la recherche future
En substance, l'étude montre que le comportement complexe des facteurs d'épissage peut être condensé en un score d'activité unique et interprétable, dérivé de la façon dont les exons sont inclus ou exclus. Cela rend possible l'étude de la régulation de l'épissage dans de larges cohortes de patients et diverses expériences en utilisant uniquement des données d'ARN-seq standard, sans nécessiter de profils multi-omiques coûteux. Pour un lecteur non spécialiste, le message clé est que les motifs de découpe et de collage des gènes portent une information riche sur les systèmes de contrôle cachés de la cellule, et que décoder ces motifs peut révéler de nouveaux moteurs du cancer, améliorer le pronostic et orienter la recherche de traitements plus précis.
Citation: Anglada-Girotto, M., Segura-Morales, C., Moakley, D.F. et al. Exon inclusion signatures enable accurate estimation of splicing factor activity. Nat Commun 17, 1994 (2026). https://doi.org/10.1038/s41467-026-69642-3
Mots-clés: Épissage de l'ARN, facteurs d'épissage, génomique du cancer, transcriptomique, inférence d'activité des protéines