Clear Sky Science · fr
Ingénierie génétique du microenvironnement tumoral par LOAd703 en association avec l’atezolizumab dans le mélanome malin métastatique : essai de phase I/II
Pourquoi cette nouvelle étude sur le mélanome est importante
Pour les personnes atteintes d’un mélanome cutané avancé qui ne répond plus aux immunothérapies puissantes actuelles, les options de traitement sont limitées et souvent éprouvantes. Cette étude teste une idée différente : injecter directement dans les tumeurs un virus génétiquement modifié, associé à un médicament immunostimulant déjà utilisé, pour réveiller les défenses de l’organisme et reprendre le contrôle du cancer. Les premiers résultats suggèrent que cette approche peut être administrée en toute sécurité et pourrait bénéficier à une part significative de patients dont la maladie résistait auparavant aux soins standard.
Un cancer de la peau tenace qui déjoue les traitements
Le mélanome est l’un des cancers de la peau les plus graves et fréquents dans les pays occidentaux, et son incidence a fortement augmenté ces dernières décennies. Les médicaments modernes ciblant les points de contrôle immunitaire — qui relâchent les freins exercés sur les lymphocytes T — ont transformé le pronostic, portant la survie à cinq ans des formes avancées à environ la moitié des patients. Cependant, de nombreuses tumeurs finissent par ne plus répondre. Souvent, ces cancers résistants sont entourés d’un environnement « froid » de cellules et de molécules qui empêchent l’accès des cellules immunitaires ou les inactivent. Trouver des moyens de reconfigurer ce microenvironnement tumoral pour que les lymphocytes T reconnaissent et attaquent à nouveau la tumeur est une priorité majeure de la recherche.
Un virus conçu pour reconfigurer le voisinage tumoral
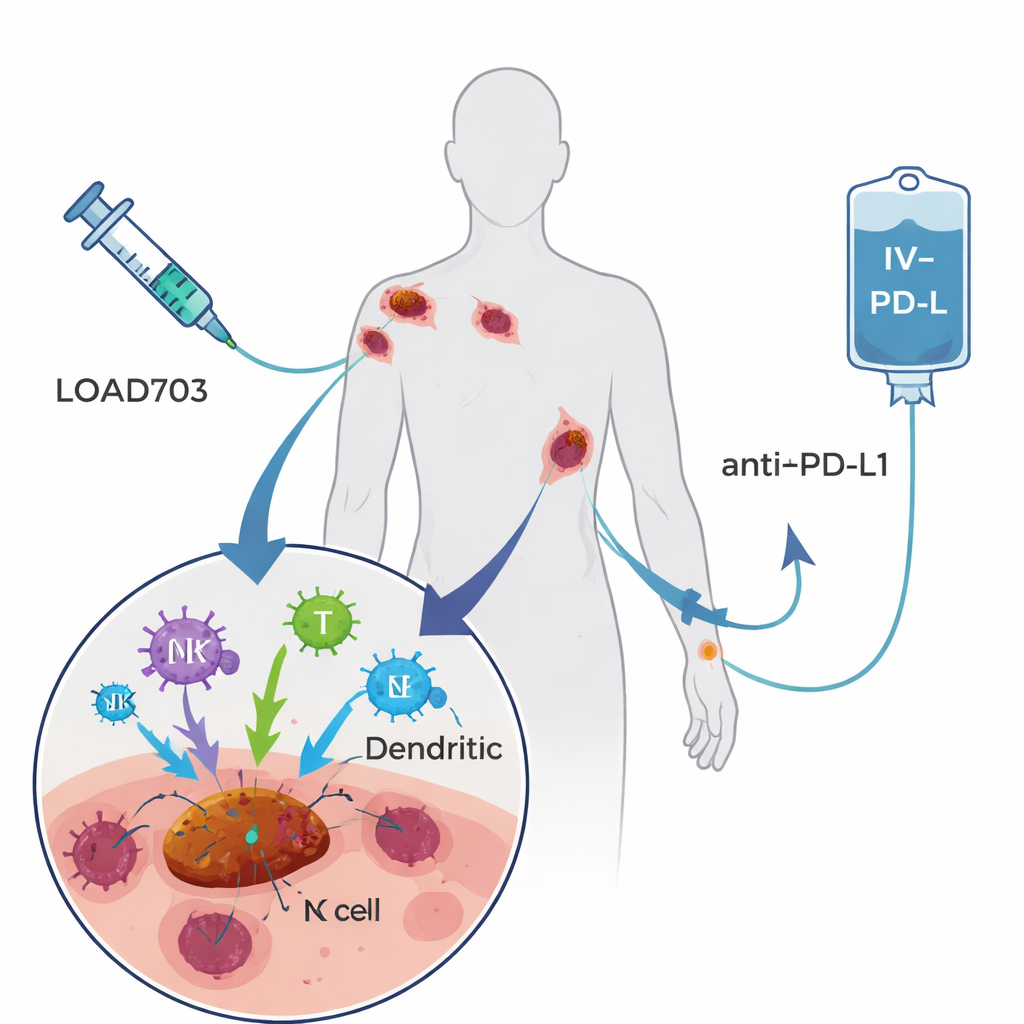
Le traitement étudié ici, nommé LOAd703, est un adénovirus modifié — un type de virus du rhume courant — conçu pour accomplir deux fonctions. Premièrement, il préfère se répliquer dans les cellules tumorales et les détruire, stratégie connue sous le nom de virothérapie oncolytique. Deuxièmement, il véhicule des instructions génétiques pour deux signaux puissants stimulant l’immunité exprimés sur les cellules infectées. Ces signaux, CD40L et 4‑1BBL, favorisent la maturation des sentinelles immunitaires professionnelles (cellules dendritiques) et la présentation de fragments tumoraux, et ils renforcent et expandent les lymphocytes T et les cellules NK (natural killer) combattant le cancer. Les patients de l’essai ont reçu LOAd703 injecté directement dans une ou plusieurs tumeurs toutes les trois semaines, en association avec l’atezolizumab, un anticorps établi administré par voie intraveineuse qui bloque la voie PD‑L1. L’espoir était que le virus transforme les tumeurs en véritables usines vaccinales in situ, tandis que l’anticorps maintient l’activité des lymphocytes T réactivés.
Qui a été traité et quels ont été les résultats
L’essai de phase I/II a recruté 24 personnes atteintes d’un mélanome de stade IV ayant clairement progressé malgré au moins un traitement antérieur bloquant PD‑1 ; beaucoup avaient reçu plusieurs lignes d’immunothérapie et de thérapies ciblées. Deux niveaux de dose du virus ont été évalués. Dans l’ensemble, la combinaison a été bien tolérée. Les effets secondaires les plus fréquents liés au virus — fièvre, frissons, nausées et symptômes de type grippal — étaient majoritairement légers et temporaires. Deux patients seulement ont présenté des réactions plus sérieuses mais réversibles à la dose la plus élevée, et personne n’a dû interrompre le traitement en raison d’effets liés au virus. Lors de l’évaluation des réponses tumorales, quatre patients (17 %) ont présenté une réduction mesurable de leurs tumeurs, et plus de la moitié ont connu au moins une maladie stable pendant un certain temps. Deux ans après l’inclusion, près de la moitié des participants étaient encore en vie, y compris certains dont les examens montraient un contrôle durable ou une disparition complète des lésions détectables après l’arrêt de la thérapie.
Signes d’une réactivation du système immunitaire
Pour analyser ce qui se passait au sein des tumeurs et dans le sang, l’équipe a étudié des biopsies tissulaires et des prélèvements sanguins réalisés avant le traitement et environ neuf semaines après le début. Dans les tumeurs injectées, ils ont observé une activité accrue de gènes associés aux réponses immunitaires de type 1, y compris des marqueurs de lymphocytes T et de cellules NK activés, et des molécules facilitant l’entrée de ces cellules dans les tumeurs depuis les vaisseaux sanguins voisins. Les signaux liés à la présentation d’antigènes — le processus par lequel des fragments tumoraux sont exposés aux lymphocytes T — ont également augmenté, suggérant que la thérapie virale convertissait le microenvironnement tumoral d’un état suppressif vers un état plus favorable à l’immunité. Dans le sang, plusieurs protéines liées à l’immunité, y compris PD‑L1 lui‑même, ont augmenté après la thérapie, cohérent avec une activation large des voies immunitaires. Les patients ayant survécu plus longtemps montraient globalement des profils géniques associés à une fonction T robuste et une protection antivirale, tandis que ceux à survie plus courte présentaient des profils liés à des types cellulaires suppressifs et à des signaux de remodelage tissulaire.
Ce que cela pourrait signifier pour les soins futurs
Il s’agissait d’une petite étude à bras unique sans groupe comparateur, de sorte que ses chiffres de survie et de réponse doivent être interprétés avec prudence. Néanmoins, la combinaison d’une bonne tolérabilité, d’une activation immunitaire au sein des tumeurs et d’un contrôle de la maladie encourageant chez des patients fortement prétraités suggère que des virus oncolytiques génétiquement modifiés comme LOAd703 pourraient aider à re‑sensibiliser le mélanome aux inhibiteurs de points de contrôle — ou même maintenir les tumeurs sous contrôle de manière autonome. Les résultats appellent à des essais plus larges et contrôlés, éventuellement en associant le virus à d’autres agents ciblant l’immunité, afin de préciser quels patients en bénéficient le plus et comment intégrer au mieux cette stratégie dans la prise en charge du mélanome.
Citation: Hamid, O., Ekström-Rydén, V., Mehmi, I. et al. LOAd703-induced tumor microenvironment gene engineering in combination with atezolizumab in metastatic malignant melanoma: a phase I/II trial. Nat Commun 17, 1760 (2026). https://doi.org/10.1038/s41467-026-69629-0
Mots-clés: mélanome, immunothérapie, virus oncolytique, microenvironnement tumoral, résistance aux inhibiteurs de points de contrôle