Clear Sky Science · fr
Des médicaments « cagoulés » permettent la décohésion photocatalytique simultanée de l’oxyde nitrique et d’anesthésiques pour une analgésie antibactérienne
Combattre les germes et la douleur en même temps
Les infections bactériennes ne menacent pas seulement notre santé ; elles causent aussi une douleur importante. Les traitements standards visent généralement les germes mais laissent les patients dépendants d’antalgiques séparés, qui peuvent s’estomper rapidement ou provoquer des effets indésirables. Cette étude présente un médicament contrôlé par la lumière visant à tuer les bactéries et soulager la douleur en une seule étape coordonnée, offrant un aperçu de soins des infections plus intelligents et confortables.
Une idée de médicament deux-en-un
Les chercheurs ont construit leur approche autour de la tétracaïne, un anesthésique local familier utilisé pour engourdir la peau et les nerfs. Ils ont chimiquement lié l’oxyde nitrique, une petite molécule gazeuse connue pour ses puissantes actions antibactériennes et anti-inflammatoires, à la tétracaïne. Cela a créé un « pro-médicament » appelé TTC-NO qui est essentiellement inactif jusqu’à activation. TTC-NO a ensuite été encapsulé, avec une molécule adjuvante photosensible, dans de petites bulles de polymère appelées micelles qui peuvent circuler dans des milieux aqueux tels que le sang ou le liquide tissulaire. 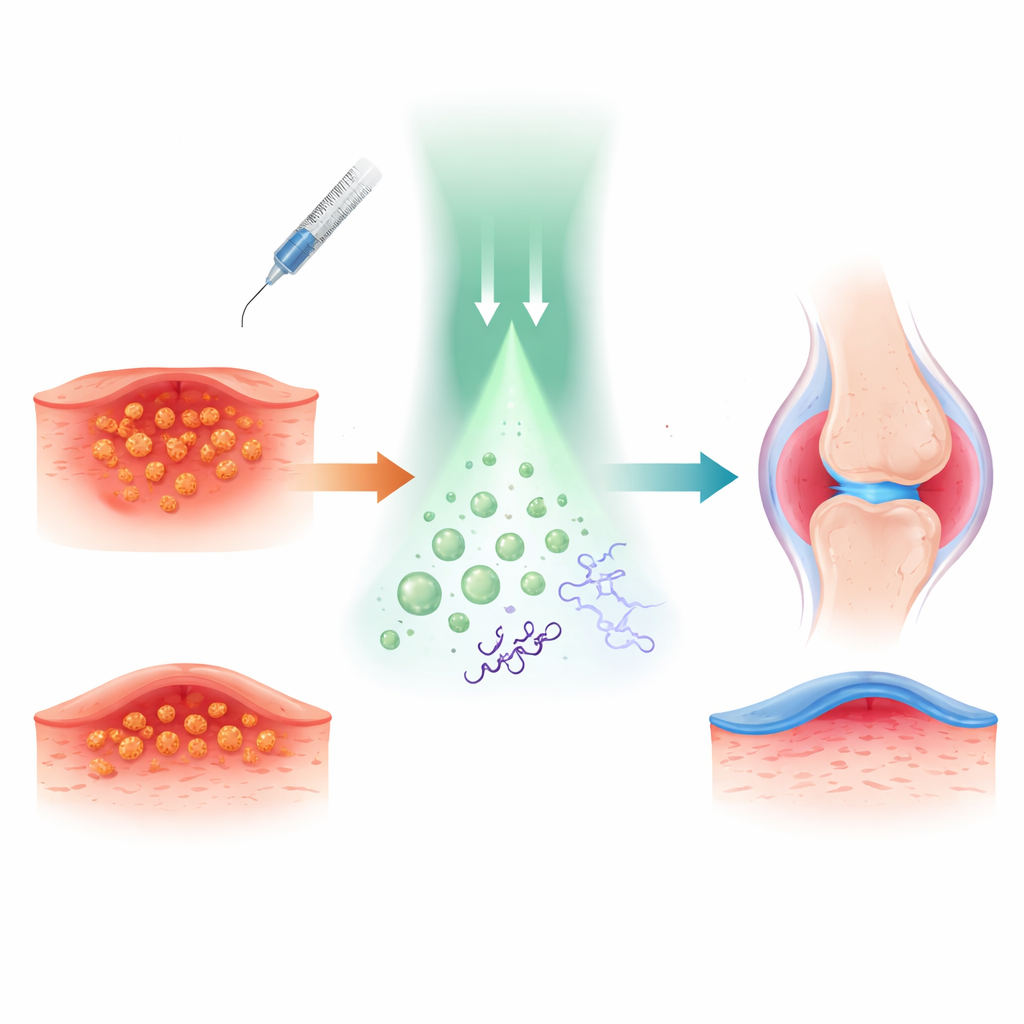
Activer le médicament par une lumière douce
Pour comprendre ce mécanisme d’allumage par la lumière, l’équipe a étudié la chimie en solution. Ils ont montré qu’un photocatalyseur à base d’iridium peut transférer un électron à TTC-NO lorsqu’il est illuminé par une lumière verte. Cela fragilise une liaison spécifique, entraînant la libération de l’oxyde nitrique et la restauration de la tétracaïne sous sa forme active. Des mesures par spectroscopie et chromatographie ont confirmé que TTC-NO est presque entièrement converti en tétracaïne et en oxyde nitrique dans ces conditions, tout en restant essentiellement inchangé dans l’obscurité. Lorsque les deux composants ont été encapsulés dans des micelles, les particules sont restées stables, d’environ 80 nanomètres de diamètre, et n’ont libéré leur contenu que sous irradiation, prouvant que le concept de « médicament cagoulé par un médicament » peut être contrôlé depuis l’extérieur du corps par la lumière.
Aider les plaies infectées à guérir plus vite
L’équipe est ensuite passée à des souris porteuses de plaies cutanées délibérément infectées par Staphylococcus aureus résistant à la méticilline (SARM), un germe problématique en milieu hospitalier. Certaines plaies ont reçu des traitements standard tels qu’un antibiotique ou un facteur de croissance, tandis que d’autres ont été traitées par des micelles de TTC-NO, avec ou sans lumière. Quand la lumière a été activée, le système TTC-NO a fortement réduit les nombres bactériens, calmé l’inflammation, favorisé la néovascularisation et augmenté le dépôt de collagène, éléments essentiels à une réparation correcte. Les plaies traitées de cette manière se sont refermées plus rapidement et plus complètement que celles traitées par la tétracaïne seule ou par des micelles maintenues dans l’obscurité, et leurs résultats étaient comparables à ceux d’un antibiotique de première intention. Fait important, les contrôles de sécurité n’ont montré aucun dommage majeur aux organes ou à la biochimie sanguine.
Soulager la douleur et calmer les signaux nerveux
Parce que l’infection et la lésion tissulaire activent fortement les voies de la douleur, les scientifiques ont mesuré attentivement les comportements liés à la douleur dans le même modèle de plaie. La tétracaïne traditionnelle augmentait brièvement la force nécessaire pour déclencher une réponse douloureuse mais s’estompa en quelques heures. En revanche, les micelles TTC-NO activées par la lumière ont procuré un soulagement allant jusqu’à 12 heures. Des études microscopiques des amas nerveux près de la moelle épinière et des enregistrements d’activité dans le cortex sensoriel ont révélé que le traitement combiné diminuait le déclenchement des neurones sensoriels de la douleur bien après la disparition de l’effet de la tétracaïne pure. D’autres expériences suggèrent que cette durée prolongée provient de la réduction de la charge bactérienne et de l’inflammation par l’oxyde nitrique, et non seulement de l’engourdissement des nerfs.
Protéger les articulations infectées et douloureuses
Les chercheurs ont également testé le système chez des souris atteintes d’arthrite septique, une infection sévère à SARM à l’intérieur de l’articulation du genou qui provoque gonflement, perte osseuse et douleur intense. Les micelles TTC-NO activées par la lumière ont réduit la largeur articulaire, diminué le nombre de bactéries et protégé la structure osseuse, comme l’ont montré des scans haute résolution. Les taux de molécules inflammatoires délétères dans le sang ont chuté, tandis que les molécules de signalisation protectrices ont augmenté. Sur le plan comportemental, les souris traitées pouvaient supporter une pression mécanique plus forte sur la patte affectée et se déplaçaient plus librement dans une arène ouverte, montrant une fois de plus un soulagement plus durable que la tétracaïne seule. Les mesures nerveuses et cérébrales reflétaient ces bénéfices comportementaux, indiquant un affaiblissement généralisé des voies de la douleur sans toxicité locale ou systémique évidente. 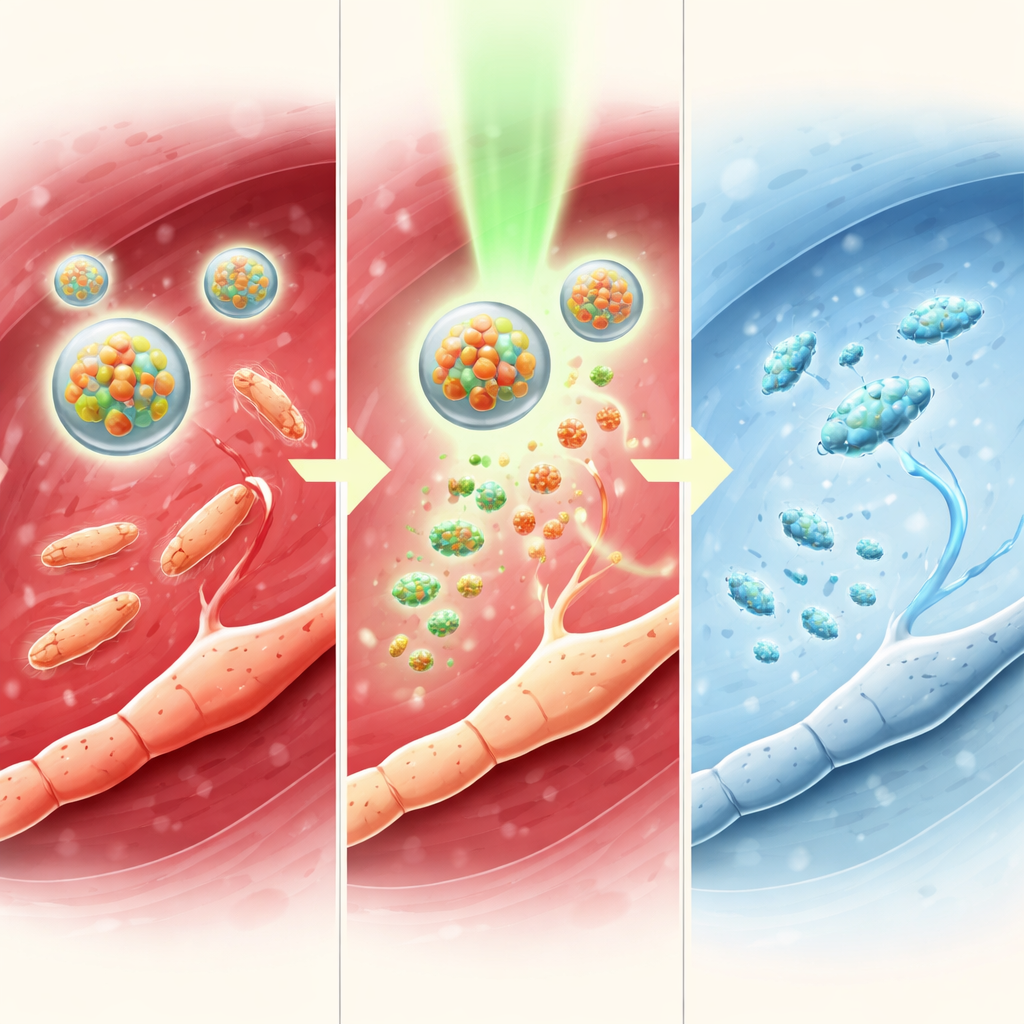
Ce que cela pourrait signifier pour les patients
En résumé, ce travail démontre un nanosystème unique activé par la lumière capable à la fois d’éliminer des infections bactériennes tenaces et de réduire significativement la douleur associée. En « cagoulant » chimiquement un anesthésique à l’intérieur d’une structure libérant de l’oxyde nitrique et en l’emballant dans des micelles, les auteurs obtiennent une libération localisée et à la demande de deux agents utiles à l’aide d’une lumière visible douce. Dans des modèles animaux de plaies cutanées et d’infections articulaires, cette conception accélère la guérison et prolonge le soulagement de la douleur au-delà de ce qu’un anesthésique local conventionnel peut offrir. Bien que de nombreux tests restent nécessaires avant l’utilisation humaine, l’étude illustre comment des médicaments intelligents et commutables pourraient un jour rendre les traitements des infections à la fois plus efficaces et plus confortables.
Citation: Zhang, J., Gan, G., Cao, C. et al. Drug-caged drugs enable photocatalytic dual decaging of nitric oxide and anesthetics for antibacterial analgesia. Nat Commun 17, 2843 (2026). https://doi.org/10.1038/s41467-026-69624-5
Mots-clés: thérapie à l’oxyde nitrique, médicaments activés par la lumière, analgésie antibactérienne, nanomédecine, infections à SARM