Clear Sky Science · fr
Cation radical isolable et dication de la dialumène
Pourquoi cette histoire d’aluminium importe
Les chimistes cherchent en permanence des métaux moins coûteux et plus abondants capables d’exécuter les fonctions sophistiquées aujourd’hui assurées par des éléments précieux comme le palladium ou le platine. Cette étude montre que l’aluminium — métal mieux connu pour les canettes et l’aéronautique — peut être amené à former des espèces exceptionnellement réactives qui se comportent un peu comme de minuscules interrupteurs électroniques. Comprendre et maîtriser ces espèces d’aluminium exotiques pourrait, à terme, permettre de développer de nouveaux catalyseurs pour des procédés chimiques et des matériaux plus propres.
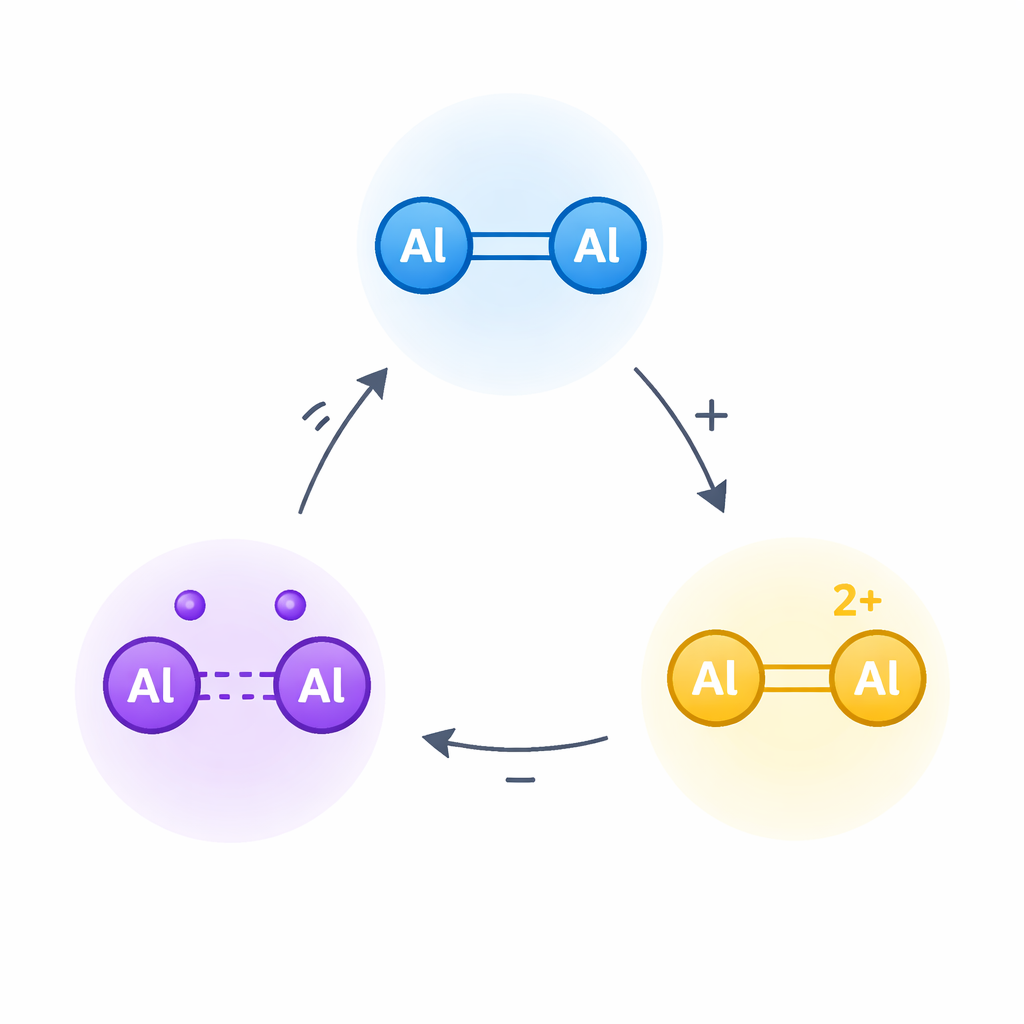
Transformer une liaison familière en commutateur électronique
Le travail porte sur la dialumène, une molécule où deux atomes d’aluminium partagent une double liaison, un peu comme la double liaison carbone–carbone dans les alcènes usuels. Dans les molécules organiques, de telles doubles liaisons peuvent être oxydées par étapes pour donner d’abord des cations radicaux, puis des dications — des formes hautement chargées et très réactives qui sous-tendent de nombreuses réactions en électrochimie et en science des matériaux. Les auteurs se sont demandé si la double liaison aluminium–aluminium de la dialumène pouvait subir une oxydation en deux étapes similaire, malgré le fort appétit électronique de l’aluminium et l’instabilité attendue de telles espèces chargées.
Concevoir un cadre moléculaire protecteur
Pour maîtriser cette réactivité, l’équipe a construit une dialumène entourée de groupes volumineux à base de silicium et de ligands « carbène » fortement donneurs d’électrons. Ils jouent le rôle d’une armure matelassée et de coussins électroniques : ils protègent le cœur aluminium–aluminium délicat des réactions indésirables et aident à fournir la densité électronique nécessaire. À partir de cette dialumène neutre, désignée 1, ils ont utilisé des oxydants choisis avec soin pour enlever d’abord un électron, puis un second, générant un cation radical centré sur l’aluminium (2) puis un dication (3). La cristallographie par rayons X a fourni des instantanés des trois états, révélant comment la liaison aluminium–aluminium s’allonge progressivement et change de nature à mesure que les électrons sont retirés.
Prouver un véritable cycle redox à trois états
Des mesures clés ont confirmé que le cation radical porte réellement un électron non apparié centré entre les deux atomes d’aluminium, et non sur les ligands périphériques. La spectroscopie par résonance paramagnétique électronique a montré un signal net compatible avec un électron unique partagé par les deux centres aluminium. Les études computationnelles confirment ce tableau, indiquant que l’électron liant restant occupe essentiellement un orbital aluminium–aluminium. Lorsque le second électron est retiré pour former le dication, la liaison s’affaiblit vers un caractère de simple liaison et la charge positive s’accumule sur la paire d’aluminium. Fait important, les chercheurs ont montré que tous ces changements sont réversibles : l’ajout d’électrons avec un réducteur régénère d’abord le cation radical puis la dialumène initiale, et le mélange des formes neutre et doublement chargée donne le cation radical par un processus de comproportionnement. Ensemble, ces réactions démontrent un cycle redox robuste et isolable à trois états sur une simple unité aluminium–aluminium.
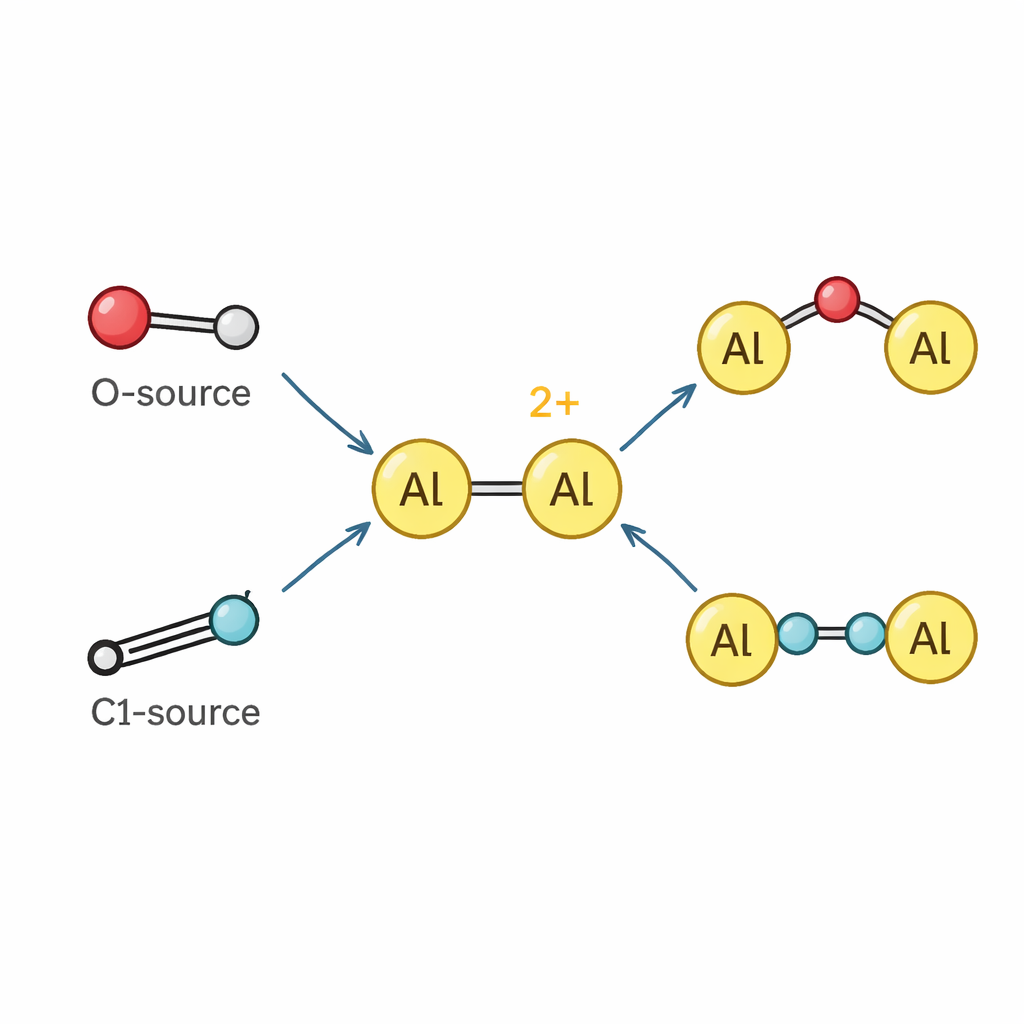
Faire agir l’aluminium comme un métal de transition
Avec le dication en main, l’équipe a exploré ses réactions avec d’autres molécules. Étant donné que ses atomes d’aluminium sont fortement appauvris en électron, le dication se comporte comme un puissant acide de Lewis, se liant facilement à des partenaires basiques tels que la pyridine et des espèces apparentées pour donner de nouveaux complexes dialuminium. Au-delà de la simple coordination, le dication peut cliver et s’insérer dans des liaisons chimiques. Il extrait des atomes d’oxygène de l’oxyde nitreux et de l’oxyde de pyridine, formant des espèces stables où un atome d’oxygène pont entre les deux centres aluminium ou est incorporé dans une courte chaîne aluminium–oxygène–silicium rappelant un petit fragment de réseau zéolitique. Il réagit également avec des isocyanides — petites unités carbone–azote utilisées comme blocs monocarbone — pour les assembler en fragments plus longs N–C–C–N qui s’étendent entre deux atomes d’aluminium, démontrant un exemple rare d’« homologation » d’isocyanides pilotée par un cation d’élément principal.
Ce que cela implique pour la suite
En termes concrets, les chercheurs ont transformé une liaison aluminium–aluminium en un interrupteur électronique à trois positions contrôlable, basculable entre des états neutre, monocationique et dicationique, chacun ayant des géométries et des réactivités distinctes. La version doublement chargée est particulièrement polyvalente, captant des électrons et de petits fragments d’autres molécules de façons habituellement associées aux métaux de transition plus coûteux. En montrant que ce comportement est possible avec l’aluminium et que les états peuvent être interconvertis de manière fiable, ce travail ouvre la voie à la conception de nouveaux catalyseurs et matériaux fonctionnels durables, construits à partir d’un des métaux les plus abondants sur Terre.
Citation: Liu, X., Kostenko, A., Körber, E. et al. Isolable radical cation and dication of dialumene. Nat Commun 17, 1937 (2026). https://doi.org/10.1038/s41467-026-69607-6
Mots-clés: catalyse à l’aluminium, molécules à commutation redox, chimie des éléments principaux, cations radicaux, activation de petites molécules