Clear Sky Science · fr
L’axe Treg–γδ T détermine le dimorphisme sexuel dans l’hépatocarcinogenèse
Pourquoi certains cancers du foie touchent davantage les hommes
Les cliniciens savent depuis longtemps que le cancer du foie frappe les hommes environ deux fois plus souvent que les femmes, mais les raisons vont au‑delà des simples différences hormonales. Cette étude explore les cellules immunitaires présentes dans les tumeurs hépatiques et révèle une conversation cachée entre deux types de cellules T qui aide à expliquer pourquoi le foie des hommes est plus vulnérable — et comment cette connaissance pourrait orienter des traitements nouveaux et mieux ciblés.
La lutte immunitaire au sein des tumeurs hépatiques
Le cancer du foie, en particulier le carcinome hépatocellulaire, se développe dans un micro‑environnement complexe fait de cellules immunitaires, de vaisseaux sanguins et de tissu cicatriciel. Les auteurs ont comparé les tumeurs d’hommes et de femmes, chez des patients et des modèles murins, et ont constaté un déséquilibre frappant : les tumeurs masculines étaient plus riches en cellules T régulatrices, ou Tregs, un type cellulaire qui calme normalement les réactions immunitaires excessives. En revanche, le nombre total des autres cellules T courantes ne variait pas beaucoup entre les sexes. Comme des niveaux élevés de Tregs étaient associés à une survie plus mauvaise, l’équipe a pensé que ces cellules n’étaient pas de simples spectatrices, mais des complices actives aidant les tumeurs à échapper à l’attaque immunitaire. 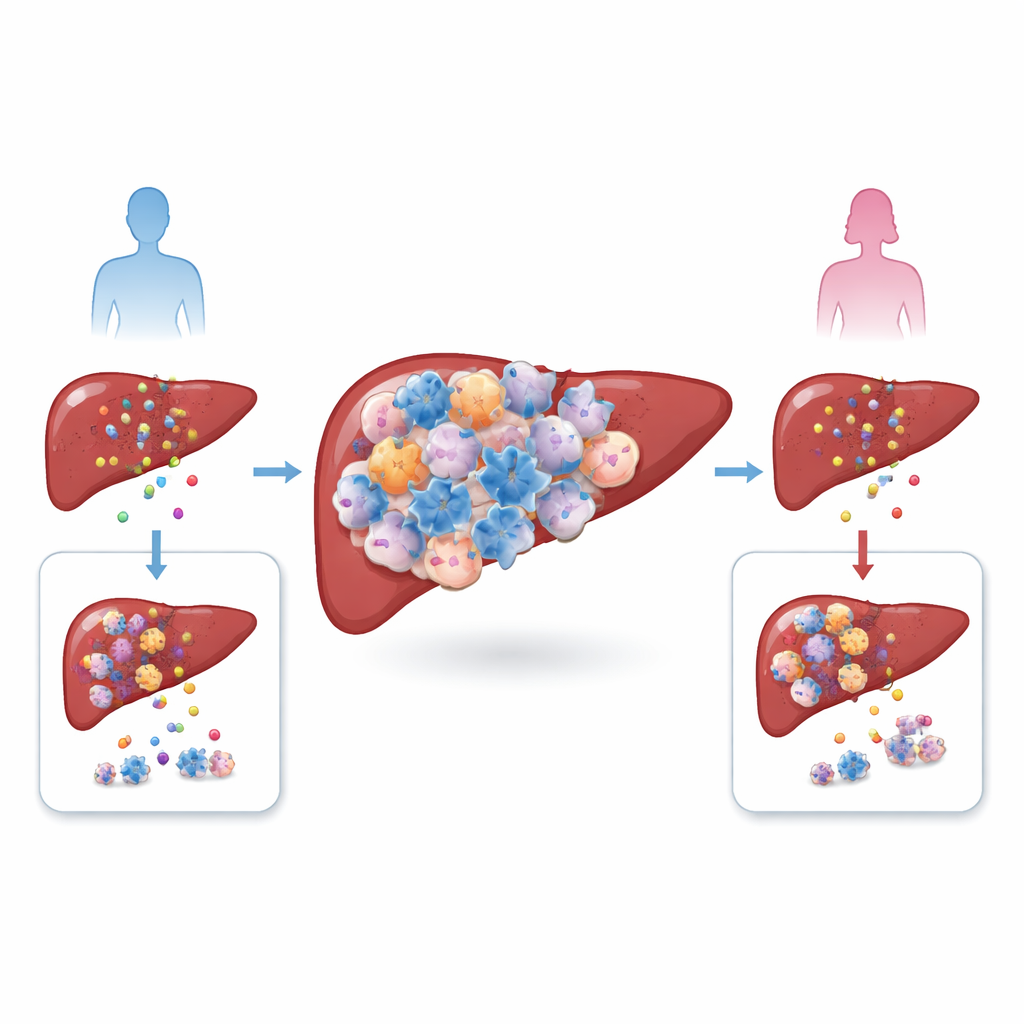
Comment les hormones mâles attirent les cellules suppressives
Pour comprendre pourquoi les tumeurs masculines recrutent davantage de Tregs, les chercheurs se sont intéressés aux signaux chimiques produits par les cellules cancéreuses. Ils ont trouvé que les tumeurs du foie chez l’homme produisaient en plus grande quantité une molécule nommée Ccl2, tandis que les Tregs exprimaient davantage son récepteur correspondant, Ccr2. Cette paire agit comme un signal de guidage, attirant les Tregs dans la tumeur. Lorsque le signal Ccl2 ou le récepteur Ccr2 était supprimé chez la souris, les tumeurs régresseraient et beaucoup moins de Tregs infiltraient le foie, surtout chez les mâles. L’équipe a ensuite montré que la testostérone, principale hormone sexuelle masculine, pilote ce processus : elle active une cascade de protéines dans les cellules tumorales hépatiques qui met en marche le gène Ccl2, renforçant ainsi l’appel chimique qui convoque les Tregs. Les souris mâles castrées, qui produisent moins de testostérone, présentaient des tumeurs avec moins de Ccl2 et moins de Tregs infiltrants.
Des cellules gardiennes qui pourraient combattre le cancer — mais sont bridées
Un autre type de cellule T, connu sous le nom de cellules T gamma‑delta, peut agir comme des « gardiens » à réponse rapide qui reconnaissent et tuent les cellules tumorales sans le recours habituel à la présentation d’antigènes. Dans le foie sain, ces cellules sont relativement rares, mais dans le cancer du foie elles peuvent être des combattantes puissantes. L’étude a montré que les tumeurs féminines contenaient davantage de ces cellules gamma‑delta, qui étaient aussi plus actives et mieux équipées en molécules toxiques. La suppression des hormones sexuelles mâles chez la souris augmentait le nombre et la vigueur des cellules gamma‑delta dans les tumeurs, tandis que les cellules CD8 tueuses classiques restaient pour l’essentiel inchangées. En culture, les cellules gamma‑delta endommageaient facilement les cellules du cancer hépatique, mais cet effet était atténué quand des Tregs étaient ajoutés, ce qui suggère que les Tregs freinent spécifiquement cette population anti‑tumorale prometteuse.
Hypoxie, paquets secrets et défenseurs réduits au silence
En creusant davantage, les chercheurs ont cherché comment les Tregs parviennent à inhiber les cellules gamma‑delta. Dans les tumeurs, l’oxygène fait souvent défaut, un état appelé hypoxie. Dans ces conditions de faible oxygénation, les Tregs des tumeurs masculines commençaient à produire de grandes quantités d’une protéine appelée S100a4. Plutôt que d’agir librement, S100a4 était empaquetée dans de petites particules entourées d’une membrane connues sous le nom de vésicules extracellulaires. Ces vésicules bourgeonnaient à partir des Tregs et étaient captées par les cellules gamma‑delta voisines. Une fois à l’intérieur, S100a4 remodelait les systèmes de régulation génétique des cellules : elle réduisait l’accessibilité des régions d’ADN contrôlant des molécules clés de signalisation et de cytotoxicité et abaissait leur activité. Les cellules gamma‑delta devenaient moins capables de répondre via leurs récepteurs T et moins aptes à libérer protéines toxiques et cytokines, émoussant ainsi leur lame anti‑cancer. 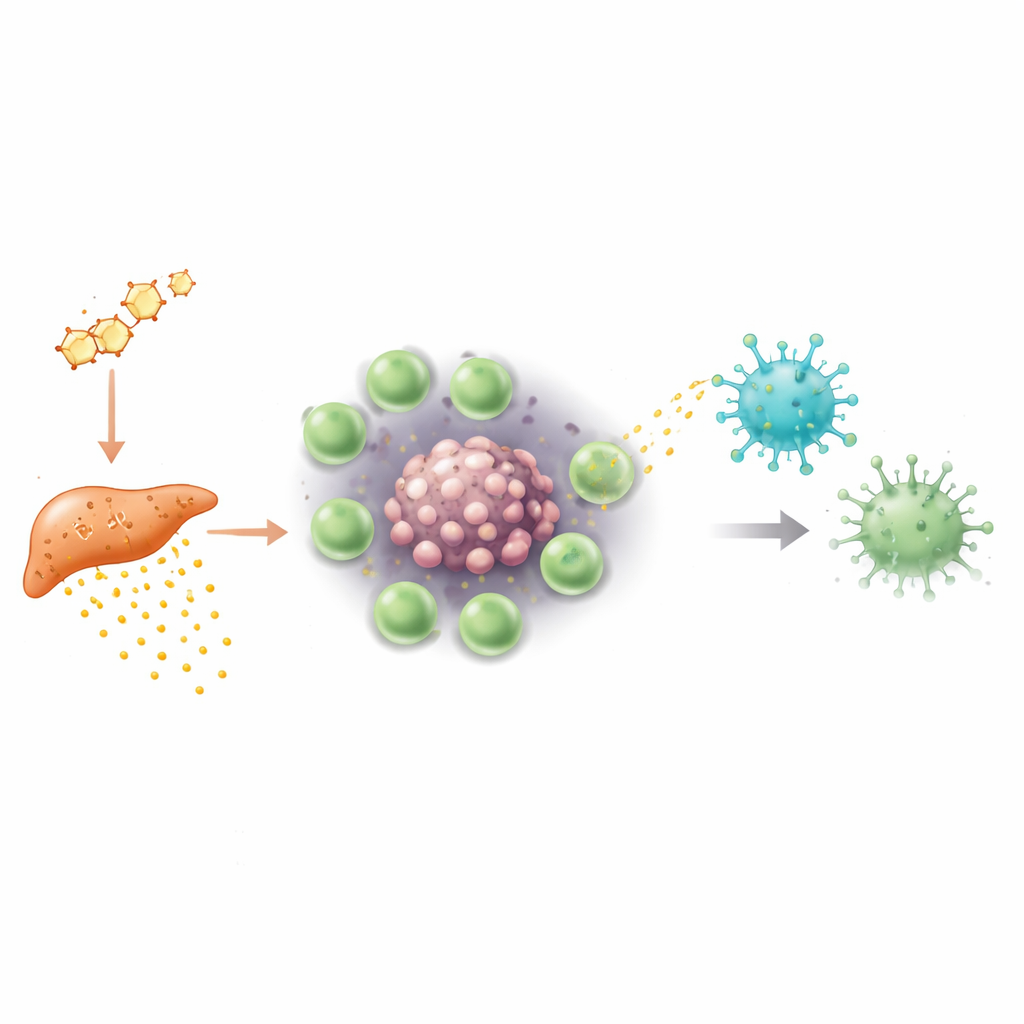
Rompre le circuit délétère
Enfin, l’équipe a testé ce qui se passe si cet axe Treg–S100a4–gamma‑delta est interrompu. Chez des souris génétiquement modifiées pour empêcher les Tregs de produire S100a4, les tumeurs hépatiques masculines ont diminué, le niveau global de S100a4 dans les tumeurs a chuté, et les cellules gamma‑delta sont devenues plus nombreuses et plus actives. Fait notable, le nombre de Tregs dans la tumeur n’a pas baissé — seul leur impact suppressif sur les gamma‑delta a été levé. Ce changement a presque effacé l’écart habituel de gravité tumorale entre souris mâles et femelles, soulignant à quel point cette voie est centrale dans les différences liées au sexe du cancer du foie.
Ce que cela signifie pour les traitements futurs
En termes accessibles, l’étude montre que les hormones mâles incitent les cellules du cancer hépatique à émettre des « signaux d’accueil » renforcés pour les Tregs immunosuppressives. Une fois dans la tumeur — et sous la contrainte de la faible oxygénation — ces Tregs envoient des vésicules remplies de S100a4 qui neutralisent discrètement les cellules gamma‑delta voisines, lesquelles pourraient autrement contenir la progression tumorale. En ciblant soit le signal Ccl2 qui attire les Tregs, soit les messages S100a4 qui réduisent l’activité des gamma‑delta, des thérapies futures pourraient restaurer les défenses naturelles de l’organisme, en particulier chez les hommes. Ce travail suggère que le traitement du cancer du foie pourrait tirer profit d’une approche tenant compte du sexe et d’une valorisation, plutôt que d’une négligence, des points forts uniques des cellules T gamma‑delta.
Citation: Liang, Q., Zhang, Q., Zhang, W. et al. Treg-γδ T cell axis determines sexual dimorphism in hepatocarcinogenesis. Nat Commun 17, 2640 (2026). https://doi.org/10.1038/s41467-026-69603-w
Mots-clés: carcinome hépatocellulaire, cellules T régulatrices, cellules T gamma-delta, differences liées au sexe, immunologie tumorale